Metode instrumentale de analiză în analitică. Metode fizico-chimice sau instrumentale de analiză. Numărul de electroni acceptați mz și nz dați trebuie să fie egal, astfel încât ecuația procesului redox poate fi scrisă ca
Chimie Analitică II. Metode instrumentale de analiză Maystrenko V. N. Bashkir Universitatea de Stat Departamentul de Chimie Analitică [email protected] en Tel: 229 -97 -12
 Chimie analitică - știința determinării compoziției chimice a substanțelor și parțial a structurii lor chimice Metode chimice de analiză Metode fizico-chimice de analiză Metode fizice de analiză Metode instrumentale de analiză
Chimie analitică - știința determinării compoziției chimice a substanțelor și parțial a structurii lor chimice Metode chimice de analiză Metode fizico-chimice de analiză Metode fizice de analiză Metode instrumentale de analiză
 Metode instrumentale de analiză - metode de chimie analitică, care necesită echipamente electrochimice, optice, radiochimice și alte echipamente. Metodele instrumentale de analiză includ: metode electrochimice - potențiometrie (ionometrie), coulometrie, voltametrie, conductometrie etc.; metode bazate pe emisia sau absorbția radiațiilor electromagnetice - emisie, absorbție, spectroscopie atomică și moleculară fluorescentă, metode fotometrice, analiză spectrală cu raze X etc.; analiza spectrală de masă; RMN, EPR, metode bazate pe măsurarea radioactivității etc.
Metode instrumentale de analiză - metode de chimie analitică, care necesită echipamente electrochimice, optice, radiochimice și alte echipamente. Metodele instrumentale de analiză includ: metode electrochimice - potențiometrie (ionometrie), coulometrie, voltametrie, conductometrie etc.; metode bazate pe emisia sau absorbția radiațiilor electromagnetice - emisie, absorbție, spectroscopie atomică și moleculară fluorescentă, metode fotometrice, analiză spectrală cu raze X etc.; analiza spectrală de masă; RMN, EPR, metode bazate pe măsurarea radioactivității etc.
 Definiție y = f(x) х y Semnal analitic Semnal care conține informații cantitative despre valoare, legate funcțional de conținutul analitului, și înregistrat în timpul analizei unei substanțe sau material „Control analitic al obiectului. Termeni și definiții. "
Definiție y = f(x) х y Semnal analitic Semnal care conține informații cantitative despre valoare, legate funcțional de conținutul analitului, și înregistrat în timpul analizei unei substanțe sau material „Control analitic al obiectului. Termeni și definiții. "

 Definiții Măsurarea mărimii y = f(x) х1 хn х2 Definiția substanței Analiza obiectului y 1 y 2 y 3 yn
Definiții Măsurarea mărimii y = f(x) х1 хn х2 Definiția substanței Analiza obiectului y 1 y 2 y 3 yn
 Definiție Semnal, y Funcția de calibrare ∆y α ∆x b tgα = a = ∆y/∆x Concentrație, x y = f(x) y = b + ax
Definiție Semnal, y Funcția de calibrare ∆y α ∆x b tgα = a = ∆y/∆x Concentrație, x y = f(x) y = b + ax
 Definiție y = f(x) х Limita de detectare y Сlim = y 0 + 3σ Concentrație, x
Definiție y = f(x) х Limita de detectare y Сlim = y 0 + 3σ Concentrație, x
 Definiție y = f(x) lgх Limita de detecție y Сlim = y 0 + 3σ Concentrație, lgx
Definiție y = f(x) lgх Limita de detecție y Сlim = y 0 + 3σ Concentrație, lgx
 Definiție y = f(x) х Intervalul concentrațiilor determinate y a = tgα y = ax + b Concentrație, x
Definiție y = f(x) х Intervalul concentrațiilor determinate y a = tgα y = ax + b Concentrație, x

 Metoda şi tehnica analizei Metoda analizei este o metodă destul de universală şi fundamentată teoretic de determinare a compoziţiei, indiferent de componenta care se determină şi (de regulă) obiectul de analizat. Metoda de analiză - o descriere detaliată a analizei unui obiect dat folosind metoda selectată. „Controlul analitic al unui obiect. Termeni și definiții.” GOST R 52361–2005.
Metoda şi tehnica analizei Metoda analizei este o metodă destul de universală şi fundamentată teoretic de determinare a compoziţiei, indiferent de componenta care se determină şi (de regulă) obiectul de analizat. Metoda de analiză - o descriere detaliată a analizei unui obiect dat folosind metoda selectată. „Controlul analitic al unui obiect. Termeni și definiții.” GOST R 52361–2005.
 Metode de chimie analitică Metode de prelevare (prelevare) Metode de descompunere a probei Metode de separare a componentelor Metode de concentrare Metode de detectare (identificare) Metode de determinare
Metode de chimie analitică Metode de prelevare (prelevare) Metode de descompunere a probei Metode de separare a componentelor Metode de concentrare Metode de detectare (identificare) Metode de determinare
 Sample Proba - sau proba - este subiectul cercetării analistului, obiectul luat pentru analiză. Conform GOST: o probă este o parte dintr-o substanță (material) care face obiectul controlului analitic, selectată pentru analiza și/sau studiul structurii sale și/sau determinarea proprietăților, reflectând compoziția și/sau structura sa chimică și/sau sau proprietăți. O probă reprezentativă a unei substanțe sau material care face obiectul controlului analitic este o probă care este identică ca compoziție chimică și/sau proprietăți și/sau structură cu obiectul controlului analitic din care a fost prelevată.
Sample Proba - sau proba - este subiectul cercetării analistului, obiectul luat pentru analiză. Conform GOST: o probă este o parte dintr-o substanță (material) care face obiectul controlului analitic, selectată pentru analiza și/sau studiul structurii sale și/sau determinarea proprietăților, reflectând compoziția și/sau structura sa chimică și/sau sau proprietăți. O probă reprezentativă a unei substanțe sau material care face obiectul controlului analitic este o probă care este identică ca compoziție chimică și/sau proprietăți și/sau structură cu obiectul controlului analitic din care a fost prelevată.
 Clasificarea probelor În funcție de modalitatea de obținere: unică, punctuală (singura, privată), instantanee, zilnică etc. În funcție de stadiul prelucrării primare: inițială, intermediară, combinată, medie, redusă, de laborator, analitică etc. de la numire: control, lucru, rezervă, arbitraj etc.
Clasificarea probelor În funcție de modalitatea de obținere: unică, punctuală (singura, privată), instantanee, zilnică etc. În funcție de stadiul prelucrării primare: inițială, intermediară, combinată, medie, redusă, de laborator, analitică etc. de la numire: control, lucru, rezervă, arbitraj etc.
 Metode absolute și relative de analiză Metodele absolute nu necesită calibrare și probe standard (gravimetrie, coulometrie etc.). Metode relative - parametrii funcției de calibrare se determină experimental (potențiometrie, voltametrie etc.) folosind probe standard.
Metode absolute și relative de analiză Metodele absolute nu necesită calibrare și probe standard (gravimetrie, coulometrie etc.). Metode relative - parametrii funcției de calibrare se determină experimental (potențiometrie, voltametrie etc.) folosind probe standard.
 Metode unidimensionale și multidimensionale Metodele unidimensionale se bazează pe măsurarea intensității semnalului la o singură poziție de măsurare. Semnal, y Metode multivariate - sunt utilizate mai multe poziții de măsurare. Poziția maximului vârfului sau benzii este o caracteristică calitativă. Înălțimea sau aria vârfului este o caracteristică cantitativă. A doua coordonată, z
Metode unidimensionale și multidimensionale Metodele unidimensionale se bazează pe măsurarea intensității semnalului la o singură poziție de măsurare. Semnal, y Metode multivariate - sunt utilizate mai multe poziții de măsurare. Poziția maximului vârfului sau benzii este o caracteristică calitativă. Înălțimea sau aria vârfului este o caracteristică cantitativă. A doua coordonată, z

 Clasificarea metodelor de analiză Clasificare generală calitativ / cantitativ elementar / izotopic / molecular / structural-grup brut / distributiv (local) / real / contact de fază / la distanță distructiv / nedistructiv macro-> 0.1 g semimicro- 0.1 - 0. 01 g micro 0.01 – 0.001 g ultramicro 10 -6 g submicro 10 -9 g macro / semimicro / ultramicro / submicro
Clasificarea metodelor de analiză Clasificare generală calitativ / cantitativ elementar / izotopic / molecular / structural-grup brut / distributiv (local) / real / contact de fază / la distanță distructiv / nedistructiv macro-> 0.1 g semimicro- 0.1 - 0. 01 g micro 0.01 – 0.001 g ultramicro 10 -6 g submicro 10 -9 g macro / semimicro / ultramicro / submicro

 Clasificarea metodelor de analiză După metoda de înregistrare a semnalului Chimic (eroare
Clasificarea metodelor de analiză După metoda de înregistrare a semnalului Chimic (eroare
 Clasificarea metodelor de analiză După metoda de înregistrare a semnalului Chimic (eroare
Clasificarea metodelor de analiză După metoda de înregistrare a semnalului Chimic (eroare
 Clasificarea metodelor de analiză După metoda de înregistrare a semnalului Chimic Fizic Biologic Fizico-chimic Spectroscopic Spectrul de masă Bazat pe radioactivitate Electrochimic Biochimic Termic
Clasificarea metodelor de analiză După metoda de înregistrare a semnalului Chimic Fizic Biologic Fizico-chimic Spectroscopic Spectrul de masă Bazat pe radioactivitate Electrochimic Biochimic Termic
 Prin metoda de măsurare a semnalului Spectroscopie Molecular Atomic Nuclear Metode electrochimice Voltametrie Potențiometrie Conductometrie Coulometrie Cronopotențiometrie, cronoamperometrie
Prin metoda de măsurare a semnalului Spectroscopie Molecular Atomic Nuclear Metode electrochimice Voltametrie Potențiometrie Conductometrie Coulometrie Cronopotențiometrie, cronoamperometrie

 Clasificare După obiectul analizei x După starea de agregare După natura chimică După originea obiectului După gradul de prevalență și importanță După gradul de puritate
Clasificare După obiectul analizei x După starea de agregare După natura chimică După originea obiectului După gradul de prevalență și importanță După gradul de puritate
 Analiza distributivă Analiza distribuției unui element pe suprafață Analiza distribuției unui element pe straturi - adică distribuția în adâncime și în general - în volum. Distribuția fazelor individuale pe suprafață și pe volum
Analiza distributivă Analiza distribuției unui element pe suprafață Analiza distribuției unui element pe straturi - adică distribuția în adâncime și în general - în volum. Distribuția fazelor individuale pe suprafață și pe volum
 Criterii de comparare Caracteristici analitice Caracteristici metrologice Cerințe pentru pregătirea probei Caracteristici ale instrumentarului Cerințe speciale legate de natura obiectului de testat Caracteristici economice
Criterii de comparare Caracteristici analitice Caracteristici metrologice Cerințe pentru pregătirea probei Caracteristici ale instrumentarului Cerințe speciale legate de natura obiectului de testat Caracteristici economice
 Literatură 1. Fundamentele chimiei analitice. Carte. 2. Metode de analiză chimică. / Ed. Yu. A. Zolotova. a 2-a ed. Moscova: Liceu, 2004. 2. Chimie analitică. Metode fizico-fizico-chimice de analiză. Ed. O. M. Petrukhina. Moscova: Chimie, 2001. 3. V. P. Vasiliev, Chimie analitică. Carte. 2. Metode fizico-chimice de analiză. M.: Bustard, 2004. Literatură suplimentară 1. Christian G. Analytical chemistry. În 2 vol. M. : BINOM, 2009. 2. Chimie analitică. Probleme și abordări: În 2 volume / Ed. R. Kellner, J-M. Merme, M. Otto, N. Widmera. M. : Mir, 2004. 3. Otto M. Metode moderne de chimie analitică. În 2 vol. M.: Technosfera, 2003.
Literatură 1. Fundamentele chimiei analitice. Carte. 2. Metode de analiză chimică. / Ed. Yu. A. Zolotova. a 2-a ed. Moscova: Liceu, 2004. 2. Chimie analitică. Metode fizico-fizico-chimice de analiză. Ed. O. M. Petrukhina. Moscova: Chimie, 2001. 3. V. P. Vasiliev, Chimie analitică. Carte. 2. Metode fizico-chimice de analiză. M.: Bustard, 2004. Literatură suplimentară 1. Christian G. Analytical chemistry. În 2 vol. M. : BINOM, 2009. 2. Chimie analitică. Probleme și abordări: În 2 volume / Ed. R. Kellner, J-M. Merme, M. Otto, N. Widmera. M. : Mir, 2004. 3. Otto M. Metode moderne de chimie analitică. În 2 vol. M.: Technosfera, 2003.
 Metode instrumentale de analiză: spectre ale atomilor și moleculelor Maistrenko V. N. Bashkir State University Departamentul de chimie analitică [email protected] en Tel: 229 -97 -12
Metode instrumentale de analiză: spectre ale atomilor și moleculelor Maistrenko V. N. Bashkir State University Departamentul de chimie analitică [email protected] en Tel: 229 -97 -12
 În arsenalul chimiei analitice moderne, locul cel mai important îl ocupă metodele spectroscopiei optice atomice, bazate pe măsurarea intensității radiațiilor electromagnetice emise sau absorbite de atomii elementelor aflate în stare de gaz sau vapori. Aceste metode sunt multi-element și sunt utilizate pe scară largă pentru a determina compoziția diferitelor obiecte - aliaje, minerale, minereuri, produse alimentare, obiecte de mediu etc.
În arsenalul chimiei analitice moderne, locul cel mai important îl ocupă metodele spectroscopiei optice atomice, bazate pe măsurarea intensității radiațiilor electromagnetice emise sau absorbite de atomii elementelor aflate în stare de gaz sau vapori. Aceste metode sunt multi-element și sunt utilizate pe scară largă pentru a determina compoziția diferitelor obiecte - aliaje, minerale, minereuri, produse alimentare, obiecte de mediu etc.

 Istoria analizei spectrale atomice a început cu experimentele lui Isaac Newton (1666) privind descompunerea luminii într-un spectru. Primele spectre atomice au fost observate la începutul secolului al XIX-lea în cursul cercetărilor astronomice. Apariția analizei spectrale ca metodă de determinare a compoziției chimice a unei substanțe datează din 1859, când oamenii de știință germani G. Kirchhoff și R. Bunsen, studiind comportamentul sărurilor metalice în flacără, au observat apariția liniilor în spectre. de elemente. Gustav Kirchhoff (stânga) și Robert Bunsen (dreapta) Kirchhoff și spectroscopul Bunsen
Istoria analizei spectrale atomice a început cu experimentele lui Isaac Newton (1666) privind descompunerea luminii într-un spectru. Primele spectre atomice au fost observate la începutul secolului al XIX-lea în cursul cercetărilor astronomice. Apariția analizei spectrale ca metodă de determinare a compoziției chimice a unei substanțe datează din 1859, când oamenii de știință germani G. Kirchhoff și R. Bunsen, studiind comportamentul sărurilor metalice în flacără, au observat apariția liniilor în spectre. de elemente. Gustav Kirchhoff (stânga) și Robert Bunsen (dreapta) Kirchhoff și spectroscopul Bunsen

 Experimentul Bunsen-Kirchhoff A - cutie de trabucuri, B - parte dintr-un telescop, C - telescop, D - arzător cu gaz Bunsen, E - trepied cu sare de sodiu, F - prismă de sticlă cu CS 2, G - oglindă, H - dispozitiv rotativ
Experimentul Bunsen-Kirchhoff A - cutie de trabucuri, B - parte dintr-un telescop, C - telescop, D - arzător cu gaz Bunsen, E - trepied cu sare de sodiu, F - prismă de sticlă cu CS 2, G - oglindă, H - dispozitiv rotativ
 Context istoric Sfârșitul secolului al XX-lea Anii 1960 AAS, ICP AES ICP-MS Anii 20 ai secolului XX Mijlocul secolului al XIX-lea Metode de analiză cantitativă Analiză calitativă și semi-cantitativă
Context istoric Sfârșitul secolului al XX-lea Anii 1960 AAS, ICP AES ICP-MS Anii 20 ai secolului XX Mijlocul secolului al XIX-lea Metode de analiză cantitativă Analiză calitativă și semi-cantitativă
 Spectrele atomilor Atomii elementelor chimice au frecvente strict definite la care emit sau absorb lumina. În același timp, în spectrele elementelor din anumite locuri se observă linii luminoase sau întunecate, caracteristice fiecărui element. Spectrele atomice se obțin prin transferul substanțelor în stare de vapori prin încălzire la 1000-10000 ° C. Ca surse de excitație a atomilor sunt folosite o scânteie, un arc de curent alternativ, o flacără sau o plasmă de diferite gaze, lasere etc.. Spectrele de absorbție și emisie ale atomilor de sodiu
Spectrele atomilor Atomii elementelor chimice au frecvente strict definite la care emit sau absorb lumina. În același timp, în spectrele elementelor din anumite locuri se observă linii luminoase sau întunecate, caracteristice fiecărui element. Spectrele atomice se obțin prin transferul substanțelor în stare de vapori prin încălzire la 1000-10000 ° C. Ca surse de excitație a atomilor sunt folosite o scânteie, un arc de curent alternativ, o flacără sau o plasmă de diferite gaze, lasere etc.. Spectrele de absorbție și emisie ale atomilor de sodiu



 Liniile spectrale caracterizează frecvența radiației, care corespunde tranziției cuantice dintre nivelurile de energie Еi și Еk ale atomului conform relației h = Еi - Еk, unde h este constanta lui Planck, precum și lungimea de undă = c / (c). este viteza luminii), numărul de undă ' = 1 / și energia fotonului h. Frecvențele liniilor spectrale sunt exprimate în secunde reciproce (s-1), lungimi de undă - în nm, microni și angstromi, numere de undă - în centimetri reciproci (cm-1), energia fotonului în electroni volți (e. V). Spectrele de emisie (emisia) sunt obținute prin excitarea atomilor în diferite moduri. Durata de viață a stării excitate este de 10 -7 - 10 -8 s. În acest timp, atomul emite o cantitate de radiație electromagnetică și intră într-o stare cu o energie mai mică. Spectrele de absorbție (absorbția) se observă în timpul trecerii radiațiilor electromagnetice, care au un spectru continuu, prin vapori sau gaze ale atomilor. Apariția spectrelor optice și natura lor este determinată de sistemul de electroni atomici, care se caracterizează prin patru numere cuantice: numărul cuantic principal (nivelele K, L, M, N…Q), numărul cuantic orbital (subnivelurile s, p). , d, f…), numere cuantice magnetice și spin.
Liniile spectrale caracterizează frecvența radiației, care corespunde tranziției cuantice dintre nivelurile de energie Еi și Еk ale atomului conform relației h = Еi - Еk, unde h este constanta lui Planck, precum și lungimea de undă = c / (c). este viteza luminii), numărul de undă ' = 1 / și energia fotonului h. Frecvențele liniilor spectrale sunt exprimate în secunde reciproce (s-1), lungimi de undă - în nm, microni și angstromi, numere de undă - în centimetri reciproci (cm-1), energia fotonului în electroni volți (e. V). Spectrele de emisie (emisia) sunt obținute prin excitarea atomilor în diferite moduri. Durata de viață a stării excitate este de 10 -7 - 10 -8 s. În acest timp, atomul emite o cantitate de radiație electromagnetică și intră într-o stare cu o energie mai mică. Spectrele de absorbție (absorbția) se observă în timpul trecerii radiațiilor electromagnetice, care au un spectru continuu, prin vapori sau gaze ale atomilor. Apariția spectrelor optice și natura lor este determinată de sistemul de electroni atomici, care se caracterizează prin patru numere cuantice: numărul cuantic principal (nivelele K, L, M, N…Q), numărul cuantic orbital (subnivelurile s, p). , d, f…), numere cuantice magnetice și spin.

 Spectrul Set de linii spectrale aparținând unei particule date Excitație termică Spectru de emisie Excitație non-termică Spectru de luminescență Rapid (spontan) Spectru de fluorescență (atomi și molecule) Spectru de fosforescență lent (molecule)
Spectrul Set de linii spectrale aparținând unei particule date Excitație termică Spectru de emisie Excitație non-termică Spectru de luminescență Rapid (spontan) Spectru de fluorescență (atomi și molecule) Spectru de fosforescență lent (molecule)
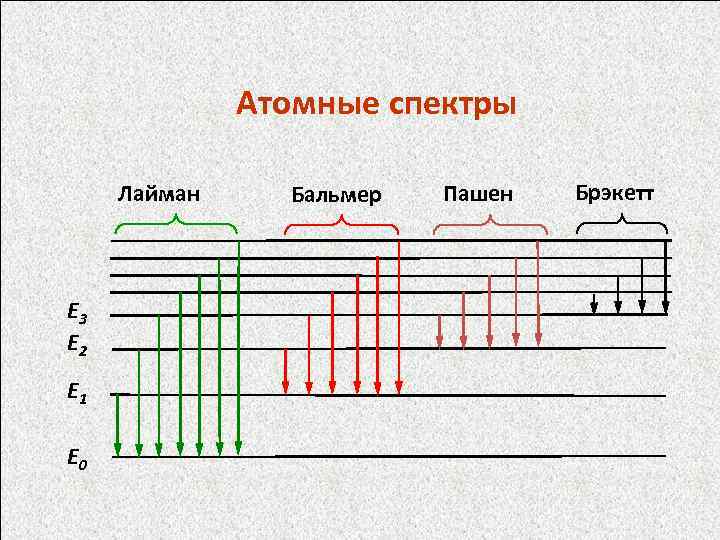
 Spectrele atomilor cu un număr mic de electroni de valență (metale alcaline, hidrogen) au relativ puține linii (mai puțin de 100) în intervalul 200 - 800 nm. Atomii cu învelișuri de electroni mai complexe (elemente ale grupurilor laterale) au spectre cu un număr mare de linii (Cu - mai mult de 500, Fe - mai mult de 3000, U - câteva mii). Liniile datorate tranziției electronilor la nivelul de energie al solului sunt numite rezonante. Datorită intensității lor mari, oferă cea mai mare sensibilitate a determinărilor și sunt utilizate în scopuri analitice. Pentru a excita liniile de rezonanță ale metalelor alcaline, este necesară o energie mică, în timp ce pentru nemetale este mare, iar spectrele sunt deplasate din regiunea vizibilă în regiunea ultravioletă greu de atins: pentru Na - 589 nm, Mg - 285 nm, Si - 251 nm, P - 176 nm. Domeniul principal de aplicare al spectroscopiei atomice este determinarea elementelor cu proprietăți metalice și semimetalice. Pentru a obține informații cantitative, se măsoară intensitatea uneia dintre liniile spectrale ale elementului care se determină. Procesele care au loc cu un atom în timpul absorbției sau emiterii unui foton sunt descrise folosind termeni spectrale care caracterizează starea energetică a atomului absorbant sau emițător. Termenii spectrale sunt obținuți prin adăugarea vectorială a momentului orbital și a spinurilor tuturor electronilor dintr-un atom.
Spectrele atomilor cu un număr mic de electroni de valență (metale alcaline, hidrogen) au relativ puține linii (mai puțin de 100) în intervalul 200 - 800 nm. Atomii cu învelișuri de electroni mai complexe (elemente ale grupurilor laterale) au spectre cu un număr mare de linii (Cu - mai mult de 500, Fe - mai mult de 3000, U - câteva mii). Liniile datorate tranziției electronilor la nivelul de energie al solului sunt numite rezonante. Datorită intensității lor mari, oferă cea mai mare sensibilitate a determinărilor și sunt utilizate în scopuri analitice. Pentru a excita liniile de rezonanță ale metalelor alcaline, este necesară o energie mică, în timp ce pentru nemetale este mare, iar spectrele sunt deplasate din regiunea vizibilă în regiunea ultravioletă greu de atins: pentru Na - 589 nm, Mg - 285 nm, Si - 251 nm, P - 176 nm. Domeniul principal de aplicare al spectroscopiei atomice este determinarea elementelor cu proprietăți metalice și semimetalice. Pentru a obține informații cantitative, se măsoară intensitatea uneia dintre liniile spectrale ale elementului care se determină. Procesele care au loc cu un atom în timpul absorbției sau emiterii unui foton sunt descrise folosind termeni spectrale care caracterizează starea energetică a atomului absorbant sau emițător. Termenii spectrale sunt obținuți prin adăugarea vectorială a momentului orbital și a spinurilor tuturor electronilor dintr-un atom.
Src="https://present5.com/presentation/89020358_158004652/image-47.jpg" alt="(!LANG:Termeni spectrali Formula Balmer (m > n) Seria Lyman n = 1 serie Balmer:"> Спектральные термы Формула Бальмера (m > n) Серия Лаймана n = 1 Серия Бальмера: n = 2 Серия Пашена: n = 3 Серия Брэкетта: n = 4 Терм: Спектральный терм: R = 109 677 см− 1 – постоянная Ридберга, m – целые числа.!}

 Termenii spectrali ai atomilor multielectroni Luând în considerare sarcina nucleară: He+, Li 2+, Be 3+ Luând în considerare momentul unghiular orbital total și spin total
Termenii spectrali ai atomilor multielectroni Luând în considerare sarcina nucleară: He+, Li 2+, Be 3+ Luând în considerare momentul unghiular orbital total și spin total

 Lungimi de undă ale radiației electromagnetice Domeniul lungimii de undă Secțiunea spectrului 10 -4 - 0,1 nm radiații γ 0,01 - 10 nm radiații X 10 - 400 nm radiații ultraviolete 400 - 760 nm Lumină vizibilă 760 - 106 -10 nm radiații infraroșii m Microunde (MW) >1 m Unde radio
Lungimi de undă ale radiației electromagnetice Domeniul lungimii de undă Secțiunea spectrului 10 -4 - 0,1 nm radiații γ 0,01 - 10 nm radiații X 10 - 400 nm radiații ultraviolete 400 - 760 nm Lumină vizibilă 760 - 106 -10 nm radiații infraroșii m Microunde (MW) >1 m Unde radio
 Intensitatea liniei spectrale Energie absorbită, emisă sau disipată pe unitatea de timp Spectrul de emisie: spectroscopie cu raze X, AES, APS Spectru de absorbție: AAS, UV-Vis, IR, spectroscopie cu microunde și RF
Intensitatea liniei spectrale Energie absorbită, emisă sau disipată pe unitatea de timp Spectrul de emisie: spectroscopie cu raze X, AES, APS Spectru de absorbție: AAS, UV-Vis, IR, spectroscopie cu microunde și RF
 Lățimea liniei spectrale UV natural: 10 -5 nm mișcare termică (lărgire Doppler) UV: 10 -3 -10 -2 nm coliziunea particulelor (largirea Lorentz) împărțirea nivelurilor de energie într-un câmp magnetic (efectul Zeeman)
Lățimea liniei spectrale UV natural: 10 -5 nm mișcare termică (lărgire Doppler) UV: 10 -3 -10 -2 nm coliziunea particulelor (largirea Lorentz) împărțirea nivelurilor de energie într-un câmp magnetic (efectul Zeeman)
 SPECTRE MOLECULARE - spectre de absorbție, emisie sau împrăștiere care decurg din tranzițiile cuantice ale moleculelor de la o stare energetică la alta. Spectrele moleculare sunt determinate de compoziția moleculelor, structura lor, natura legăturilor chimice și interacțiunile cu atomii și moleculele din jur. Cele mai caracteristice sunt spectrele moleculare ale moleculelor de gaze rarefiate, care constau din linii înguste. Spectrele moleculare constau din spectre electronice, vibraționale și rotaționale și se află în domeniul undelor electromagnetice de la frecvențe radio până la regiunea de raze X a spectrului. Frecvențele tranzițiilor între nivelurile de energie de rotație se încadrează de obicei în regiunea microundelor, frecvențele tranzițiilor între nivelurile vibraționale - în regiunea IR și frecvențele tranzițiilor între nivelurile electronice - în regiunile vizibil și UV ale spectrului. Tranzițiile de rotație cad adesea în regiunea IR, tranzițiile vibraționale în regiunea vizibilă și tranzițiile electronice în regiunea IR. Tranzițiile electronice sunt însoțite de o modificare a energiei vibraționale a moleculelor, în timp ce tranzițiile vibraționale modifică energia de rotație. Prin urmare, spectrele electronice reprezintă de obicei benzi electronice de vibrație. La rezoluție mare, este detectată și structura rotațională.
SPECTRE MOLECULARE - spectre de absorbție, emisie sau împrăștiere care decurg din tranzițiile cuantice ale moleculelor de la o stare energetică la alta. Spectrele moleculare sunt determinate de compoziția moleculelor, structura lor, natura legăturilor chimice și interacțiunile cu atomii și moleculele din jur. Cele mai caracteristice sunt spectrele moleculare ale moleculelor de gaze rarefiate, care constau din linii înguste. Spectrele moleculare constau din spectre electronice, vibraționale și rotaționale și se află în domeniul undelor electromagnetice de la frecvențe radio până la regiunea de raze X a spectrului. Frecvențele tranzițiilor între nivelurile de energie de rotație se încadrează de obicei în regiunea microundelor, frecvențele tranzițiilor între nivelurile vibraționale - în regiunea IR și frecvențele tranzițiilor între nivelurile electronice - în regiunile vizibil și UV ale spectrului. Tranzițiile de rotație cad adesea în regiunea IR, tranzițiile vibraționale în regiunea vizibilă și tranzițiile electronice în regiunea IR. Tranzițiile electronice sunt însoțite de o modificare a energiei vibraționale a moleculelor, în timp ce tranzițiile vibraționale modifică energia de rotație. Prin urmare, spectrele electronice reprezintă de obicei benzi electronice de vibrație. La rezoluție mare, este detectată și structura rotațională.

 Spectrele moleculare ale substanțelor: a - contur neted, b - urme ale structurii vibraționale, c - spectrul de absorbție al vaporilor de antracen cu o structură vibrațională clară
Spectrele moleculare ale substanțelor: a - contur neted, b - urme ale structurii vibraționale, c - spectrul de absorbție al vaporilor de antracen cu o structură vibrațională clară
 Spectrele electronice ale moleculelor Spectrele electronice se datorează tranzițiilor între nivelurile de energie electronică. Cum sunt definite spectrele electronice? Pentru atomii cu configurația electronică a atomilor Pentru moleculele cu configurația electronică a moleculelor Tranzițiile electronice în molecule au, de regulă, energii corespunzătoare regiunilor UV și vizibile ale spectrului electromagnetic.
Spectrele electronice ale moleculelor Spectrele electronice se datorează tranzițiilor între nivelurile de energie electronică. Cum sunt definite spectrele electronice? Pentru atomii cu configurația electronică a atomilor Pentru moleculele cu configurația electronică a moleculelor Tranzițiile electronice în molecule au, de regulă, energii corespunzătoare regiunilor UV și vizibile ale spectrului electromagnetic.


 Spectrele moleculare vibraționale se datorează tranzițiilor cuantice între nivelurile de energie vibrațională ale moleculelor. Observați experimental spectrele de absorbție IR și spectrele Raman (spectre Raman) ale energiei primite. În cel mai simplu caz, o moleculă diatomică este reprezentată printr-un model de două mase punctuale care interacționează M 1 și M 2. În timpul tranziției între nivelurile vibraționale învecinate este absorbit un foton cu energie h = Ev+1 – Ev și frecvență. F
Spectrele moleculare vibraționale se datorează tranzițiilor cuantice între nivelurile de energie vibrațională ale moleculelor. Observați experimental spectrele de absorbție IR și spectrele Raman (spectre Raman) ale energiei primite. În cel mai simplu caz, o moleculă diatomică este reprezentată printr-un model de două mase punctuale care interacționează M 1 și M 2. În timpul tranziției între nivelurile vibraționale învecinate este absorbit un foton cu energie h = Ev+1 – Ev și frecvență. F
 Există două tipuri principale de vibrații în molecule: valența (), în care atomii oscilează de-a lungul legăturilor, - legăturile se întind alternativ, apoi se scurtează (vibrații simetrice și asimetrice); deformare (), la care se modifică unghiurile de legătură dintre legăturile unui atom (foarfecă, pendul, evantai, vibrații de torsiune). Valenta simetrica (s) Deformare antisimetrica (as) (pendul) Valenta antisimetrica (as), (a) Deformare ventilator () Deformare simetrica (s) (foarfeca) Deformare torsionala ()
Există două tipuri principale de vibrații în molecule: valența (), în care atomii oscilează de-a lungul legăturilor, - legăturile se întind alternativ, apoi se scurtează (vibrații simetrice și asimetrice); deformare (), la care se modifică unghiurile de legătură dintre legăturile unui atom (foarfecă, pendul, evantai, vibrații de torsiune). Valenta simetrica (s) Deformare antisimetrica (as) (pendul) Valenta antisimetrica (as), (a) Deformare ventilator () Deformare simetrica (s) (foarfeca) Deformare torsionala ()
 Vibrații normale ale unei molecule de apă (s) = 3652 cm-1 (as) = 3756 cm-1 N = 3 n-6 = 3 x 3 – 6 = 3 (s) = 1595 cm-1
Vibrații normale ale unei molecule de apă (s) = 3652 cm-1 (as) = 3756 cm-1 N = 3 n-6 = 3 x 3 – 6 = 3 (s) = 1595 cm-1
 Frecvența de vibrație depinde de masa atomilor (atom mai ușor - frecvență mai mare) C - H 3000 cm-1 C - D 2200 cm-1 C - O 1100 cm-1 C - Cl 700 cm-1 Frecvența de vibrație depinde de energie de legătură (legatura este mai puternică - frecvență mai mare) C C 2143 cm-1 C = O 1715 cm-1 C - O 1100 cm-1
Frecvența de vibrație depinde de masa atomilor (atom mai ușor - frecvență mai mare) C - H 3000 cm-1 C - D 2200 cm-1 C - O 1100 cm-1 C - Cl 700 cm-1 Frecvența de vibrație depinde de energie de legătură (legatura este mai puternică - frecvență mai mare) C C 2143 cm-1 C = O 1715 cm-1 C - O 1100 cm-1
 Frecvențe tipice de vibrație ale grupurilor funcționale, cm-1 Grup Domeniu de frecvență Vibrații de întindere Grup Domeniu de frecvență Vibrații de deformare (O – H) 3600 – 3000 (O – H), (N – H) 1650 – 1550 (C C), (C N) 2400 – 2100 (C - H) 1450 - 1250 (P - H), (C - H) 2250 - 2100 (C - O), (C - N) 1300 - 1000 (C = O) 1850 - 1650 (C - H) ), (N - H) 950 - 800 (C = C), (N = O) 1750 - 1600 (Si - O), (P = O) 700 - 550 (N = N) 1650 - 1450 (S - O) ) 650 - 450 (Si - O), (P = O) 1300 - 1000 (S - O) 1000 - 800 (C - CI) 750 - 690
Frecvențe tipice de vibrație ale grupurilor funcționale, cm-1 Grup Domeniu de frecvență Vibrații de întindere Grup Domeniu de frecvență Vibrații de deformare (O – H) 3600 – 3000 (O – H), (N – H) 1650 – 1550 (C C), (C N) 2400 – 2100 (C - H) 1450 - 1250 (P - H), (C - H) 2250 - 2100 (C - O), (C - N) 1300 - 1000 (C = O) 1850 - 1650 (C - H) ), (N - H) 950 - 800 (C = C), (N = O) 1750 - 1600 (Si - O), (P = O) 700 - 550 (N = N) 1650 - 1450 (S - O) ) 650 - 450 (Si - O), (P = O) 1300 - 1000 (S - O) 1000 - 800 (C - CI) 750 - 690


 Literatură 1. Fundamentele chimiei analitice. Carte. 2. Metode de analiză chimică. / Ed. Yu. A. Zolotova. a 2-a ed. Moscova: Liceu, 2004. 2. Chimie analitică. Metode fizico-fizico-chimice de analiză. Ed. O. M. Petrukhina. Moscova: Chimie, 2001. 3. V. P. Vasiliev, Chimie analitică. Carte. 2. Metode fizico-chimice de analiză. M.: Bustard, 2004. Literatură suplimentară 1. Christian G. Analytical chemistry. În 2 vol. M. : BINOM, 2009. 2. Chimie analitică. Probleme și abordări: În 2 volume / Ed. R. Kellner, J-M. Merme, M. Otto, N. Widmera. M. : Mir, 2004. 3. Otto M. Metode moderne de chimie analitică. În 2 vol. M. : Tekhnosfera, 2003. 4. Yu. Ya. Kuzyakov, K. A. Semenenko, N. B. Zorov, Methods of Spectral Analysis. M. : MGU, 1990. 5. Kazitsyna L. A., Kupletskaya N. B. Aplicarea spectroscopiei UV, IR și RMN în chimia organică. M. : Liceu, 1971.
Literatură 1. Fundamentele chimiei analitice. Carte. 2. Metode de analiză chimică. / Ed. Yu. A. Zolotova. a 2-a ed. Moscova: Liceu, 2004. 2. Chimie analitică. Metode fizico-fizico-chimice de analiză. Ed. O. M. Petrukhina. Moscova: Chimie, 2001. 3. V. P. Vasiliev, Chimie analitică. Carte. 2. Metode fizico-chimice de analiză. M.: Bustard, 2004. Literatură suplimentară 1. Christian G. Analytical chemistry. În 2 vol. M. : BINOM, 2009. 2. Chimie analitică. Probleme și abordări: În 2 volume / Ed. R. Kellner, J-M. Merme, M. Otto, N. Widmera. M. : Mir, 2004. 3. Otto M. Metode moderne de chimie analitică. În 2 vol. M. : Tekhnosfera, 2003. 4. Yu. Ya. Kuzyakov, K. A. Semenenko, N. B. Zorov, Methods of Spectral Analysis. M. : MGU, 1990. 5. Kazitsyna L. A., Kupletskaya N. B. Aplicarea spectroscopiei UV, IR și RMN în chimia organică. M. : Liceu, 1971.

Metodele instrumentale (fizice și fizico-chimice) de analiză se bazează pe utilizarea relației dintre proprietățile fizice măsurate ale substanțelor și compoziția lor calitativă și cantitativă. Deoarece proprietățile fizice ale substanțelor sunt măsurate folosind diverse instrumente - „instrumente”, aceste metode de analiză sunt numite și metode instrumentale.
Numărul total de metode fizico-chimice de analiză este destul de mare - se ridică la câteva zeci. Cele mai importante dintre ele sunt următoarele:
metode optice, bazat pe măsurarea proprietăților optice ale substanțelor;
metode electrochimice, bazat pe măsurarea proprietăților electrochimice ale sistemului;
metode cromatografice, bazat pe utilizarea capacității diferitelor substanțe de sorbție selectivă.
Dintre aceste grupuri, cel mai extins din punct de vedere al numărului de metode și important din punct de vedere al semnificației practice este grupul metode optice de analiză .
Analiza spectrală a emisiilor. Metoda se bazează pe măsurarea intensității luminii emise de o substanță (atomi sau ioni) în timpul excitației energetice a acesteia, de exemplu, într-o plasmă cu descărcare electrică. Metoda face posibilă determinarea micro- și ultramicro-cantităților unei substanțe, analiza mai multor elemente într-un timp scurt.
Fotometria flacara este un tip de analiză a emisiilor. Se bazează pe utilizarea unei flăcări de gaz ca sursă de excitare a energiei radiației. Metoda este utilizată în principal pentru analiza metalelor alcaline și alcalino-pământoase.
Analiza spectrală de absorbție se bazează pe studiul spectrelor de absorbţie a razelor de către substanţele analizate. Când trece printr-o soluție, lumina sau componentele sale sunt absorbite sau reflectate. Natura și concentrația substanței este judecată după mărimea absorbției sau reflectării razelor.
Analiza absorbției atomice. Metoda se bazează pe măsurarea absorbției radiațiilor monocromatice de către atomii analitului în faza gazoasă după atomizarea substanței.
Analiza nefelometrică. Se bazează pe reflectarea luminii de către particulele solide suspendate într-o soluție. Analiza se efectuează cu instrumente nefelometrice.
Analiza luminiscentă- Acesta este un set de metode optice de analiză bazate pe luminescență (strălucirea unei substanțe care apare atunci când este excitată de diverse surse de energie). Conform metodei (sursei) de excitație, există: luminescență cu raze X - strălucirea unei substanțe sub influența razelor X; X emiluminiscență - luminiscența unei substanțe datorită energiei unei reacții chimice.
În practica analitică, dintre toate tipurile de luminescență, fluorescența, care apare sub acțiunea radiațiilor în regiunile spectrale UV și vizibile, este cea mai utilizată. Un mare avantaj al metodei de fluorescență cu raze X este posibilitatea de a analiza o probă fără a o distruge, ceea ce este deosebit de valoros atunci când se analizează produse unice.
Metode electrochimice de analiză se bazează pe studiul și utilizarea proceselor care au loc pe suprafața electrodului sau în spațiul apropiat de electrod. Un semnal analitic poate fi orice parametru electric (potențial, puterea curentului, rezistența etc.), care este legat de concentrația soluției analizate printr-o dependență funcțională și măsurabilă.
Există metode electrochimice directe și indirecte.
LA metode directe se folosește dependența puterii curentului (potențial etc.) de concentrația componentei determinate. LA metode indirecte puterea curentului (potenţialul etc.) este măsurată pentru a găsi componenta fiind determinată de un titrant adecvat, adică se utilizează dependenţa parametrului măsurat de volumul titrantului.
Cele mai comune metode electrochimice de analiză sunt potențiometrice, voltametrice și conductometrice.
Metoda potențiometrică se bazează pe măsurarea potențialelor electrodului, care depind de activitatea ionilor, iar în soluții diluate - de concentrația ionilor.
Pentru măsurători, o celulă galvanică este formată din doi electrozi: un electrod de referință (al cărui potențial electrod este cunoscut) și un electrod indicator, pe care are loc procesul principal - schimbul de ioni și apare un potențial de electrod, care este măsurat prin comparaţie. Apoi, conform ecuației Nernst, se găsește cantitatea componentei determinate.
Titrare potențiometrică pe baza determinării punctului de echivalență din rezultatele măsurătorilor potențiometrice. În apropierea punctului de echivalență, există o schimbare bruscă (salt) a potențialului electrodului indicator.
Pentru titrarea potențiometrică, un circuit este asamblat dintr-un electrod indicator în soluția analizată și un electrod de referință. Electrozii de referință cei mai des utilizați sunt calomelul sau clorura de argint.
Metoda voltametrică de analiză pe baza studiului polarizării sau curbe curent-tensiune(curbe de dependență a intensității curentului de tensiune), care se obțin dacă, în timpul electrolizei unei soluții de analit, tensiunea este crescută treptat și puterea curentului este fixată. Electroliza trebuie efectuată folosind un electrod ușor polarizabil cu o suprafață mică, pe care are loc electroreducerea sau electrooxidarea substanței.
Titrare amperometrică(titrare cu polarizare potențiometrică) - un fel de metodă voltametrică (împreună cu polarografie). Se bazează pe măsurarea mărimii curentului dintre electrozii unei celule electrochimice, căreia i se aplică o anumită tensiune, corespunzătoare mărimii curentului de limitare. Pe baza acestor date, se construiește o curbă de titrare amperometrică în coordonatele „putere curentă - volum de titrant” și se găsește grafic punctul de echivalență. Ca electrod indicator în titrarea amperometrică, se folosesc de obicei electrozi rotativi de platină, grafit și alți solizi.
Exemple de rezolvare a problemelor
Exemplul 1În timpul descoperirii cationilor de argint Ag + prin reacția cu ionii de clorură Cl - într-o soluție apoasă pentru a forma un precipitat alb de clorură de argint AgCl
Ag ++ Cl – ® AgCl↓
limita de detecție a cationilor de argint este de 0,1 μg, limitând diluția V lim = 1∙104 ml/g. Determinați concentrația limită Cu lim și volum minim V min de soluție extrem de diluată.
Decizie. Să găsim concentrația limită Cu min:
C min = = = 1 ∙ 10 -4 g/ml.
Calculați volumul minim al unei soluții extrem de diluate:
V min = = = 0,001 ml.
Astfel, concentrația maximă a unei soluții extrem de diluate Cu min = 1 ∙ 10 -4 g/ml și volum minim V min = 0,001 ml.
Exemplul 2 Cationii Ag + argint pot fi deschiși prin reacția cu ionii de cromat CrO pentru a forma un precipitat roșu de cromat de argint Ag 2 CrO 4
2 Ag + + CrO → Ag 2CrO 4
la V min = 0,02 ml într-o soluție apoasă de azotat de argint AgNO 3 cu o concentrație molară Cu(AgNO 3) \u003d 0,0004 mol / l. Determinați limita de detecție g și limitați diluția V lim pentru cationul Ag +.
Decizie. Să aflăm mai întâi concentrația limită a cationilor de argint, ținând cont că în starea problemei este dată concentrația de nitrat de argint, exprimată în mol/l:
C min== ![]() = 4 ∙ 10 –5 g/ml,
= 4 ∙ 10 –5 g/ml,
Unde M(Ag +) este masa atomică a argintului.
g = C min V min ∙ 10 6 = 4 ∙ 10 –5 ∙ 0,02 ∙ 10 6 = 0,8 µg,
V lim = = = 2,5 ∙ 10 -4 ml/g.
Astfel, limita de detecție pentru cationul Ag + g = 0,8 μg, iar diluția limită V lim \u003d 2,5 ∙ 10 -4 ml / g.
Exemplul 3
Se separă cationii Al +3 și Mg +2 folosind un reactiv de grup.
Decizie. Al +3 aparține grupului IV de cationi, iar Mg +2 aparține grupului V. Hidroxidul de sodiu este un reactiv de grup pentru cationii din grupele IV și V. Ca semnal analitic, se observă precipitarea hidroxizilor corespunzători:
Al +3 + 3OH - ⇄ Al(OH)3↓;
Mg + 2 + 2OH - ⇄ Mg (OH) 2 ↓.
Cu toate acestea, atunci când se adaugă un exces de reactiv, Al (OH) 3 se dizolvă cu formarea unui compus complex, în timp ce Mg (OH) 2 nu:
Al(OH)3 + NaOH ⇄ Na;
Mg (OH)2 + NaOH1.
Astfel, în timpul separării, cationul Al +3 va fi în filtrat, iar cationul Mg +2 va fi în precipitat.
Exemplul 4
Ce volum dintr-o soluție de AgNO 3 cu o fracție de masă de 2% va fi necesar pentru a precipita clorura dintr-o probă de CaCl 2 ∙ 6 H 2 O cântărind 0,4382 g?
Decizie. Masa AgNO 3 se calculează pe baza legii echivalentelor.
Metodele instrumentale de analiză și-au primit numele datorită utilizării instrumentelor adecvate. Conform IUPAC (International Union of Pure and Applied Chemistry), un instrument este un dispozitiv care este folosit pentru a observa un anumit obiect, a măsura sau a raporta date despre starea unei substanțe. Dispozitivul înlocuiește acțiunile unei persoane, completează sau crește capacitățile acesteia.
În metodele instrumentale de analiză, diferite tipuri de instrumente sunt utilizate ca instrumente, concepute pentru a efectua proceduri de analiză de bază, pentru a măsura proprietățile fizice și fizico-chimice ale substanțelor și, de asemenea, pentru a înregistra rezultatele măsurătorilor. Datorită instrumentelor computerizate moderne, sensibilitatea analizei poate fi crescută semnificativ. Multe proprietăți fizico-chimice sunt specifice.
Toate metodele instrumentale (fizice și fizico-chimice) se bazează pe măsurarea mărimilor fizice corespunzătoare care caracterizează analitul din obiectul analizat.
Pentru fiecare metodă instrumentală se utilizează un semnal analitic adecvat. Tabelul 1 oferă exemple de semnale analitice și metodele corespunzătoare acestora, care aparțin celor două grupe majore - metode electrochimice de analiză și metode optice de analiză. Aceleași grupuri includ și alte metode care nu sunt prezentate în tabel. De exemplu, metodele optice includ metode luminiscente, de absorbție atomică și alte metode spectroscopice, nefelometrie, turbidimetrie și polarimetrie.
Pe lângă metodele electrochimice și optice, sunt cunoscute și alte grupuri de metode. Deci, de exemplu, metodele în care se măsoară radioactivitatea sunt denumite metode de fizică nucleară. Se mai folosesc metode spectrometrice de masă, metode termice etc.. Această clasificare este condiționată și nu este singura posibilă.
Dependența semnalului analitic de conținutul analitului X numita functie de calibrare. Se scrie ca o ecuație a formei I=f(C). În această ecuație, simbolul C indicați conținutul analitului X, care poate fi exprimat în diferite unități, de exemplu, unități de cantitate de substanță (mol), unități de masă (g, kg), unități de concentrație molară (mol / dm 3). Aceste unități sunt direct proporționale între ele. Mărimea semnalului analitic este în general indicată prin simbol eu, deși în unele metode sunt utilizate denumiri specifice (a se vedea tabelul 1). În fiecare metodă, funcțiile de calibrare sunt de același tip, dar forma exactă a funcției de calibrare pentru o anumită tehnică depinde de natura substanței care este determinată. Xși condițiile de măsurare a semnalului. Deci, în toate variantele de analiză refractometrică, semnalul analitic este indicele de refracție al fasciculului luminos (n), care depinde liniar de conținutul substanței. Xîn soluția de testare ( eu= n = a + k C). Aceasta înseamnă că în determinarea refractometrică a oricărei substanțe, curba de calibrare este dreaptă, dar nu trece prin originea coordonatelor (Fig. 1). Valorile numerice ale constantelor a și k depind de ce componentă este determinată și în ce condiții (solvent, temperatură, lungime de undă) se măsoară indicele de refracție.
Tabelul 1. Exemple de metode instrumentale de analiză
|
Metode electrochimice |
Semnal analitic |
Tipul funcției de calibrare |
|
|
Primar, I |
Secundar, I* |
||
|
Conductometrie |
Rezistență electrică, R |
conductivitate electrică, L |
L= a + k |
|
Potențiometrie |
E.D.S. dulap electrochimic, E |
potenţialul electrodului, E |
E= a + log b |
|
Voltametrie |
puterea curentului, i |
Limitarea curentului difuz, i d |
i d= k |
|
Coulometrie |
Cantitatea de energie electrică Q |
||
|
Electrogravimetrie |
masa produsului de electroliză, m |
||
|
Metode optice |
Semnal analitic |
Tipul funcției de calibrare |
|
|
Primar, I |
Secundar, I* |
||
|
Analiza spectrală a emisiilor atomice |
Fotocurent, i; înnegrire relativă, S |
i= a C b S= a + k lgC |
|
|
Spectrofotometrie |
Densitate optica, D |
D = l C |
|
|
Refractometrie |
indicele de refracție, n |
n = n - n o |
n = n 0 + kC |
În multe metode, dependența semnalului de concentrație este descrisă de funcții neliniare, de exemplu, în analiza luminiscentă, aceasta este o funcție exponențială ( eu\u003d kC n), în potențiometrie - o funcție logaritmică (E \u003d E 0 + k lgC), etc. În ciuda acestor diferențe, toate funcțiile de calibrare sunt similare prin aceea că, pe măsură ce valoarea lui C crește (conținutul analitului X) mărimea semnalului se modifică continuu, iar fiecare valoare a lui C corespunde unei singure valori eu.
Funcțiile de calibrare sunt stabilite experimental folosind probe standard de referință (standarde) care conțin diferite cantități exact cunoscute de substanță care trebuie determinată. X. Datele obţinute în urma măsurării semnalului pentru fiecare etalon permit ca funcţia de calibrare să fie prezentată sub forma unui tabel, grafic sau formulă algebrică. Dacă acum măsurăm semnalul analitic al probei de testat cu același instrument în aceleași condiții ca și semnalul standardului, atunci prin mărimea unui astfel de semnal va fi posibil să se determine conținutul Xîn proba de testare folosind funcția de calibrare.
Este ușor de calculat rezultatul analizei dacă semnalul eu direct proporțional cu conținutul de analit X. Dacă o astfel de dependență proporțională nu există, atunci semnalul analitic măsurat direct (primar). eu transformat într-un semnal analitic secundar eu*. Metoda de conversie este aleasă astfel încât semnalul analitic secundar eu* a fost direct proporțional cu cantitatea de analit X. Deci, de exemplu, rezistența electrică a soluției ( R) depinde într-un anumit fel de concentrația electrolitului dizolvat (C). Rezistența soluției analizate este ușor de măsurat, dar poate fi aplicată R ca semnal analitic este incomod deoarece pe măsură ce C crește, valoarea R scade și neliniar. Prin urmare, în analiza conductometrică, semnalul secundar este conductivitatea electrică a soluției L, care este legat de rezistență R prin următoarea formulă:
Conductibilitatea soluției L crește proporțional pe măsură ce crește concentrația de electrolit puternic dizolvat. În plus, din toate valorile L obţinut pentru soluţii de acelaşi tip cu concentraţii diferite X, puteți scădea aceeași valoare L 0 - conductivitatea electrică a unei soluții care nu conține X. Valoarea „corectată” a conductibilității electrice L* = L - L 0 nu depinde doar liniar de concentrație X, dar direct proporțional cu concentrația electrolitului din soluție, adică L* = kC.

Orez. 1.1. Grafice de calibrare tipice pentru unele metode instrumentale: 1 - refractometrie; 2 - analiza luminiscente; 3 - potențiometrie
Această tehnică se numește scădere de fundal. În metodele instrumentale, este folosit foarte des. Multe dispozitive sunt configurate înainte de a începe măsurarea, astfel încât să arate imediat semnalul corectat, care este direct proporțional cu C. Scara unui astfel de dispozitiv poate fi calibrată direct în unități de concentrație. Uneori, pentru a asigura liniaritatea graficelor de calibrare, acestea convertesc nu ordonata, ci abscisa. De exemplu, în analiza potențiometrică, conținutul nu este reprezentat de-a lungul axei orizontale X, și logaritmul său. Și în unele variante de analiză spectrală, se realizează o dublă transformare - atât semnalul, cât și concentrația sunt logaritmice, apoi se construiește o dependență grafică în linie dreaptă. lgI din lgC.
Medicina modernă are o gamă largă de capacități de diagnosticare. Pe lângă interogarea și examinarea pacientului, se folosesc metode de cercetare suplimentare. Gama de studii efectuate pentru ca pacienții să pună un diagnostic este în continuă extindere. Unele metode de cercetare sunt aplicate tuturor pacienților fără excepție, altele sunt efectuate conform indicațiilor individuale, în funcție de calea căutării diagnosticului.
Metode de cercetare instrumentală - cercetare folosind diverse dispozitive, instrumente și instrumente. Toate metodele instrumentale pot fi împărțite în două grupuri mari: neinvazive și invazive.
Metodele neinvazive sunt cele care nu sunt însoțite de o încălcare a integrității țesuturilor tegumentare și, în consecință, nu sunt asociate cu posibilitatea apariției complicațiilor. Și se împart în:
- radiografie (fluoroscopie, radiografie, tomografie cu raze X, angiografie, fluorografie);
Complicații- perforarea esofagului sau stomacului, reactii alergice sau laringotraheita traumatica, traumatisme ale peretilor organelor, infasurarea endoscopului in lumenul organului, pneumonie de aspiratie.
- RRS - - examinarea rectului și a colonului sigmoid - vă permite să examinați direct membrana mucoasă a rectului și a colonului sigmoid (rectoscopul este introdus la o adâncime de 25-30 cm), identificați prezența unui proces inflamator, hemoroizi interni, eroziune, hemoragie, neoplasme, efectuați biopsie țintită, obțineți frotiuri, efectuați răzuire din mucoasă.
Contraindicatii- colita ulcerativa in stadiul acut, hemoroizi strangulati, fisuri anale in stadiul acut.
Complicații – perforație intestinală, sângerare intestinală.
- – examinarea colonului – vă permite să examinați direct membrana mucoasă a colonului, să identificați prezența unui proces inflamator, hemoroizi interni, fisuri, eroziune, hemoragii, neoplasme, efectuați biopsie țintită, obțineți frotiuri, efectuați răzuire din mucoasă.
Contraindicatii- obstructie intestinala, insuficienta circulatorie decompensata, in stadiul acut, sangerari intestinale abundente, hipertensiune in stadiul III.
Complicații– perforarea intestinului în timpul exacerbarii colitei ulcerative, reacție dureroasă severă la tensiunea mezenterului, traumatisme și sângerări.
Intestoscopie cu capsule - consta in inghitirea de catre pacient a unei capsule speciale dotate cu o camera video in miniatura, un procesor, un sistem de transmitere a informatiilor. În timp ce trece prin intestine, capsula transmite constant, cu o viteză de 2 cadre pe secundă, o imagine video către un dispozitiv de înregistrare cu semiconductor printr-un sistem de senzori atașați la pielea abdomenului. Ulterior, dispozitivul de înregistrare este conectat la o stație de lucru computer unde imaginile sunt procesate și pot fi vizualizate pe un monitor și tipărite. Numărul total de imagini este mai mare de 50 000. Această metodă poate detecta leziuni ulcerative ale intestinului subțire, helmintiază, sângerări din intestinul subțire sau tulburări funcționale ale motilității intestinale. Capsulele moderne au capacitatea de a controla prin modificarea câmpului magnetic aplicat peretelui abdominal.
- Cistoscopie - examinarea cavității vezicii urinare - vă permite să examinați direct pereții vezicii urinare, să identificați prezența unui proces inflamator, a neoplasmelor și să efectuați o biopsie țintită.
Contraindicatii- tumori ale uretrei.
Complicații– leziuni ale organelor, sângerări, tulburări funcționale, infecție a cavităților și a organelor.
- - pentru diagnosticarea eroziunilor și ulcerelor mucoasei bronșice, extragerea corpilor străini, îndepărtarea polipilor bronșici, tratarea bronșiectaziei și abcesele pulmonare localizate central, administrarea de medicamente, efectuarea biopsiei țintite.
Contraindicatii - acut .
Complicații – stare colaptoidă, afectarea pereților bronhiilor, reacție alergică la anestezic.
Procedura cu ultrasunete
Ecografie - examinare cu ultrasunete - se bazează pe capacitatea undelor ultrasonice de a fi reflectate din țesuturi și organe cu densități diferite, cu înregistrarea pe un ecran de monitor video sau film fotografic. Vă permite să vă faceți o idee despre natura modificărilor patologice în orice organ parenchimatos.
1. Ecografia organelor abdominale (ficat, vezica biliară, pancreas, splină) - folosind metoda de cercetare cu ultrasunete, este posibilă determinarea dimensiunii și structurii organelor abdominale, diagnosticarea modificărilor patologice ale organelor abdominale (calculi, tumori, chisturi).
- (vezica urinara, uter, ovare, prostata) folosind metoda de cercetare cu ultrasunete, este posibil să se determine dimensiunea și structura organelor pelvine, diagnosticul modificărilor patologice în organele abdominale (calcul, tumori, chisturi).
- – este posibil să se determine dimensiunea și structura rinichilor, diagnosticul modificărilor patologice ale acestora (pietre, tumori, chisturi).
- Ecografia organelor de localizare superficială (glanda tiroidă, glande mamare, vasele limfatice regionale) - nu este necesară o pregătire specială.
Imagistică prin rezonanță magnetică
Imagistica prin rezonanță magnetică (RMN) este o metodă modernă de diagnostic neinvazivă sigură (fără radiații ionizante) care oferă vizualizarea țesuturilor biologice profund localizate, utilizată pe scară largă în practica medicală, în special în neurologie și neurochirurgie.
Metoda RMN de imagistică prin rezonanță magnetică face posibilă vizualizarea secțiunilor craniului și creierului, coloanei vertebrale și măduvei spinării pe ecranul de afișare și apoi pe filmul cu raze X.
Informațiile permit diferențierea substanțelor cenușii și albe ale creierului, a judeca starea sistemului său ventricular, a spațiului subarahnoidian, pentru a identifica multe forme de patologie, în special procese volumetrice în creier, zone de demielinizare, focare de inflamație și edem, hidrocefalie. , leziuni traumatice, hematoame, focare de manifestare a tulburărilor circulației cerebrale după tipul ischemic și hemoragic, apropo, focarele ischemice la nivelul creierului pot fi detectate încă de la 2-4 ore după un accident vascular cerebral.
Un avantaj important al imagistică prin rezonanță magnetică RMN față de CT este capacitatea de a obține o imagine în orice proiecție: axială, frontală, sagitală. Aceasta permite vizualizarea spațiului subtentorial, canalului rahidian, depistarea neuromului acustic în cavitatea canalului auditiv intern, tumorii hipofizare, hematom subdural în perioada subacută, chiar și în cazurile în care nu este vizualizat pe CT.
Tehnica imagistică prin rezonanță magnetică (examen RMN) constă în așezarea pacientului în poziție orizontală într-un tunel îngust al tomografului, timpul depinde de tipul de examinare. Pacientul trebuie să mențină imobilitatea completă a zonei anatomice studiate.
Cercetarea radioizotopilor
Cercetarea radioizotopilor - toate metodele se bazează pe același principiu: izotopii diferitelor elemente chimice iau parte la procesele fiziologice care au loc în organism, la fel ca și substanțele stabile (radioactive) similare. Introducerea radionuclizilor în organism face posibilă determinarea cantității acestora în organe și medii biologice cu mare fiabilitate (ținând cont de activitatea introdusă pacientului).
- Scanare- folosit pentru a studia ficatul, pancreasul, rinichii, glanda tiroidă.
Au (198) sau J (131) este injectat în pacient pentru scanare. Scanarea se efectuează după 40-50 de minute folosind un dispozitiv special - un scanner, a cărui parte principală este un detector de radiații nucleare, care se deplasează automat peste zona organului studiat în două direcții perpendiculare. Folosind un dispozitiv special de scris, rezultatele măsurării activității sunt înregistrate pe hârtie sau film sub formă de linii linie cu linie, iar frecvența și intensitatea eclozării depind de activitatea acumulată în organ.
Astfel, în urma scanării, se obține o imagine scanogramă-plană a organului studiat, ceea ce face posibilă aprecierea gradului, caracteristicilor de acumulare și distribuție a izotopului în țesuturile organului după natura eclozionarii. . În prezent, se utilizează scanarea color, în care zonele cu grade diferite de umplere cu izotopi sunt reproduse în culori diferite pe scanogramă. La evaluarea unei scanări, se ia în considerare dimensiunea și forma imaginii, intensitatea umbririi în diferite zone, prezența „defectelor de umplere” - absența umbririi în anumite zone.
- Studiu funcțional al organelor și sistemelor– se bazează pe același principiu: determinarea vitezei și gradului de intrare, acumulare sau distribuție și excreție a izotopilor și compușilor marcați în organele și sistemele organismului.
Un element radioactiv este de obicei administrat pacientului pe cale intravenoasă, iar apoi, folosind senzori ai dispozitivelor radiometrice, radiațiile emanate din organe sau țesuturi sunt înregistrate și înregistrate ca imagine grafică sau în valori digitale.
Această metodă este în prezent cea mai utilizată pentru diagnosticul patologiei tiroidiene, de exemplu, un test în două faze cu iod radioactiv, ale cărui rezultate reflectă acumularea de J 131 în glanda tiroidă sau concentrația de iod în plasmă.
- studii radioimunohormonale -în ultimii ani, acest tip de diagnosticare cu radioizotopi a devenit din ce în ce mai important, deoarece. are o sensibilitate și o specificitate foarte ridicate în comparație cu diagnosticul imun și biochimic convențional și vă permite să determinați conținutul multor hormoni și enzime din serul sanguin.
Studiul se desfășoară „in vitro”, materialul de testat este serul sanguin al pacientului, la care se adaugă hormonul etichetat corespunzător cu o anumită activitate, precum și unele specifice. Apoi, în comparație cu standardele speciale, se determină cu un grad ridicat de acuratețe în concentrația hormonului enzimei afide studiate, de exemplu, endogen, pepsină, angiotensină, gastrină, secretină.
Laparoscopie
Examinarea endoscopică a cavităților care nu au legătură cu mediul extern - laparoscopie- este o metodă de cercetare constând în introducerea unui endoscop special în cavitatea abdominală - un laparoscop printr-o mică incizie pentru a vizualiza direct procesul patologic.
Laparoscopul este un tub metalic cu diametrul de 5 mm cu un sistem complex de lentile si ghid de lumina.
Puteți privi în lentila unui laparoscop cu ochiul - acest lucru se face de multe decenii. Cu toate acestea, în ultimii treizeci de ani, odată cu apariția camerelor video endoscopice miniaturale (acum cântăresc 50 g) atașate lentilei laparoscopului, a devenit posibil ca toată lumea din sala de operație să observe întregul curs al operației pe ecranul monitorului.
FEDERAȚIA RUSĂ
"APROBA":
Și despre. prorector-şef
Departamentul pentru lucrări științifice
_______________________
2011
forme de învăţământ cu normă întreagă şi cu frecvenţă redusă
„______” ___________2011
Revizuit la o întâlnire a Departamentului de Chimie Organică și Ecologică
Îndeplinește cerințele de conținut, structură și design.
Volumul 12 pagini.
Cap departament ______________________________/ /
„______” ___________ 2011
Considerat la ședința UMK IMENIT
„______” ____________ 2011, protocol Nr.
Corespunde FGT cu structura principalului program educațional profesional de învățământ profesional postuniversitar (studii postuniversitare)
"DE ACORD":
Președintele CMD ________________________/ /
„______” _____________2011
"DE ACORD":
Început departament postuniversitar
și studii de doctorat ______________________
„______” _____________2011
FEDERAȚIA RUSĂ
MINISTERUL EDUCAȚIEI ȘI ȘTIINȚEI
Instituție de învățământ de stat
studii profesionale superioare
UNIVERSITATEA DE STAT TYUMEN
Institutul de Matematică, Științe ale Naturii și Tehnologii Informaționale
Catedra de Chimie Organică şi Ecologică
NOI METODE INSTRUMENTALE ÎN CHIMIA ANALITĂ
Complex de instruire și metodologie. Program de lucru
pentru absolvenții specialității 02.00.02 Chimie analitică
forme de învăţământ cu normă întreagă şi cu frecvenţă redusă
Universitatea de Stat din Tyumen
2011
Noi metode instrumentale în chimia analitică. Complex de instruire și metodologie. Program de lucru pentru studenții postuniversitari ai specialității 02.00.02 Chimie analitică. Tyumen, 2011, 12 pagini.
Programul de lucru este întocmit în conformitate cu FGT la structura principalului program educațional profesional de învățământ profesional postuniversitar (studii postuniversitare).
REDATOR RESPONSABIL: Șef Catedră de Chimie Organică și Ecologică, Doctor în Științe, Profesor
© Universitatea de Stat Tyumen, 2011.
Notă explicativă Scopurile și obiectivele disciplinei
Scopul disciplinei: dezvoltarea metodelor moderne de cercetare instrumentală utilizate în chimie și necesare desfășurării efective a principalului program de învățământ profesional de învățământ profesional postuniversitar (studiu postuniversitar) în specialitatea 02.00.02 Chimie analitică și pregătirea unui doctorat. .D. teză.
Obiectivele disciplinei: stăpânirea următoarelor întrebări de către studenții absolvenți:
Fundamentele teoretice ale metodelor instrumentale (modele structurale ale moleculelor și solidelor, interacțiunea materiei cu radiația); aplicarea practică a metodelor instrumentale în chimia analitică modernă.
Locul disciplinei în structura OPPO
Disciplina „Noi metode instrumentale în chimie analitică” aparține ciclului disciplinelor speciale din ramura științei și specialității științifice.
Pentru dezvoltarea cu succes a acestei discipline, studenții trebuie să posede concepte teoretice în domeniul structurii substanțelor chimice, bazele metodelor spectrale, de difracție, cromatografice și electrochimice.
Stăpânirea disciplinei „Noi metode instrumentale în chimie analitică” este necesară pentru a finaliza o cercetare de disertație.
Cerințe pentru rezultatele stăpânirii disciplinei
Procesul de studiu al disciplinei are ca scop formarea următoarelor competențe:
Competențe generale
- utilizarea legilor de bază ale științelor naturii în activități profesionale, utilizarea metodelor de analiză și modelare matematică, cercetare teoretică și experimentală; posesia metodelor de bază, modalităților și mijloacelor de obținere, stocare, prelucrare a informațiilor, deținerea deprinderilor de a lucra cu calculatorul ca mijloc de gestionare a informațiilor.
Competențe profesionale
- înțelegerea esenței și semnificației sociale a profesiei, a principalelor perspective și probleme care determină un anumit domeniu de activitate - chimia analitică; cunoașterea fundamentelor teoretice ale metodelor de cercetare instrumentală; posesia deprinderilor de experiment chimic analitic si prelucrarea datelor experimentale.
Ca urmare a stăpânirii disciplinei, studentul trebuie:
Cunoaște: bazele teoretice ale metodelor de cercetare spectrală, de difracție, cromatografică și electrochimică; modele structurale ale moleculelor.
Să fie capabil: să colecteze și să analizeze informații științifice, tehnologice și statistice; planifica cercetări științifice experimentale în domeniul chimiei analitice, procesează date experimentale, elaborează articole și rezumate pentru publicare.
Proprietar: metode moderne de cercetare experimentală în domeniul chimiei analitice, metode de statistică matematică și modelare matematică, tehnologia informației, inclusiv metode de lucru cu un calculator și baze de date electronice.
Intensitatea muncii a disciplinei
Disciplina se predă în semestrul 5. Forma de certificare intermediară este un test. Intensitatea totală de muncă a disciplinei este de 3 credite, 108 ore.
Plan tematic
tabelul 1
Plan tematic
Total ore | tipuri de muncă educațională și muncă independentă, pe oră. | Forme de control |
|||||
seminarii | clase de laborator | muncă independentă |
|||||
Fundamentele teoretice ale metodelor instrumentale |
|
||||||
Metode de analiză spectrală și de difracție |
Protecția de laborator. lucrări |
||||||
Separare și metode electrochimice de analiză |
Protecția de laborator. lucrări |
||||||
masa 2
Planificarea muncii independente a studenților absolvenți
Secțiuni ale disciplinei și legături interdisciplinare cu disciplinele furnizate (ulterioare).
Conținutul disciplinei
Tema 1. Fundamentele teoretice ale metodelor instrumentale
Fundamentele doctrinei structurii moleculelor. Stări staționare: electronică, vibrațională, rotațională, spin nuclear. Tranziții cuantice între stări staționare, probabilități și reguli de selecție. Tipuri de spectre moleculare: electronice, vibrațional-rotaționale, RMN, fotoelectron. Metode de înregistrare și prelucrare a spectrelor. Analiza spectrală calitativă, cantitativă și structurală.
Difracția undelor electromagnetice și a fasciculelor de electroni pe obiecte punctuale și cristale.
Caracteristicile de adsorbție ale moleculelor organice. Cromatograma și caracteristicile acesteia, metode de înregistrare și prelucrare. Timpul de retenție și indici de retenție, relația lor cu structura moleculelor de sorbat și sorbant. Metode de bază de analiză cromatografică. Analize cromatografice calitative, cantitative și structurale.
Structura soluțiilor electrolitice. Procesele electrochimice și mecanismele acestora.
Tema 2. Metode spectrale și de difracție
Identificarea compușilor chimici prin metode spectrale: utilizarea spectroscopiei UV, IR și RMN și spectrometriei de masă. Spectroscopie cu raze X: metoda XPS, metoda structurii fine extinse cu absorbție de raze X (PTSRP, EXAFS). Legătura spectrului cu natura substanței studiate. Oportunități și limitări.
Determinarea cantitativă a elementelor și compușilor chimici prin metode spectrale. Sensibilitatea, selectivitatea și acuratețea analizei. Specificul tehnicii de analiză în monitorizarea mediului. Analiza spectrală structurală. Determinarea fragmentelor structurale ale unei molecule (radicali, grupe funcționale, tip de schelet, legături multiple etc.).
Tehnici moderne de difracție: difractometrie cu raze X, difracție electronică de joasă energie (LEED), împrăștiere cu fascicul de ioni de energie scăzută (LEIS), împrăștiere cu raze X cu unghi mic (XANES), microscopie electronică de transmisie/scanare.
Microscopie cu scanare tunel.
Utilizarea metodelor spectrale pentru studiul structurii moleculelor și solidelor, catalizatorilor, mecanismelor reacțiilor chimice.
Identificarea compușilor organici prin metode cromatografice: utilizarea metodelor GLC și HPLC. Metode de îmbunătățire a calității cromatogramei, selecția detectorilor, coloanelor, fazelor staționare, eluanților, condițiilor de temperatură. electroforeza capilara. Posibilitățile și limitările metodelor de separare.
Determinarea cantitativă a ionilor și compușilor organici prin metode de separare. Sensibilitatea, selectivitatea și acuratețea analizei. Specificul tehnicii de analiză în monitorizarea mediului.
Analiza cromatografică structurală. Indici de retenție, relația lor cu structura moleculelor. Determinarea fragmentelor structurale ale unei molecule (radicali, grupe funcționale, tip de schelet, legături multiple etc.).
Noutăți în metodele electrochimice de analiză: potențiometrie, voltametrie, coulometrie, electrogravimetrie.
Planuri de seminar.
Seminariile nu sunt incluse în curriculum
Subiecte de lucru de laborator. (atelier de laborator)
Tema 2. Metode de analiză spectrală și de difracție
Lucrare de laborator nr 1 (6 ore). Cercetare și dezvoltare: Determinarea separată a conținutului de compuși saturați și aromatici într-o probă de ulei. Obiectul cercetării: probă de ulei sau produs petrolier (benzină, motorină, ulei). Metode utilizate: prelevarea spectrelor UV și IR, prelucrarea și interpretarea acestora.
Lucrare de laborator nr.2 (6 ore). R&D: Determinarea structurii unei molecule. Obiectul de studiu: o probă de hidrocarbură aromatică petrolieră. Metode utilizate: prelevarea spectrelor UV și IR, prelucrarea și interpretarea acestora, determinarea numărului și tipului de substituenți din nucleul aromatic al moleculei.
Tema 3. Separarea și metodele electrochimice de analiză
Lucrare de laborator nr. 3 (6 ore). R&D: Analiza calitativă a unui eșantion de produs petrolier (benzină, motorină). Obiectul de studiu: benzină comercială sau motorină. Metode utilizate: obţinerea unei cromatograme cu ajutorul unui gazcromatograf. Identificarea componentelor amestecului folosind o bază de date. Calculul conținutului relativ de componente din amestec.
Lucrare de laborator nr.4 (6 ore). R&D: Studiul cineticii reacțiilor de alchilare. Obiectul de studiu: butandiol-1,4, clorură de alil, oxid de piridină. Metode utilizate: prelevarea de probe a mediului de reacție, analiza chimică a produselor de reacție (eteri mono- și dialilici ai butandiolului), determinarea randamentului în produse, calculul activității și selectivității catalizatorului.
Subiecte aproximative ale lucrărilor trimestriale.
Lucrările de curs nu sunt incluse în curriculum.
Suport educațional și metodologic pentru munca independentă a studenților absolvenți.
Instrumente de evaluare pentru monitorizarea curentă a progresului, certificare intermediară pe baza rezultatelor stăpânirii disciplinei (modul).
Principiul principal al organizării muncii independente este o abordare integrată care vizează stimularea următoarelor tipuri de activități pentru ca studenții absolvenți să dobândească competențe:
reproductiv - îndeplinirea sarcinilor după model în vederea consolidării cunoștințelor teoretice, dezvoltării deprinderilor și abilităților (citire, vizionare, luare de notițe, ascultare, memorare; răspuns la întrebări pentru autotestare; repetare material educațional, rezolvare de probleme tipice);
reconstructiv - efectuarea de sarcini cu transformarea obligatorie a informaţiei (pregătire pentru lecţiile de la clasă, discuţii tematice; pregătirea mesajelor, rapoartelor şi discursurilor la seminarii; selecţia literaturii; efectuarea de teste; rezolvarea problemelor practice);
creativ - selecția și analiza critică a informațiilor (scrierea de eseuri, rapoarte; participarea la lucrări de cercetare, îndeplinirea sarcinilor creative speciale; pregătirea proiectelor și prezentărilor de diapozitive).
Lista de verificare pentru credit
Stări staționare ale atomilor și moleculelor: electronică, vibrațională, rotațională, spin nuclear. Tranziții cuantice între stări staționare, probabilități și reguli de selecție. Tipuri de spectre atomice și moleculare: electronice, vibrațional-rotaționale, RMN, fotoelectron. Metode de înregistrare și prelucrare a spectrelor. Analiza spectrală calitativă, cantitativă și structurală. Difracția undelor electromagnetice și a fasciculelor de electroni pe obiecte punctuale și cristale. Caracteristicile de adsorbție ale moleculelor organice. Cromatograma și caracteristicile acesteia, metode de înregistrare și prelucrare. Timpul de retenție și indici de retenție, relația lor cu structura moleculelor de sorbat și sorbant. Metode de bază de analiză cromatografică. Analize cromatografice calitative, cantitative și structurale. Structura soluțiilor electrolitice. Procesele electrochimice și mecanismele acestora. Identificarea compușilor chimici prin metode spectrale: utilizarea spectroscopiei UV, IR și RMN și spectrometriei de masă. Spectroscopie cu raze X: metoda XPS, metoda structurii fine extinse cu absorbție de raze X (PTSRP, EXAFS). Legătura spectrului cu natura substanței studiate. Oportunități și limitări. Determinarea cantitativă a elementelor și compușilor chimici prin metode spectrale. Sensibilitatea, selectivitatea și acuratețea analizei. Analiza spectrală structurală. Determinarea fragmentelor structurale ale unei molecule (radicali, grupe funcționale, tip de schelet, legături multiple etc.). Tehnici moderne de difracție: difractometrie cu raze X, difracție electronică de joasă energie (LEED), împrăștiere cu fascicul de ioni de energie scăzută (LEIS), împrăștiere cu raze X cu unghi mic (XANES), microscopie electronică de transmisie/scanare. Microscopie cu scanare tunel. Utilizarea metodelor spectrale pentru studiul structurii moleculelor și solidelor, catalizatorilor, mecanismelor reacțiilor chimice. Identificarea compușilor organici prin metode cromatografice: utilizarea metodelor GLC și HPLC. Metode de îmbunătățire a calității cromatogramei, selecția detectorilor, coloanelor, fazelor staționare, eluanților, condițiilor de temperatură. electroforeza capilara. Posibilitățile și limitările metodelor de separare. Determinarea cantitativă a ionilor și compușilor organici prin metode de separare. Sensibilitatea, selectivitatea și acuratețea analizei. Analiza cromatografică structurală. Indici de retenție, relația lor cu structura moleculelor. Determinarea fragmentelor structurale ale unei molecule (radicali, grupe funcționale, tip de schelet, legături multiple etc.) d.). Noutăți în metodele electrochimice de analiză: potențiometrie, voltametrie, coulometrie, electrogravimetrie.
Subiecte aproximative pentru teste și sondaje
1. Tranziții electronice în molecule organice
2. Tranziții vibrațional-rotaționale în molecule organice
3. Tranziții nucleare de spin în molecule organice
4. Proprietățile de adsorbție ale moleculelor organice
5. Metode de prelucrare matematică a spectrelor moleculare
6. Metode de prelucrare matematică a cromatogramelor
7. Metode de cercetare a difracției
8. Metode de studiere a mecanismelor de reacție
9. Instrumente spectrale și cromatografice moderne
Exemple de teste și întrebări pentru autocontrol
Metode spectrale:
1. Ce caracteristici stau la baza împărțirii scalei undelor electromagnetice în intervale și care sunt caracteristicile domeniului optic?
2. Cum este numărul de undă legat de lungimea de undă?
1) ν = λ; 2) Δν = –Δλ/λ2; 3) ν = с/λ; 4) ν = 1/λ..
3. Cea mai mare energie necesară:
1) a excita electronii;
2) a excita vibrațiile atomilor dintr-o moleculă;
3) să excite rotații ale moleculei;
4) pentru reorientarea spinurilor nucleare.
4. Care este raportul dintre energiile stărilor Her electronice, Eυ vibraționale și Er rotaționale ale unei molecule?
1) Еe > Еυ > Еr; 2) Eυ > Er > Ee; 3) Er > Ee > Eυ; 4) Er > Eυ > Ee.
5. Când se analizează spectre de ce tip ar trebui să se țină cont de principiul Franck-Condon?
1) IR. 2) rotativ. 3) KR-. 4) electronice.
6. În ce regiuni ale spectrului se observă spectre electronic-vibrațional-rotațional, vibrațional-rotațional și rotațional?
7. În ce regiuni ale spectrului se manifestă tranzițiile între stările electronice, vibraționale și rotaționale ale moleculelor?
1) Vibrațional - în regiunea IR, rotațional - în regiunea UV, electronic - în regiunea microundelor.
2) Vibrațional - în cuptorul cu microunde, electronic - în regiunea UV, rotațional - în regiunea IR.
3) Vibrațional - în regiunea IR, rotațional - în regiunea microunde, electronic - în regiunea UV.
4) Vibrațional - în regiunea UV, electronic - în regiunea IR, rotațional - în regiunea microundelor.
8. Metodele de analiză bazate pe măsurarea luminii absorbite de o probă se numesc:
1) radiometrie; 2) absorbiometrie; 3) fluorimetrie;
4) turbidimetrie.
Metode cromatografice:
Care este scopul condiționării coloanelor cromatografice? De ce se efectuează această procedură fără a conecta coloana la detector? Ce raport dintre diametrul coloanei și dimensiunea granulelor de absorbant este optim pentru coloanele pliate? Dacă volumul coloanei este de 45 ml, câtă cantitate de ambalaj trebuie folosită pentru a umple coloana? Ce mecanism stă la baza tratamentului purtătorilor minerali cu dimetildiclorosilan, trimetilclorosilan și hexametildisilazan? În ce caz se formează produse gazoase periculoase? Dacă pe cromatogramă timpul de retenție al dodecanului și tetradecanului este de 12,4, respectiv 14,7 min, ce număr de plăci teoretice pentru această coloană va fi mai mare: calculat 1) atât pentru dodecan, cât și pentru tetradecan, 2) pentru dodecan, 3) pentru tetradecan? Dacă HETP pentru o coloană metalică (2 m × 3 mm) umplută cu sorbent polimeric Porapak N (80-100 mesh) la analiza unei probe de propan în heliu (C = 0,3% vol.) este 8,3; 6,6; 2.1; 2,7; 4,5 și 5,4 mm la o viteză spațială a heliului de 10; treisprezece; cincisprezece; 20; 30 și 40 ml/min, care ar fi viteza optimă a gazului purtător pentru separarea eficientă a propanului, izobutanului și n-butanului? Este posibil să se determine timpul mort în aer cu un detector TDS folosind o coloană cromatografică umplută cu sită moleculară CaX (coloană 2 m × 3 mm, fracțiunea sorbant 0,25-0,30 mm, viteza heliului - 15 ml / min, temperatura termostatului: 45 ° CU)? Dacă proba analizată (volum 1 µl) a fost injectată în evaporatorul cromatograf cu microseringi de 1 și 10 µl de 5 ori, caz în care abaterea standard a înălțimilor și zonelor vârfurilor cromatografice va fi mai mare? Care este factorul determinant pentru un timp de retenție constant al compusului analizat (viteza gazului purtător, precizia menținerii temperaturii termostatului coloanelor, aceeași procedură pentru introducerea probei cu o microseringă în evaporator)? Dacă graficul timpilor de retenție corectați ai hidrocarburilor normale dodecan (C12) - tetracosan (C24) are o pauză după eluarea C21, ce se poate spune despre regimul de temperatură al termostatului coloanei (coloana capilară HP-5, 30 m × 0,32 mm, viteza liniară a heliului - 30 cm/s)? Ce compuși pot fi utilizați ca standarde în determinarea indicilor de retenție în studiile biochimice ale probelor prin cromatografie în gaz? Ce combinație de detectoare care funcționează secvențial va determina concentrația de eter metil terțiar butilic (MTBEA) în benzina A-92? Ce detector este de preferat la determinarea compușilor de sulf din petrol și produse petroliere? Care este fereastra de căutare pentru indicii Kovacs ai hidrocarburilor într-un amestec complex? Ce faze staționare pot fi utilizate pentru a determina compoziția individuală a benzinei prin cromatografie capilară în gaze?
Criterii de evaluare a CDS:
calitatea însușirii materialului educațional (capacitatea elevului de a utiliza cunoștințele teoretice în îndeplinirea sarcinilor practice); elaborarea tuturor aspectelor sarcinii, proiectarea materialului în conformitate cu cerințele, respectarea termenelor stabilite pentru depunerea lucrărilor spre verificare; gradul de independență, activitatea creativă, inițiativa absolvenților, prezența elementelor de noutate în procesul de finalizare a sarcinilor.Rezultatele IWS sunt însumate în săptămânile de control, al căror calendar este determinat de programul procesului educațional.
Tehnologii educaționale.
Tipuri de muncă educațională | Tehnologii educaționale |
sala de clasa | a) Prelegeri (demonstrații multimedia și video, testare scrisă pe materialul acoperit (4 teste cu câte 10 întrebări fiecare). b) Desfășurarea orelor de laborator (elaborarea unui plan de experimentare, discuții în grup și analiza problemelor, demonstrații multimedia, audierea și discutarea rapoartelor orale, mesaje, discursuri, întâlniri cu profesori din alte discipline). c) Tehnologii interactive (discuții de grup, analiza unor situații specifice). |
Muncă independentă | a) Studiul literaturii educaționale și metodologice, inclusiv căutarea informațiilor în rețele electronice și baze de date, pregătirea prezentărilor. b) Pregătirea pentru teste c) Pregătirea lucrărilor de laborator pentru protecție (folosind prezentări multimedia) |
11.1. Literatura principala:
1., Chimie analitică. M.: IC „Academie”. 2011.
2. Reviste: „Chimie analitică”, „Uspekhi khimii”, „Russian Chemical Journal” pentru 2001-2011.
11.2. Literatură suplimentară:
1. Planificarea și prelucrarea matematică a rezultatelor unui experiment chimic. Omsk: Editura OmGU. 2005.
2. Curs practic de analiză a absorbției atomice. Curs de curs. Ekaterinburg. 2003.
3. Metode pentru studiul catalizatorilor / ed. J. Thomas și R. Lembert. M., Mir, 1983.
11.3. Software și resurse de internet:
www. e-bibliotecă. ro
chimic. /rus/teaching/analyt/
www. ftchimie. dsmu. /ana_him/lek_13.html
Mijloace tehnice și suport logistic al disciplinei (modul).
Prelegerile sunt prevăzute cu prezentări multimedia și videoclipuri. Pentru a susține prelegeri este necesar să existe săli de clasă dotate cu echipamente multimedia (calculator, proiector etc.).
Pentru munca de laborator, sunt dotate laboratoare pentru spectroscopie (117, clădirea 5) și cromatografie (116, clădirea 5).
Pentru munca independentă a studenților absolvenți, este necesar accesul la o clasă de calculatoare cu acces la internet.