Инструментальные методы анализа в аналитической. Физико-химические или инструментальные методы анализа. Количество принятых mз и отданных nз электронов должно быть равно, поэтому уравнение окислительно-восстановительного процесса можно записать в виде
Аналитическая химия II. Инструментальные методы анализа Майстренко В. Н. Башкирский государственный университет Кафедра аналитической химии V_maystrenko@mail. ru Тел: 229 -97 -12
 Аналитическая химия – наука об определении химического состава веществ и отчасти их химического строения Химические методы анализа Физико-химические методы анализа Физические методы анализа Инструментальные методы анализа
Аналитическая химия – наука об определении химического состава веществ и отчасти их химического строения Химические методы анализа Физико-химические методы анализа Физические методы анализа Инструментальные методы анализа
 Инструментальные методы анализа - методы аналитической химии, для выполнения которых требуется электрохимическая, оптическая, радио-химическая и иная аппаратура. К инструментальным методам анализа относятся: электрохимические методы - потенциометрия (ионометрия), кулонометрия, вольтамперометрия, кондуктометрия и др. ; методы, основанные на испускании или погло-щении электромагнитного излучения – эмиссионная, абсорбционная, флуоресцентная атомная и молеку-лярная спектроскопия, фотометрические методы, рентгеноспектральный анализ и др. ; масс-спектральный анализ; ЯМР, ЭПР, методы, основанные на измерении радиоактивности и др.
Инструментальные методы анализа - методы аналитической химии, для выполнения которых требуется электрохимическая, оптическая, радио-химическая и иная аппаратура. К инструментальным методам анализа относятся: электрохимические методы - потенциометрия (ионометрия), кулонометрия, вольтамперометрия, кондуктометрия и др. ; методы, основанные на испускании или погло-щении электромагнитного излучения – эмиссионная, абсорбционная, флуоресцентная атомная и молеку-лярная спектроскопия, фотометрические методы, рентгеноспектральный анализ и др. ; масс-спектральный анализ; ЯМР, ЭПР, методы, основанные на измерении радиоактивности и др.
 Дефиниция y = f(x) х y Аналитический сигнал Сигнал, содержащий количественную информацию о величине, функционально связанной с содержанием определяемого компонента, и регистрируемый в ходе анализа вещества или материала "Контроль объекта аналитический. Термины и определения. " ГОСТ Р 52361– 2005.
Дефиниция y = f(x) х y Аналитический сигнал Сигнал, содержащий количественную информацию о величине, функционально связанной с содержанием определяемого компонента, и регистрируемый в ходе анализа вещества или материала "Контроль объекта аналитический. Термины и определения. " ГОСТ Р 52361– 2005.

 Дефиниции Измерение величины y = f(x) х1 хn х2 Определение вещества Анализ объекта y 1 y 2 y 3 yn
Дефиниции Измерение величины y = f(x) х1 хn х2 Определение вещества Анализ объекта y 1 y 2 y 3 yn
 Дефиниция Сигнал, y Градуировочная функция ∆y α ∆х b tgα = а = ∆y/∆х Концентрация, х y = f(x) y = b + аx
Дефиниция Сигнал, y Градуировочная функция ∆y α ∆х b tgα = а = ∆y/∆х Концентрация, х y = f(x) y = b + аx
 Дефиниция y = f(x) х Предел обнаружения y Сlim = y 0 + 3σ Концентрация, x
Дефиниция y = f(x) х Предел обнаружения y Сlim = y 0 + 3σ Концентрация, x
 Дефиниция y = f(x) lgх Предел обнаружения y Сlim = y 0 + 3σ Концентрация, lgx
Дефиниция y = f(x) lgх Предел обнаружения y Сlim = y 0 + 3σ Концентрация, lgx
 Дефиниция y = f(x) х Интервал определяемых концентраций y a = tgα y = ax + b Концентрация, x
Дефиниция y = f(x) х Интервал определяемых концентраций y a = tgα y = ax + b Концентрация, x

 Метод и методика анализа Метод анализа – достаточно универсальный и теоретически обоснованный способ определения состава безотносительно к определяемому компоненту и (обычно) к анализируемому объекту. Методика анализа – подробное описание анализа данного объекта с использованием выбранного метода. "Контроль объекта аналитический. Термины и определения. " ГОСТ Р 52361– 2005.
Метод и методика анализа Метод анализа – достаточно универсальный и теоретически обоснованный способ определения состава безотносительно к определяемому компоненту и (обычно) к анализируемому объекту. Методика анализа – подробное описание анализа данного объекта с использованием выбранного метода. "Контроль объекта аналитический. Термины и определения. " ГОСТ Р 52361– 2005.
 Методы аналитической химии Методы отбора проб (пробоотбора) Методы разложения проб Методы разделения компонентов Методы концентрирования Методы обнаружения (идентификации) Методы определения
Методы аналитической химии Методы отбора проб (пробоотбора) Методы разложения проб Методы разделения компонентов Методы концентрирования Методы обнаружения (идентификации) Методы определения
 Проба Проба – или образец – предмет исследования аналитика, объект, взятый для анализа. По ГОСТ: проба - часть вещества (материала), являющегося объектом аналитического контроля, отобранная для анализа и/или исследования его структуры, и/или определе-ния свойств, отражающая его химический состав и/или структуру, и/или свойства. Представительная проба вещества или материала - объекта аналитического контроля – проба, которая по химическому составу и/или свойствам, и/или структуре идентична объекту аналитического контроля, от которого она отобрана.
Проба Проба – или образец – предмет исследования аналитика, объект, взятый для анализа. По ГОСТ: проба - часть вещества (материала), являющегося объектом аналитического контроля, отобранная для анализа и/или исследования его структуры, и/или определе-ния свойств, отражающая его химический состав и/или структуру, и/или свойства. Представительная проба вещества или материала - объекта аналитического контроля – проба, которая по химическому составу и/или свойствам, и/или структуре идентична объекту аналитического контроля, от которого она отобрана.
 Классификация проб В зависимости от способа получения: разовая, точечная (единичная, частная), мгновенная, суточная и т. п. В зависимости от стадии первичной обработки: исходная, промежуточная, объединенная, средняя, сокращенная, лабораторная, аналитическая и др. В зависимости от назначения: контрольная, рабочая, резервная, арбитражная и др.
Классификация проб В зависимости от способа получения: разовая, точечная (единичная, частная), мгновенная, суточная и т. п. В зависимости от стадии первичной обработки: исходная, промежуточная, объединенная, средняя, сокращенная, лабораторная, аналитическая и др. В зависимости от назначения: контрольная, рабочая, резервная, арбитражная и др.
 Абсолютные и относительные методы анализа Абсолютные методы – не требуют градуировки и стандартных образцов (гравиметрия, кулонометрия и т. д.). Относительные методы – параметры градуировочной функции определяют экспериментально (потенциометрия, вольтамперометрия и т. д.) с использованием стандартных образцов.
Абсолютные и относительные методы анализа Абсолютные методы – не требуют градуировки и стандартных образцов (гравиметрия, кулонометрия и т. д.). Относительные методы – параметры градуировочной функции определяют экспериментально (потенциометрия, вольтамперометрия и т. д.) с использованием стандартных образцов.
 Одномерные и многомерные методы Одномерные методы основаны на измерении интенсивности сигнала в единственной измеритель-ной позиции. Сигнал, y Многомерные методы – используются несколько измерительных позиций. Положение максимума пика или полосы – качественная характеристика. Высота или площадь пика – количественная характеристика. Вторая координата, z
Одномерные и многомерные методы Одномерные методы основаны на измерении интенсивности сигнала в единственной измеритель-ной позиции. Сигнал, y Многомерные методы – используются несколько измерительных позиций. Положение максимума пика или полосы – качественная характеристика. Высота или площадь пика – количественная характеристика. Вторая координата, z

 Классификация методов анализа Общая классификация качественный / количественный элементный / изотопный / молекулярный / структурно-групповой валовый / распределительный (локальный) / вещественный / фазовый контактный / дистанционный деструктивный / недеструктив-ный макро- > 0. 1 г полумикро- 0. 1 - 0. 01 г микро- 0. 01 – 0. 001 г ультрамикро- 10 -6 г субмикро- 10 -9 г макро- / полумикро- / ультрамикро- / субмикро-
Классификация методов анализа Общая классификация качественный / количественный элементный / изотопный / молекулярный / структурно-групповой валовый / распределительный (локальный) / вещественный / фазовый контактный / дистанционный деструктивный / недеструктив-ный макро- > 0. 1 г полумикро- 0. 1 - 0. 01 г микро- 0. 01 – 0. 001 г ультрамикро- 10 -6 г субмикро- 10 -9 г макро- / полумикро- / ультрамикро- / субмикро-

 Классификация методов анализа По способу регистрации сигнала Химические (погрешность
Классификация методов анализа По способу регистрации сигнала Химические (погрешность
 Классификация методов анализа По способу регистрации сигнала Химические (погрешность
Классификация методов анализа По способу регистрации сигнала Химические (погрешность
 Классификация методов анализа По способу регистрации сигнала Химические Физические Биологические Физико-химические Спектроскопические Масс-спектральные Основанные на радиоактивности Электрохимические Биохимические Термические
Классификация методов анализа По способу регистрации сигнала Химические Физические Биологические Физико-химические Спектроскопические Масс-спектральные Основанные на радиоактивности Электрохимические Биохимические Термические
 По способу измерения сигнала Спектроскопия Молекулярная Атомная Ядерная Электрохимические методы Вольтамперометрия Потенциометрия Кондуктометрия Кулонометрия Хронопотенциометрия, хроноамперометрия
По способу измерения сигнала Спектроскопия Молекулярная Атомная Ядерная Электрохимические методы Вольтамперометрия Потенциометрия Кондуктометрия Кулонометрия Хронопотенциометрия, хроноамперометрия

 Классификация По объекту анализа х по агрегатному состоянию по химической природе по происхождению объекта по степени распространенности и важности по степени чистоты
Классификация По объекту анализа х по агрегатному состоянию по химической природе по происхождению объекта по степени распространенности и важности по степени чистоты
 Распределительный анализ Анализ распределения элемента по поверхности Анализ распределения элемента по слоям – т. е. распределение по глубине и в целом – по объему. Распределение отдельных фаз по поверхности и по объему
Распределительный анализ Анализ распределения элемента по поверхности Анализ распределения элемента по слоям – т. е. распределение по глубине и в целом – по объему. Распределение отдельных фаз по поверхности и по объему
 Критерии сравнения Аналитические характеристики Метрологические характеристики Требования к пробоподготовке Особенности приборного оснащения Специальные требования, связанные с природой объекта контроля Экономические характеристики
Критерии сравнения Аналитические характеристики Метрологические характеристики Требования к пробоподготовке Особенности приборного оснащения Специальные требования, связанные с природой объекта контроля Экономические характеристики
 Литература 1. Основы аналитической химии. Кн. 2. Методы химического анализа. / Под ред. Ю. А. Золотова. 2 -е изд. М. : Высшая школа, 2004. 2. Аналитическая химия. Физические и физико-химические методы анализа. Под ред. О. М. Петрухина. М. : Химия, 2001. 3. Васильев В. П. Аналитическая химия. Кн. 2. Физико-химические методы анализа. М. : Дрофа, 2004. Дополнительная литература 1. Кристиан Г. Аналитическая химия. В 2 -х т. М. : БИНОМ, 2009. 2. Аналитическая химия. Проблемы и подходы: В 2 -х т. / Под ред. Р. Кельнера, Ж-М. Мерме, М. Отто, Н. Видмера. М. : Мир, 2004. 3. Отто М. Современные методы аналитической химии. В 2 т. М. : Техносфера, 2003.
Литература 1. Основы аналитической химии. Кн. 2. Методы химического анализа. / Под ред. Ю. А. Золотова. 2 -е изд. М. : Высшая школа, 2004. 2. Аналитическая химия. Физические и физико-химические методы анализа. Под ред. О. М. Петрухина. М. : Химия, 2001. 3. Васильев В. П. Аналитическая химия. Кн. 2. Физико-химические методы анализа. М. : Дрофа, 2004. Дополнительная литература 1. Кристиан Г. Аналитическая химия. В 2 -х т. М. : БИНОМ, 2009. 2. Аналитическая химия. Проблемы и подходы: В 2 -х т. / Под ред. Р. Кельнера, Ж-М. Мерме, М. Отто, Н. Видмера. М. : Мир, 2004. 3. Отто М. Современные методы аналитической химии. В 2 т. М. : Техносфера, 2003.
 Инструментальные методы анализа: спектры атомов и молекул Майстренко В. Н. Башкирский государственный университет Кафедра аналитической химии V_maystrenko@mail. ru Тел: 229 -97 -12
Инструментальные методы анализа: спектры атомов и молекул Майстренко В. Н. Башкирский государственный университет Кафедра аналитической химии V_maystrenko@mail. ru Тел: 229 -97 -12
 В арсенале современной аналитической химии важнейшее место занимают методы атомной оптической спектроскопии, основанные на измерении интенсивности электромагнитного излучения, испускаемого или поглощаемого атомами элементов, которые находятся в газо- или парообразном состоянии. Эти методы являются многоэлементными и широко используются для установления состава различных объектов – сплавов, минералов, руд, пищевых продуктов, объектов окружающей среды и др.
В арсенале современной аналитической химии важнейшее место занимают методы атомной оптической спектроскопии, основанные на измерении интенсивности электромагнитного излучения, испускаемого или поглощаемого атомами элементов, которые находятся в газо- или парообразном состоянии. Эти методы являются многоэлементными и широко используются для установления состава различных объектов – сплавов, минералов, руд, пищевых продуктов, объектов окружающей среды и др.

 История атомного спектрального анализа началась с опытов Исаака Ньютона (1666 г) по разложению света в спектр. Первые атомные спектры наблюдали в начале XIX века в ходе астрономических исследований. Возникновение спектрального анализа как метода определения химичес-кого состава вещества относят к 1859 г. , когда немецкие ученые Г. Кирхгоф и Р. Бунзен, исследуя поведение солей металлов в пламени, наблюдали появление линий в спектрах элементов. Густав Кирхгоф (слева) и Роберт Бунзен (справа) Спектроскоп Кирхгофа и Бунзена
История атомного спектрального анализа началась с опытов Исаака Ньютона (1666 г) по разложению света в спектр. Первые атомные спектры наблюдали в начале XIX века в ходе астрономических исследований. Возникновение спектрального анализа как метода определения химичес-кого состава вещества относят к 1859 г. , когда немецкие ученые Г. Кирхгоф и Р. Бунзен, исследуя поведение солей металлов в пламени, наблюдали появление линий в спектрах элементов. Густав Кирхгоф (слева) и Роберт Бунзен (справа) Спектроскоп Кирхгофа и Бунзена

 Эксперимент Бунзена-Кирхгофа А – сигарный ящик, B – часть подзорной трубы, С – подзорная труба, D – газовая горелка Бунзена, E – штатив с солью натрия, F – призма из стекла с CS 2, G – зеркало, H – поворотное устройство
Эксперимент Бунзена-Кирхгофа А – сигарный ящик, B – часть подзорной трубы, С – подзорная труба, D – газовая горелка Бунзена, E – штатив с солью натрия, F – призма из стекла с CS 2, G – зеркало, H – поворотное устройство
 Историческая справка Конец XX века 1960 -е годы ААС, ИСП АЭС ИСП - МС 20 -е годы XX века Середина XIX века Методы количественного анализа Качественный и полуколичественный анализ
Историческая справка Конец XX века 1960 -е годы ААС, ИСП АЭС ИСП - МС 20 -е годы XX века Середина XIX века Методы количественного анализа Качественный и полуколичественный анализ
 Спектры атомов Атомы химических элементов имеют строго определённые частоты, на которых они излучают или поглощают свет. При этом на спектрах элементов наблюдаются светлые или темные линии в определённых местах, характерные для каждого элемента. Атомарные спектры получают переведением веществ в парообраз-ное состояние путём нагревания до 1000- 10000 °C. В качестве источни-ков возбуждения атомов применяют искру, дугу переменного тока, пламя или плазму различных газов, лазеры и др. Спектры поглощения и испускания атомов натрия
Спектры атомов Атомы химических элементов имеют строго определённые частоты, на которых они излучают или поглощают свет. При этом на спектрах элементов наблюдаются светлые или темные линии в определённых местах, характерные для каждого элемента. Атомарные спектры получают переведением веществ в парообраз-ное состояние путём нагревания до 1000- 10000 °C. В качестве источни-ков возбуждения атомов применяют искру, дугу переменного тока, пламя или плазму различных газов, лазеры и др. Спектры поглощения и испускания атомов натрия



 Спектральные линии характеризуют частотой излучения, которая соответствует квантовому переходу между уровнями энергии Еi и Еk атома согласно соотношению h = Еi - Еk , где h – постоянная Планка, а также длиной волны = с / (с – скорость света), волновым числом ’ = 1/ и энергией фотона h. Частоты спектральных линий выражают в обратных секундах (с-1), длины волн – в нм, мкм и ангстремах, волновые числа – в обратных сантиметрах (см-1), энергию фотонов в электронвольтах (э. В). Спектры испускания (эмиссионные) получают при возбуждении атомов различными способами. Время жизни возбужденного состояния 10 -7 – 10 -8 с. В течение этого времени атом испускает квант электро-магнитного излучения и переходит в состояние с более низкой энергией. Спектры поглощения (абсорбционные) наблюдаются при прохож-дении электромагнитного излучения, имеющего непрерывный спектр, через пары или газы атомов. Возникновение оптических спектров и их характер определяет система электронов атома, которые характеризуются четыремя квантовыми числами: главным квантовым числом (уровни K, L, M, N…Q), орбитальным квантовым числом (подуровни s, p, d, f…), магнитным и спиновым квантовыми числами.
Спектральные линии характеризуют частотой излучения, которая соответствует квантовому переходу между уровнями энергии Еi и Еk атома согласно соотношению h = Еi - Еk , где h – постоянная Планка, а также длиной волны = с / (с – скорость света), волновым числом ’ = 1/ и энергией фотона h. Частоты спектральных линий выражают в обратных секундах (с-1), длины волн – в нм, мкм и ангстремах, волновые числа – в обратных сантиметрах (см-1), энергию фотонов в электронвольтах (э. В). Спектры испускания (эмиссионные) получают при возбуждении атомов различными способами. Время жизни возбужденного состояния 10 -7 – 10 -8 с. В течение этого времени атом испускает квант электро-магнитного излучения и переходит в состояние с более низкой энергией. Спектры поглощения (абсорбционные) наблюдаются при прохож-дении электромагнитного излучения, имеющего непрерывный спектр, через пары или газы атомов. Возникновение оптических спектров и их характер определяет система электронов атома, которые характеризуются четыремя квантовыми числами: главным квантовым числом (уровни K, L, M, N…Q), орбитальным квантовым числом (подуровни s, p, d, f…), магнитным и спиновым квантовыми числами.

 Спектр Совокупность спектральных линий, принадлежащих данной частице Термическое возбуждение Эмиссионный спектр Нетермическое возбуждение Спектр люминесценции Быстрая (спонтанная) Спектр флуоресценции (атомы и молекулы) Медленная Спектр фосфоресценции (молекулы)
Спектр Совокупность спектральных линий, принадлежащих данной частице Термическое возбуждение Эмиссионный спектр Нетермическое возбуждение Спектр люминесценции Быстрая (спонтанная) Спектр флуоресценции (атомы и молекулы) Медленная Спектр фосфоресценции (молекулы)
 Спектры атомов с малым числом валентных электронов (щелочные металлы, водород) имеют относительно мало линий (менее 100) в диапазоне 200 - 800 нм. Атомы с более сложными электронными оболочками (элементы побочных групп) имеют спектры с большим числом линий (Cu – более 500, Fe – более 3000, U – несколько тысяч). Линии, обусловленные переходом электронов на основной энергетический уровень, называются резонансными. Вследствие высокой интенсивности они обеспечивают наибольшую чувствитель-ность определений и используются для аналитических целей. Для возбуждения резонансных линий щелочных металлов необхо-дима небольшая энергия, тогда как для неметаллов она высокая и спектры из видимой области смещаются в труднодоступную ультра-фиолетовую область: для Na – 589 нм, Mg – 285 нм, Si – 251 нм, P – 176 нм. Основная область применения атомной спектроскопии – опреде-ление элементов с металлическими и полуметаллическими свойствами. Для получения количественной информации измеряют интенсив-ность одной из спектральных линий определяемого элемента. Процессы, происходящие с атомом при поглощении или испускании фотона, описывают с помощью спектральных термов, характеризующих энергетическое состояние поглощающего или испускающего атома. Спектральные термы получают путем векторного сложения орбитальных моментов и спинов всех электронов атома.
Спектры атомов с малым числом валентных электронов (щелочные металлы, водород) имеют относительно мало линий (менее 100) в диапазоне 200 - 800 нм. Атомы с более сложными электронными оболочками (элементы побочных групп) имеют спектры с большим числом линий (Cu – более 500, Fe – более 3000, U – несколько тысяч). Линии, обусловленные переходом электронов на основной энергетический уровень, называются резонансными. Вследствие высокой интенсивности они обеспечивают наибольшую чувствитель-ность определений и используются для аналитических целей. Для возбуждения резонансных линий щелочных металлов необхо-дима небольшая энергия, тогда как для неметаллов она высокая и спектры из видимой области смещаются в труднодоступную ультра-фиолетовую область: для Na – 589 нм, Mg – 285 нм, Si – 251 нм, P – 176 нм. Основная область применения атомной спектроскопии – опреде-ление элементов с металлическими и полуметаллическими свойствами. Для получения количественной информации измеряют интенсив-ность одной из спектральных линий определяемого элемента. Процессы, происходящие с атомом при поглощении или испускании фотона, описывают с помощью спектральных термов, характеризующих энергетическое состояние поглощающего или испускающего атома. Спектральные термы получают путем векторного сложения орбитальных моментов и спинов всех электронов атома.
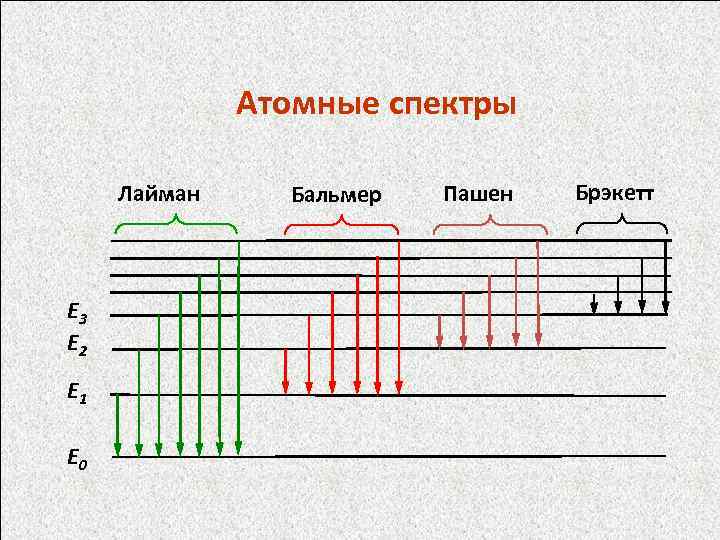
Src="https://present5.com/presentation/89020358_158004652/image-47.jpg" alt="Спектральные термы Формула Бальмера (m > n) Серия Лаймана n = 1 Серия Бальмера:"> Спектральные термы Формула Бальмера (m > n) Серия Лаймана n = 1 Серия Бальмера: n = 2 Серия Пашена: n = 3 Серия Брэкетта: n = 4 Терм: Спектральный терм: R = 109 677 см− 1 – постоянная Ридберга, m – целые числа.

 Спектральные термы многоэлектронных атомов Учет заряда ядра: He+, Li 2+, Be 3+ Учет суммарного орбитального момента и суммарного спина
Спектральные термы многоэлектронных атомов Учет заряда ядра: He+, Li 2+, Be 3+ Учет суммарного орбитального момента и суммарного спина

 Длины волн электромагнитного излучения Интервал длин волн Участок спектра 10 -4 – 0, 1 нм γ-Излучение 0, 01 – 10 нм Рентгеновское излучение 10 – 400 нм Ультрафиолетовое излучение 400 – 760 нм Видимый свет 760 – 106 нм Инфракрасное излучение 10 -3 – 1 м Микроволновое (СВЧ) >1 м Радиоволны
Длины волн электромагнитного излучения Интервал длин волн Участок спектра 10 -4 – 0, 1 нм γ-Излучение 0, 01 – 10 нм Рентгеновское излучение 10 – 400 нм Ультрафиолетовое излучение 400 – 760 нм Видимый свет 760 – 106 нм Инфракрасное излучение 10 -3 – 1 м Микроволновое (СВЧ) >1 м Радиоволны
 Интенсивность спектральных линий Энергия, поглощаемая, излучаемая или рассеиваемая в единицу времени Спектр испускания: Рентгеновская спектроскопия, АЭС, АФС Спектр поглощения: ААС, UV-Vis, ИК, микроволновая и радиочастотная спектроскопия
Интенсивность спектральных линий Энергия, поглощаемая, излучаемая или рассеиваемая в единицу времени Спектр испускания: Рентгеновская спектроскопия, АЭС, АФС Спектр поглощения: ААС, UV-Vis, ИК, микроволновая и радиочастотная спектроскопия
 Ширина спектральных линий естественная УФ: 10 -5 нм тепловое движение (допплеровское уширение) УФ: 10 -3 -10 -2 нм соударение частиц (лоренцево уширение) расщепление энергетических уровней в магнитном поле (эффект Зеемана)
Ширина спектральных линий естественная УФ: 10 -5 нм тепловое движение (допплеровское уширение) УФ: 10 -3 -10 -2 нм соударение частиц (лоренцево уширение) расщепление энергетических уровней в магнитном поле (эффект Зеемана)
 МОЛЕКУЛЯРНЫЕ СПЕКТРЫ - спектры поглощения, испускания или рассеяния, возникающие при квантовых переходах молекул из одного энергетического состояния в другое. Молекулярные спектры определяются составом молекул, их структурой, характером химических связей и взаимодействием с окружающими атомами и молекулами. Наиболее характерными являются молекулярные спектры молекул разреженных газов, которые состоят из узких линий. Молекулярные спектры состоят из электронных, колебательных и вращательных спектров и лежат в диапазоне электромагнитных волн от радиочастот до рентгеновской области спектра. Частоты переходов между вращательными уровнями энергии обычно попадают в микроволновую область, частоты переходов между колебательными уровнями - в ИК-область, а частоты переходов между электронными уровнями - в видимую и УФ-области спектра. Часто вращательные переходы попадают в ИК-область, колебательные - в видимую область, электронные - в ИК-область. Электронные переходы сопровождаются изменением колебательной энергии молекул, а при колебательных переходах изменяется вращательная энергия. Поэтому электронные спектры обычно представляют собой электронно-колебательные полосы. При высоком разрешении обнаруживается и вращательная структура.
МОЛЕКУЛЯРНЫЕ СПЕКТРЫ - спектры поглощения, испускания или рассеяния, возникающие при квантовых переходах молекул из одного энергетического состояния в другое. Молекулярные спектры определяются составом молекул, их структурой, характером химических связей и взаимодействием с окружающими атомами и молекулами. Наиболее характерными являются молекулярные спектры молекул разреженных газов, которые состоят из узких линий. Молекулярные спектры состоят из электронных, колебательных и вращательных спектров и лежат в диапазоне электромагнитных волн от радиочастот до рентгеновской области спектра. Частоты переходов между вращательными уровнями энергии обычно попадают в микроволновую область, частоты переходов между колебательными уровнями - в ИК-область, а частоты переходов между электронными уровнями - в видимую и УФ-области спектра. Часто вращательные переходы попадают в ИК-область, колебательные - в видимую область, электронные - в ИК-область. Электронные переходы сопровождаются изменением колебательной энергии молекул, а при колебательных переходах изменяется вращательная энергия. Поэтому электронные спектры обычно представляют собой электронно-колебательные полосы. При высоком разрешении обнаруживается и вращательная структура.

 Молекулярные спектры веществ: а – гладкий контур, б – следы колебательной структуры, в – спектр поглощения паров антрацена с четкой колебательной структурой
Молекулярные спектры веществ: а – гладкий контур, б – следы колебательной структуры, в – спектр поглощения паров антрацена с четкой колебательной структурой
 Электронные спектры молекул Электронные спектры обусловлены переходами между электронными энергетическими уровнями. Чем определяются электронные спектры? Для атомов электронной конфигурацией атомов Для молекул электронной конфигурацией молекул Электронные переходы в молекулах, как правило, имеют энергию, соответствующую УФ- и видимой областям электромагнитного спектра.
Электронные спектры молекул Электронные спектры обусловлены переходами между электронными энергетическими уровнями. Чем определяются электронные спектры? Для атомов электронной конфигурацией атомов Для молекул электронной конфигурацией молекул Электронные переходы в молекулах, как правило, имеют энергию, соответствующую УФ- и видимой областям электромагнитного спектра.


 Колебательные молекулярные спектры обусловлены квантовыми переходами между колебательными уровнями энергии молекул. Экспериментально наблюдают ИК-спектры поглощения и спектры комбинационного рассеяния (КР-спектры) полученной энергии. В простейшем случае двухатомную молекулу представляют моделью двух взаимодействующих точечных масс M 1 и M 2. При переходе между соседними колебательными уровнями поглощается фотон с энергией h = Ev+1 – Ev и частотой. F
Колебательные молекулярные спектры обусловлены квантовыми переходами между колебательными уровнями энергии молекул. Экспериментально наблюдают ИК-спектры поглощения и спектры комбинационного рассеяния (КР-спектры) полученной энергии. В простейшем случае двухатомную молекулу представляют моделью двух взаимодействующих точечных масс M 1 и M 2. При переходе между соседними колебательными уровнями поглощается фотон с энергией h = Ev+1 – Ev и частотой. F
 Существуют два основных вида колебаний в молекулах: валентные (), при которых атомы совершают колебания вдоль связей, – связи попеременно то растягиваются, то укорачиваются (симметричные и асимметричные колебания); деформационные (), при которых происходит изменение валентных углов между связями одного атома (ножничные, маятниковые, веерные, крутильные колебания). Валентное симметричное (s) Деформационное антисимметричное (аs) (маятниковое) Валентное антисимметричное (as), (a) Деформационное веерное () Деформационное симметричное (s) (ножничное) Деформационное крутильное ()
Существуют два основных вида колебаний в молекулах: валентные (), при которых атомы совершают колебания вдоль связей, – связи попеременно то растягиваются, то укорачиваются (симметричные и асимметричные колебания); деформационные (), при которых происходит изменение валентных углов между связями одного атома (ножничные, маятниковые, веерные, крутильные колебания). Валентное симметричное (s) Деформационное антисимметричное (аs) (маятниковое) Валентное антисимметричное (as), (a) Деформационное веерное () Деформационное симметричное (s) (ножничное) Деформационное крутильное ()
 Нормальные колебания молекулы воды (s) = 3652 см-1 (as) = 3756 см-1 N = 3 n-6 = 3 x 3 – 6 = 3 (s) = 1595 см-1
Нормальные колебания молекулы воды (s) = 3652 см-1 (as) = 3756 см-1 N = 3 n-6 = 3 x 3 – 6 = 3 (s) = 1595 см-1
 Частота колебаний зависит от массы атомов (легче атом – выше частота) C – H 3000 см-1 C – D 2200 см-1 C – O 1100 см-1 C – Cl 700 см-1 Частота колебаний зависит от энергии связи (связь прочнее – выше частота) C С 2143 см-1 C = O 1715 см-1 C – O 1100 см-1
Частота колебаний зависит от массы атомов (легче атом – выше частота) C – H 3000 см-1 C – D 2200 см-1 C – O 1100 см-1 C – Cl 700 см-1 Частота колебаний зависит от энергии связи (связь прочнее – выше частота) C С 2143 см-1 C = O 1715 см-1 C – O 1100 см-1
 Типичные частоты колебаний функциональных групп, см-1 Группа Диапазон частот Валентные колебания Группа Диапазон частот Деформационные колебания (O – H) 3600 – 3000 (O – H), (N – H) 1650 – 1550 (C C), (C N) 2400 – 2100 (C – H) 1450 – 1250 (P – H), (C – H) 2250 – 2100 (C – O), (C – N) 1300 – 1000 (C = O) 1850 – 1650 (C – H), (N – H) 950 – 800 (C = C), (N = O) 1750 - 1600 (Si – O), (P = O) 700 – 550 (N = N) 1650 - 1450 (S – O) 650 - 450 (Si – O), (P = O) 1300 - 1000 (S – O) 1000 – 800 (C – Cl) 750 - 690
Типичные частоты колебаний функциональных групп, см-1 Группа Диапазон частот Валентные колебания Группа Диапазон частот Деформационные колебания (O – H) 3600 – 3000 (O – H), (N – H) 1650 – 1550 (C C), (C N) 2400 – 2100 (C – H) 1450 – 1250 (P – H), (C – H) 2250 – 2100 (C – O), (C – N) 1300 – 1000 (C = O) 1850 – 1650 (C – H), (N – H) 950 – 800 (C = C), (N = O) 1750 - 1600 (Si – O), (P = O) 700 – 550 (N = N) 1650 - 1450 (S – O) 650 - 450 (Si – O), (P = O) 1300 - 1000 (S – O) 1000 – 800 (C – Cl) 750 - 690


 Литература 1. Основы аналитической химии. Кн. 2. Методы химического анализа. / Под ред. Ю. А. Золотова. 2 -е изд. М. : Высшая школа, 2004. 2. Аналитическая химия. Физические и физико-химические методы анализа. Под ред. О. М. Петрухина. М. : Химия, 2001. 3. Васильев В. П. Аналитическая химия. Кн. 2. Физико-химические методы анализа. М. : Дрофа, 2004. Дополнительная литература 1. Кристиан Г. Аналитическая химия. В 2 -х т. М. : БИНОМ, 2009. 2. Аналитическая химия. Проблемы и подходы: В 2 т. / Под ред. Р. Кельнера, Ж-М. Мерме, М. Отто, Н. Видмера. М. : Мир, 2004. 3. Отто М. Современные методы аналитической химии. В 2 т. М. : Техносфера, 2003. 4. Кузяков Ю. Я. , Семененко К. А. , Зоров Н. Б. Методы спектрального анализа. М. : МГУ, 1990. 5. Казицына Л. А. , Куплетская Н. Б. Применение УФ-, ИК- и ЯМР- спектроскопии в органической химии. М. : Высшая школа, 1971.
Литература 1. Основы аналитической химии. Кн. 2. Методы химического анализа. / Под ред. Ю. А. Золотова. 2 -е изд. М. : Высшая школа, 2004. 2. Аналитическая химия. Физические и физико-химические методы анализа. Под ред. О. М. Петрухина. М. : Химия, 2001. 3. Васильев В. П. Аналитическая химия. Кн. 2. Физико-химические методы анализа. М. : Дрофа, 2004. Дополнительная литература 1. Кристиан Г. Аналитическая химия. В 2 -х т. М. : БИНОМ, 2009. 2. Аналитическая химия. Проблемы и подходы: В 2 т. / Под ред. Р. Кельнера, Ж-М. Мерме, М. Отто, Н. Видмера. М. : Мир, 2004. 3. Отто М. Современные методы аналитической химии. В 2 т. М. : Техносфера, 2003. 4. Кузяков Ю. Я. , Семененко К. А. , Зоров Н. Б. Методы спектрального анализа. М. : МГУ, 1990. 5. Казицына Л. А. , Куплетская Н. Б. Применение УФ-, ИК- и ЯМР- спектроскопии в органической химии. М. : Высшая школа, 1971.

Инструментальные (физические и физико-химические) методы анализа основаны на использовании зависимости между измеряемыми физическими свойствами веществ и их качественным и количественным составом. Так как физические свойства веществ измеряются с помощью различных приборов – «инструментов», то эти методы анализа называют также инструментальными методами.
Общее число физико-химических методов анализа довольно велико – оно составляет несколько десятков. Наибольшее практическое значение среди них имеют следующие:
оптические методы, основанные на измерении оптических свойств веществ;
электрохимические методы, основанные на измерении электрохимических свойств системы;
хроматографические методы, основанные на использовании способности различных веществ к избирательной сорбции.
Среди указанных групп наиболее обширной по числу методов и важной по практическому значению является группа оптических методов анализа .
Эмиссионный спектральный анализ. В основе метода лежит измерение интенсивности света, излучаемого веществом (атомами или ионами) при его энергетическом возбуждении, например, в плазме электрического разряда. Метод даёт возможности определять микро- и ультрамикроколичества вещества, анализировать за короткое время несколько элементов.
Пламенная фотометрия является разновидностью эмиссионного анализа. Она основана на использовании газового пламени в качестве источника энергетического возбуждения излучения. Метод в основном используют для анализа щелочных и щелочноземельных металлов.
Абсорбционно-спектральный анализ основан на изучении спектров поглощения лучей анализируемыми веществами. При прохождении через раствор свет или его компоненты поглощаются или отражаются. По величине поглощения или отражения лучей судят о природе и концентрации вещества.
Атомно-абсорбционный анализ. В основе метода лежит измерение поглощения монохроматического излучения атомами определяемого вещества в газовой фазе после атомизации вещества.
Нефелометрический анализ. Основан на отражении света твердыми частицами, взвешенными в растворе. Анализ проводится с помощью приборов нефелометров.
Люминесцентный анализ – это совокупность оптических методов анализа, основанных на люминесценции (свечении вещества, возникающем при его возбуждении различными источниками энергии). По способу (источнику) возбуждения различают: рентгенолюминесценцию – свечение вещества под воздействием рентгеновских лучей; хемилюминесценцию – свечение вещества за счет энергии химической реакции.
В аналитической практике из всех видов люминесценции наибольшее распространение получила флуоресценция, возникающая под действием излучения в УФ и видимой области спектра. Большим достоинством рентгенофлуоресцентного метода является возможность анализа образца без его разрушения, что особенно ценно при анализе уникальных изделий.
Электрохимические методы анализа основаны на изучении и использовании процессов, протекающих на поверхности электрода или в приэлектродном пространстве. Аналитическим сигналом может служить любой электрический параметр (потенциал, сила тока, сопротивление и т. д.), который связан с концентрацией анализируемого раствора функциональной зависимостью и поддающийся измерению.
Различают прямые и косвенные электрохимические методы.
В прямых методах используется зависимость силы тока (потенциала и т. д.) от концентрации определяемого компонента. В косвенных методах силу тока (потенциал и т. д.) измеряют с целью нахождения т. к. т. определяемого компонента подходящим титрантом, т. е. используется зависимость измеряемого параметра от объёма титранта.
К наиболее распространенным электрохимическим методам анализа относятся потенциометрический, вольтамперометрический и кондуктометрический.
Потенциометрический метод основан на измерении электродных потенциалов, которые зависят от активности ионов, а в разбавленных растворах – от концентрации ионов.
Для измерений составляется гальванический элемент из двух электродов: электрода сравнения (электродный потенциал которого известен) и индикаторного электрода, на котором происходит главный процесс – обмен ионами и возникает электродный потенциал, который измеряют путем сравнения. Затем по уравнению Нернста находят количество определяемого компонента.
Потенциометрическое титрование основано на определении точки эквивалентности по результатам потенциометрических измерений. Вблизи точки эквивалентности происходит резкое изменение (скачок) потенциала индикаторного электрода.
Для потенциометрического титрования собирают цепь из индикаторного электрода в анализируемом растворе и электрода сравнения. В качестве электродов сравнения чаще всего применяют каломельный или хлорсеребряный.
Вольтамперометрический метод анализа основан на изучении поляризационных или вольтамперных кривых (кривых зависимости силы тока от напряжения), которые получаются, если при электролизе раствора анализируемого вещества постепенно повышать напряжение и фиксировать при этом силу тока. Электролиз следует проводить с использованием легкополяризуемого электрода с небольшой поверхностью, на котором происходит электровосстановление или электроокисление вещества.
Амперометрическое титрование (потенциометрическое поляризационное титрование) – разновидность вольтамперометрического метода (наряду с полярографией). Оно основано на измерении величины тока между электродами электрохимической ячейки, к которым приложено некоторое напряжение, соответствующее величине предельного тока. По этим данным строят кривую амперометрического титрования в координатах «сила тока – объём титранта» и графически находят точку эквивалентности. В качестве индикаторного электрода в амперометрическом титровании обычно используют вращающиеся платиновые, графитовые и другие твердые электроды.
Примеры решения задач
Пример 1. При открытии катионов серебра Ag + реакцией с хлорид-ионами Сl – в водном растворе по образованию белого осадка хлорида серебра AgCl
Ag + + Cl – ® AgCl↓
предел обнаружения катионов серебра равен 0,1 мкг, предельное разбавление V lim = 1∙ 10 4 мл/г. Определите предельную концентрацию С lim и минимальный объём V min предельно разбавленного раствора.
Решение. Найдем предельную концентрацию С min:
C min = = = 1 ∙ 10 –4 г/мл.
Рассчитаем минимальный объём предельно разбавленного раствора:
V min = = = 0,001 мл.
Таким образом, предельная концентрация предельно разбавленного раствора С min = 1 ∙ 10 -4 г/мл и минимальный объём V min = 0,001 мл.
Пример 2. Катионы серебра Ag + можно открыть реакцией с хромат-ионами CrO по образованию красного осадка хромата серебра Ag 2 CrO 4
2 Ag + + CrO → Ag 2 CrO 4
при V min = 0,02 мл в водном растворе нитрата серебра AgNO 3 с молярной концентрацией С (AgNO 3) = 0,0004 моль/л. Определите предел обнаружения g и предельное разбавление V lim для катиона Ag + .
Решение. Найдем вначале предельную концентрацию катионов серебра, учитывая, что в условии задачи дана концентрация нитрата серебра, выраженная в моль/л:
C
min = = ![]() = 4 ∙ 10 –5 г/мл,
= 4 ∙ 10 –5 г/мл,
где М (Ag +) – атомная масса серебра.
g = C min V min ∙ 10 6 = 4 ∙ 10 –5 ∙ 0,02 ∙ 10 6 = 0,8 мкг,
V lim = = = 2,5 ∙ 10 –4 мл/г.
Таким образом, предел обнаружения для катиона Ag + g = 0,8 мкг, а предельное разбавление V lim =2,5 ∙ 10 –4 мл/г.
Пример 3
Разделить с помощью группового реагента катионы Al +3 и Mg +2 .
Решение. Al +3 относится к катионам IV группы, а Mg +2 – V группы. Групповым реагентом на катионы IV и V групп является гидроксид натрия. В качестве аналитического сигнала наблюдается выпадение в осадок соответствующих гидроксидов:
Al +3 + 3ОН – ⇄ Al(ОН) 3 ↓;
Mg +2 + 2ОН – ⇄ Mg(ОН) 2 ↓.
Однако при добавлении избытка реагента Al(ОН) 3 растворяется с образованием комплексного соединения, а Mg(ОН) 2 – нет:
Al(ОН) 3 + NаОН ⇄ Nа;
Mg(ОН) 2 + NаОН ¹.
Таким образом, при разделении катион Al +3 будет находиться в фильтрате, а катион Mg +2 – в осадке.
Пример 4
Какой объём раствора AgNO 3 с массовой долей 2 % потребуется для осаждения хлорида из навески СаСl 2 ∙ 6 Н 2 О массой 0,4382 г?
Решение. Массу AgNO 3 вычисляем на основании закона эквивалентов.
Инструментальные методы анализа получили название благодаря применению соответствующих инструментов. По определению IUPAC (Международного Союза чистой и прикладной химии), инструментом называют устройство, которое используют для наблюдения определенного объекта, измерения или для сообщения данных о состоянии вещества. Устройство заменяет действия человека, дополняет или увеличивает его возможности.
В инструментальных методах анализа как инструменты применяют разного типа приборы, предназначенные для проведения основных процедур анализа, измерения физических и физико-химических свойств веществ, а также для регистрации результатов измерения. За счет современных компьютеризированных приборов чувствительность анализа может быть существенным образом повышена. Многие физико-химические свойства специфичны.
Все инструментальные (физические и физико-химические) методы основаны на измерении соответствующих физических величин, которые характеризуют определяемое вещество в анализируемом объекте.
Для каждого инструментального метода используют соответствующий аналитический сигнал. В таблице 1 приведенные примеры аналитических сигналов и соответствующих им методов, которые относятся к двум важнейшим группам - к электрохимическим методам анализа и оптическим методам анализа. К этим же группам относят и некоторые другие методы, не показанные в таблице. Например, к числу оптических методов относят люминесцентный, атомно-абсорбционные и другие спектроскопические методы, нефелометрию, турбидиметрию и поляриметрию.
Кроме электрохимических и оптических методов известны и другие группы методов. Так, например, методы, в которых измеряют радиоактивность, относят к ядерно-физическим методам. Используют также масс-спектрометрические методы, термические методы и др. Эта классификация условна и не является единственно возможной.
Зависимость аналитического сигнала от содержания определяемого вещества Х называют градуировочной функцией. Ее записывают как уравнение вида I = f (C) . В этом уравнении символом C обозначают содержание определяемого вещества Х , которое может быть выражено в разных единицах, например единицах количества вещества (моль), единицах массы (г, кг), единицах молярной концентрации (моль/дм 3). Эти единицы прямо пропорциональны между собой. Величину аналитического сигнала в общем случае обозначают символом I , хотя в отдельных методах используют специфические обозначения (см. табл. 1). В каждом методе градуировочные функции однотипные, но точный вид градуировочной функции для конкретной методики зависит от природы определяемого вещества Х и условий измерения сигнала. Так, во всех вариантах рефрактометрического анализа аналитическим сигналом является показатель преломления светового луча (n), который линейно зависит от содержания вещества Х в исследуемом растворе (I = n = a + k С). Это означает, что при рефрактометрическом определении любого вещества градуировочный график прямолинейный, но не проходит через начало координат (рис. 1). Численные же значения констант а и k зависят от того, какой компонент определяют и в каких условиях (растворитель, температура, длина волны) измеряют показатель преломления.
Таблица 1. Примеры инструментальных методов анализа
|
Электрохимические методы |
Аналитический сигнал |
Вид градуировочной функции |
|
|
Первичный, I |
Вторичный, I* |
||
|
Кондуктометрия |
Электрическое сопротивление, R |
Электрическая проводимость, L |
L = a + k |
|
Потенциометрия |
Э.Д.С. электрохимической каморки, Е |
Потенциал электрода, Е |
Е = a + lg b |
|
Вольтамперометрия |
Сила тока, i |
Предельный диффузный ток, i d |
i d = k |
|
Кулонометрия |
Количество электричества, Q |
||
|
Электрогравиметрия |
Масса продукта электролиза, m |
||
|
Оптические методы |
Аналитический сигнал |
Вид градуировочной функции |
|
|
Первичный, I |
Вторичный, I* |
||
|
Атомно-эмиссионный спектральный анализ |
Фототок, i ; относительное почернение, S |
i = a C b S = a + k lgC |
|
|
Спектрофотометрия |
Оптическая плотность, D |
D = l C |
|
|
Рефрактометрия |
Показатель преломления, n |
n = n - n o |
n = n 0 + kC |
Во многих методах зависимость сигнала от концентрации описывается нелинейными функциями, например, в люминесцентном анализе это показательная функция (I = kC n) , в потенциометрии - логарифмическая функция (Е = Е 0 + k lgС) і т.д. Несмотря на указанные отличия, все градуировочные функции похожи тем, что по мере возрастания величины C (содержание определяемого вещества Х ) величина сигнала изменяется беспрерывно, а каждому значению С отвечает только одно значение I .
Градуировочные функции устанавливают экспериментальным путём, используя стандартные образцы сравнения (эталоны), которые содержат различное точно известное количества определяемого вещества Х. Данные, полученные в результате измерения сигнала для каждого эталона, разрешают представить градуировочную функцию в виде таблицы, графика или алгебраической формулы. Если теперь измерять тем же прибором аналитический сигнал исследуемой пробы при тех же условиях, что и сигнал эталона, то по величине такого сигнала можно будет определить содержание Х в исследуемой пробе с помощью градуировочной функции.
Легко рассчитать результат анализа, если сигнал I прямо пропорционален содержанию определяемого вещества Х. Если же такой пропорциональной зависимости не существует, то непосредственно измеренный (первичный) аналитический сигнал I превращают во вторичный аналитический сигнал I *. Выбирают такой способ преобразования, чтобы вторичный аналитический сигнал I * был прямо пропорционален количеству определяемого вещества Х. Так, например, электрическое сопротивление раствора (R ) определённым образом зависит от концентрации растворённого электролита (С). Сопротивление анализируемого раствора легко измерить, но применять R как аналитический сигнал неудобно потому, что при возрастании С величина R уменьшается, причем нелинейно. Поэтому в кондуктометрическом анализе вторичным сигналом является электропроводность раствора L , которая связана с сопротивлением R следующей формулой:
Электропроводность раствора L пропорционально возрастает по мере роста концентрации растворённого сильного электролита. Кроме того, из всех значений L , полученных для однотипных растворов с разной концентрацией Х , можно отнять одну и ту же величину L 0 - электропроводность раствора, который не содержит Х. «Исправленная» величина электропроводности L * = L - L 0 не просто линейно зависит от концентрации Х , а прямо пропорциональная концентрации электролита в растворе, то есть L * = k C.

Рис. 1.1. Типичные градуировочные графики для некоторых инструментальных методов: 1 - рефрактометрия; 2 - люминесцентный анализ; 3 - потенциометрия
Такой приём называется вычитанием фона. В инструментальных методах его используют очень часто. Многие приборы перед началом измерения настраивают так, чтобы они сразу же показывали исправленный сигнал, прямо пропорциональный С. Шкалу такого прибора можно проградуировать прямо в единицах концентрации. Иногда для обеспечения линейности градуировочных графиков превращают не ординату, а абсциссу. Например, в потенциометрическом анализе откладывают по горизонтальной оси не содержимое Х , а его логарифм. А в некоторых вариантах спектрального анализа проводят двойное преобразование - логарифмируют и сигнал, и концентрацию, а потом строят прямолинейную графическую зависимость lgI от lgС .
Современная медицина располагает широкими диагностическими возможностями. Кроме опроса и осмотра пациента используются дополнительные методы исследования. Спектр исследований, проводимых пациентам для постановки диагноза, постоянно расширяется. Некоторые методы исследований применяются всем без исключения пациентам, другие проводятся по индивидуальным показаниям, в зависимости от пути диагностического поиска.
Инструментальные методы исследования – исследования с применением различных аппаратов, приборов и инструментов. Все инструментальные методы можно разделить на две большие группы: неинвазивные и инвазивные.
Неинвазивными называются те методы, которые не сопровождаются нарушением целостности покровных тканей и, соответственно, не сопряжены с возможностью развития осложнений. И подразделяются на:
— рентгенологические (рентгеноскопия, рентгенография, рентгентомография, ангиография, флюорография);
Осложнения – прободение пищевода или желудка, аллергические реакции или на , травматический ларинготрахеит, травмы стенок органов, заворачивание эндоскопа в просвете органа, аспирационные пневмонии.
- RRS — – исследование прямой и сигмовидной кишки – позволяет непосредственно осмотреть слизистую оболочку прямой и сигмовидной кишки (ректоскоп вводится на глубину 25-30 см), выявить наличие воспалительного процесса, внутреннего геморроя, эрозии, кровоизлияния, новообразования, провести прицельную биопсию, получить мазки, выполнить соскобы со слизистой.
Противопоказания – язвенный колит в стадии обострения, ущемленные геморроидальные узлы, трещины анального отверстия в стадии обострения.
Осложнения – прободение кишки, кишечное кровотечение.
- – исследование толстой кишки – позволяет непосредственно осмотреть слизистую оболочку толстой кишки, выявить наличие воспалительного процесса, внутреннего геморроя, трещины, эрозии, кровоизлияния, новообразования, провести прицельную биопсию, получить мазки, выполнить соскобы со слизистой.
Противопоказания – кишечная непроходимость, декомпенсированная недостаточность кровообращения, в стадии обострения, профузное кишечное кровотечение, гипертоническая болезнь III стадии.
Осложнения – прободение кишки при обострении язвенного колита, выраженная болевая реакция на натяжение брыжейки, травмы и кровотечения.
Капсульная интестиноскопия — заключается в проглатывании больным специальной капсулы, снабженной миниатюрной видеокамерой, процессором, системой для передачи информации. Во время прохождения по кишечнику капсула постоянно, со скоростью 2 кадра в секунду, передаёт видеоизображение на полупроводниковое записывающее устройство через систему датчиков, прикрепленных к коже живота. Позже, записывающее устройство подсоединяется к компьютерной рабочей станции, на которой изображения обрабатываются и могут быть просмотрены на мониторе и распечатаны. Общее количество снимков — более 50000. Данным методом можно выявить язвенные поражения тонкой кишки, гельминтоз, кровотечения из тонкой кишки или функциональные нарушения моторики кишечника. Современные капсулы обладают возможностью управления с помощью изменения магнитного поля, подаваемого на брюшную стенку.
- Цистоскопия – исследование полости мочевого пузыря – позволяет непосредственно осмотреть стенки мочевого пузыря, выявить наличие воспалительного процесса, новообразования, провести прицельную биопсию.
Противопоказания – опухоли мочеиспускательного канала.
Осложнения – травмы органов, кровотечения, функциональные расстройства, инфицирование полостей и органов.
- – для диагностики эрозий и язв слизистой оболочки бронха, извлечение инородных тел, удаление полипов бронхов, лечения бронхоэктатической болезни и центрально расположенных абсцессов легкого, вводить лекарственные средства, выполнить прицельную биопсию.
Противопоказания – острая .
Осложнения – коллаптоидное состояние, повреждение стенок бронха, аллергическая реакция на анестетик.
Ультразвуковое исследование
УЗИ-эхография – ультразвуковое исследование – основано на способности ультразвуковых волн, отражаться от тканей и органов с различной плотностью, с регистрацией на экране видеомонитора или фотопленке. Позволяет получить представление о характере патологических изменений в любом паренхиматозном органе.
1.УЗИ органов брюшной полости (печень, желчный пузырь, поджелудочная железа, селезенка) – с помощью ультразвукового метода исследования возможно определение размеров и структуры органов брюшной полости, диагностика патологических изменений органов брюшной полости (конкременты, опухоли, кисты).
- (мочевого пузыря, матки яичников, предстательной железы) – с помощью ультразвукового метода исследования возможно определение размеров и структуры органов малого таза, диагностика патологических изменений органов брюшной полости (конкременты, опухоли, кисты).
- – возможно определение размеров и структуры почек, диагностика патологических изменений в них (конкременты, опухоли, кисты).
- УЗИ органов поверхностной локализации (щитовидная железа, молочные железы, регионарные лимфатические сосуды) — с пециальной подготовки не требуется.
Магнитно-резонансная томография
Магнитно-резонансная томография (МРТ) — современный безопасный (без ионизирующего излучения) неинвазивный диагностический метод, обеспечивающий визуализацию глубоко расположенных биологических тканей, широко применяемый в медицинской практике, в частности в неврологии и нейрохирургии.
Метод магнитно-резонансной томографии МРТ создает возможность визуализировать на экране дисплея, а затем и на рентгеновской пленке срезы черепа и головного мозга, позвоночного столба и спинного мозга.
Информация позволяет дифференцировать серое и белое вещество мозга, судить о состоянии его желудочковой системы, субарахноидального пространства, выявлять многие формы патологии, в частности объемные процессы в мозге, зоны демиелинизации, очаги воспаления и отека, гидроцефалию, травматические поражения, гематомы, , очаги проявления нарушений мозгового кровообращения по ишемическому и геморрагическому типу, кстати, ишемические очаги в мозге могут быть выявлены уже через 2 — 4 ч после инсульта.
Немаловажным преимуществом магнитно-резонансной томографии МРТ перед КТ является возможность получения изображения в любой проекции: аксиальной, фронтальной, сагиттальной. Это позволяет визуализировать субтенториальное пространство, позвоночный канал, выявить невриному слухового нерва в полости внутреннего слухового прохода, опухоль гипофиза, субдуральную гематому в подостром периоде, даже в тех случаях, когда на КТ она не визуализируется.
Методика магнитно-резонансной томографии (МРТ-исследования) заключается в помещении пациента в горизонтальном положении в узкий тоннель томографа, время зависит от вида исследования. Пациент должен сохранять полную неподвижность исследуемой анатомической области.
Радиоизотопные исследования
Радиоизотопные исследования — все методы основаны на одном принципе: изотопы различных химических элементов принимают участие в физиологических процессах, протекающих в организме, точно также как аналогичные стабильные (радиоактивные) вещества. Введение в организм радионуклидов дает возможность с высокой достоверностью определить их количество в органах и биологических средах (с учетом введенной пациенту активности).
- Сканирование — используют для исследования печени, поджелудочной железы, почек, щитовидной железы.
Для проведения сканирования пациенту в/в вводится Au (198) или J (131). Сканирование производят через 40-50 минут с помощью специального прибора — сканера, основной частью которого является детектор ядерного излучения, автоматически передвигающейся над областью исследуемого органа в двух перпендикулярных направлений. При помощи специального пишущего устройства результаты измерения активности записывается на бумаге или фотопленке в виде штрихов строчка за строчкой, причем частота и интенсивность штриховки зависят от активности, накопленной в органе.
Таким образом, в результате сканирования получается сканограммаплоскостное изображение исследуемого органа, позволяющее по характеру штриховки судить о степени, особенностях накопления и распределения изотопа в тканях органа. В настоящее время используется цветное сканирование, при котором на сканограмме участки с различной степенью наполнения изотопа воспроизводятся различными цветами. При оценке сканограммы учитываются размеры и форма изображения, интенсивность штриховки на различных участках, наличие «дефектов наполнения» — отсутствие штриховки на отдельных участках.
- Функциональное исследование органов и систем – основано на одном принципе: определение скорости и степени поступления, накопления или распределения и выведения изотопов и меченых соединений в органах и системах организма.
Радиоактивный элемент, вводится пациенту обычно в/в, а затем с помощью датчиков радиометрических приборов, регистрируется исходящее от органов или тканей излучение и записывается в виде графического изображения или в цифровых величинах.
Данный метод в настоящее время наиболее широко применяется для диагностики патологии щитовидной железы, например двухфазный тест с радиоактивным йодом, результаты которого отражают накопления J 131 в щитовидной железе или концентрацию йода в плазме.
- Радиоиммуногорманальные исследования – в последние годы этот вид радиоизтопной диагностики приобретает все большее значение, т.к. обладает по сравнению с обычной иммунной и биохимической диагностикой очень высокой чувствительностью и специфичностью и позволяет определить содержание в сыворотке крови многих гормонов и ферментов.
Исследование проводится «в пробирке», исследуемый материал – сыворотка крови пациента, к которой добавляется соответствующий меченый гормон с определенной активностью, а также специфические . Затем в сравнении со специальными стандартами с высокой степенью точности определяется в концентрации исследуемого гормона тли фермента, — например, эндогенного , пепсина, ангиотензина, гастрина, секретина.
Лапароскопия
Эндоскопическое исследование полостей, не связанных с внешней средой – лапароскопия – это метод исследования, заключающийся во введении в брюшную полость специального эндоскопа – лапароскопа через небольшой разрез с целью непосредственной визуализации патологического процесса.
Лапароскоп представляет из себя металлическую трубку диаметром 5 мм со сложной системой линз и световодом.
В объектив лапароскопа можно смотреть глазом — так это делалось на протяжении многих десятилетий. Однако в последние тридцать лет с появлением миниатюрных эндоскопических видеокамер (сейчас они весят весом 50 г), присоединяемых к объективу лапароскопа, для всех, кто находится в операционной стало возможным наблюдать весь ход операции на экране монитора.
РОССИЙСКАЯ ФЕДЕРАЦИЯ
«УТВЕРЖДАЮ»:
И. о. проректора-начальник
управления по научной работе
_______________________
2011 г.
очной и заочной форм обучения
«______»___________2011 г.
Рассмотрено на заседании кафедры органической и экологической химии
Соответствует требованиям к содержанию, структуре и оформлению.
Объем 12 стр.
Зав. кафедрой ______________________________/ /
«______»___________ 2011 г.
Рассмотрено на заседании УМК ИМЕНИТ
«______»_____________2011 г., протокол №
Соответствует ФГТ к структуре основной профессиональной образовательной программы послевузовского профессионального образования (аспирантура)
«СОГЛАСОВАНО»:
Председатель УМК ________________________/ /
«______»_____________2011 г.
«СОГЛАСОВАНО»:
Нач. отдела аспирантуры
и докторантуры______________________
«______»_____________2011 г.
РОССИЙСКАЯ ФЕДЕРАЦИЯ
МИНИСТЕРСТВО ОБРАЗОВАНИЯ И НАУКИ
Государственное образовательное учреждение
высшего профессионального образования
ТЮМЕНСКИЙ ГОСУДАРСТВЕННЫЙ УНИВЕРСИТЕТ
Институт математики, естественных наук и информационных технологий
Кафедра органической и экологической химии
НОВЫЕ ИНСТРУМЕНТАЛЬНЫЕ МЕТОДЫ В АНАЛИТИЧЕСКОЙ ХИМИИ
Учебно-методический комплекс. Рабочая программа
для аспирантов специальности 02.00.02 Аналитическая химия
очной и заочной форм обучения
Тюменский государственный университет
2011
Новые инструментальные методы в аналитической химии. Учебно-методический комплекс. Рабочая программа для аспирантов специальности 02.00.02 Аналитическая химия. Тюмень, 2011, 12 стр.
Рабочая программа составлена в соответствии с ФГТ к структуре основной профессиональной образовательной программы послевузовского профессионального образования (аспирантура).
ОТВЕТСТВЕННЫЙ РЕДАКТОР: заведующий кафедрой органической и экологической химии, д. п.н., профессор
© Тюменский государственный университет, 2011.
Пояснительная записка Цели и задачи дисциплины
Цель дисциплины: освоение современных инструментальных методов исследования, применяющихся в химии и необходимых для эффективного освоения основной профессиональной образовательной программы послевузовского профессионального образования (аспирантура) по специальности 02.00.02 Аналитическая химия и подготовки кандидатской диссертации.
Задачи дисциплины: освоение аспирантами следующих вопросов:
Теоретические основы инструментальных методов (структурные модели молекул и твердых тел, взаимодействие вещества с излучением); практическое применение инструментальных методов в современной аналитической химии.
Место дисциплины в структуре ОПППО
Дисциплина «Новые инструментальные методы в аналитической химии» относится к циклу специальных дисциплин отрасли науки и научной специальности.
Для успешного освоения данной дисциплины обучающиеся должны владеть теоретическими представлениями в области строения химических веществ, основами спектральных, дифракционных, хроматографических и электрохимических методов.
Освоение дисциплины «Новые инструментальные методы в аналитической химии» необходимо для выполнения диссертационного исследования.
Требования к результатам освоения дисциплины
Процесс изучения дисциплины направлен на формирование следующих компетенций:
Общие компетенции
- использование основных законов естественнонаучных дисциплин в профессиональной деятельности, применение методов математического анализа и моделирования, теоретического и экспериментального исследования; владение основными методами, способами и средствами получения, хранения, переработки информации, имение навыков работы с компьютером как средством управления информацией.
Профессиональные компетенции
- понимание сущности и социальной значимости профессии, основных перспектив и проблем, определяющих конкретную область деятельности — аналитическую химию; знание теоретических основ инструментальных методов исследования; владение навыками аналитического химического эксперимента и обработки экспериментальных данных.
В результате освоения дисциплины обучающийся должен:
Знать: теоретические основы спектральных, дифракционных, хроматографических и электрохимических методов исследования; структурные модели молекул.
Уметь: собирать и анализировать научную, технологическую и статистическую информацию; планировать экспериментальные научные исследования в области аналитической химии, обрабатывать экспериментальные данные, подготавливать к публикации статьи и тезисы докладов.
Владеть: современными методами экспериментальных исследований в области аналитической химии, методами математической статистики и математического моделирования, информационными технологиями, в т. ч. методами работы с компьютером и электронными базами данных.
Трудоемкость дисциплины
Дисциплина преподается в 5 семестре. Форма промежуточной аттестации — зачет. Общая трудоемкость дисциплины составляет 3 зачетных единицы, 108 час.
Тематический план
Таблица 1
Тематический план
Всего часов | виды учебной работы и самостоятельная работа, в час. | Формы контроля |
|||||
семинарские занятия | лабораторные занятия | самостоятельная работа |
|||||
Теоретические основы инструментальных методов |
|
||||||
Спектральные и дифракционные методы анализа |
Защита лаборат. работ |
||||||
Сепарационные и электрохимические методы анализа |
Защита лаборат. работ |
||||||
Таблица 2
Планирование самостоятельной работы аспирантов
Разделы дисциплины и междисциплинарные связи с обеспечиваемыми (последующими) дисциплинами
Содержание дисциплины
Тема 1. Теоретические основы инструментальных методов
Основы учения о строении молекул. Стационарные состояния: электронные, колебательные, вращательные, ядерные спиновые. Квантовые переходы между стационарными состояниями, вероятности и правила отбора. Типы молекулярных спектров: электронные, колебательно-вращательные, ЯМР, фотоэлектронные. Методы регистрации и обработки спектров. Качественный, количественный и структурный спектральный анализ.
Дифракция электромагнитных волн и электронных пучков на точечных объектах и кристаллах.
Адсорбционные характеристики органических молекул. Хроматограмма и ее характеристики, методы регистрации и обработки. Время удерживания и индексы удерживания, их связь со строением молекул сорбата и сорбента. Основные методики хроматографического анализа. Качественный, количественный и структурный хроматографический анализ.
Строение растворов электролитов. Электрохимические процессы и их механизмы.
Тема 2. Спектральные и дифракционные методы
Идентификация химических соединений спектральными методами: использование УФ-, ИК - и ЯМР-спектроскопии и масс-спектрометрии. Рентгеновская спектроскопия: метод РФЭС, метод протяженной тонкой структуры рентгеновского поглощения (ПТСРП, EXAFS). Связь спектра с природой исследуемого вещества. Возможности и ограничения.
Количественное определение химических элементов и соединений спектральными методами. Чувствительность, селективность и точность анализа. Специфика методики анализа в экологическом мониторинге. Структурный спектральный анализ. Определение структурных фрагментов молекулы (радикалы, функциональные группы, тип скелета, кратные связи и т. д.).
Современные дифрактометрические методы: рентгеновская дифрактометрия, дифракция низкоэнергетических (медленных) электронов (LEED), рассеяние ионных пучков низкой энергии (LEIS), рассеяние рентгеновских лучей при малых углах (XANES), просвечивающая / сканирующая электронная микроскопия.
Сканирующая туннельная микроскопия.
Использование спектральных методов для исследования структуры молекул и твердых тел, катализаторов, механизмов химических реакций.
Идентификация органических соединений хроматографическими методами: использование ГЖХ - и ВЭЖХ-методов. Методы повышения качества хроматограммы, подбор детекторов, колонок, неподвижных фаз, элюентов, температурных режимов. Капиллярный электрофорез. Возможности и ограничения сепарационных методов.
Количественное определение ионов и органических соединений сепарационными методами. Чувствительность, селективность и точность анализа. Специфика методики анализа в экологическом мониторинге.
Структурный хроматографический анализ. Индексы удерживания, их связь со строением молекул. Определение структурных фрагментов молекулы (радикалы, функциональные группы, тип скелета, кратные связи и т. д.).
Новое в электрохимических методах анализа: потенциометрии, вольтамперометрии, кулонометрии, электрогравиметрии.
Планы семинарских занятий.
Семинарские занятия учебным планом не предусмотрены
Темы лабораторных работ. (Лабораторный практикум)
Тема 2. Спектральные и дифракционные методы анализа
Лабораторная работа № 1 (6 час.). Тема работы: Раздельное определение содержания насыщенных и ароматических соединений в образце нефти. Объект исследования: образец нефти или нефтепродукта (бензин, дизельное топливо, масло). Используемые методы: снятие УФ - и ИК-спектров, их обработка и интерпретация.
Лабораторная работа № 2 (6 час.). Тема работы: Определение структуры молекулы. Объект исследования: образец нефтяного ароматического углеводорода. Используемые методы: снятие УФ - и ИК-спектров, их обработка и интерпретация, определение числа и типа заместителей в ароматическом ядре молекулы.
Тема 3. Сепарационные и электрохимические методы анализа
Лабораторная работа № 3 (6 час.). Тема работы: Качественный анализ образца нефтепродукта (бензин, дизельное топливо). Объект исследования: продажный бензин или дизельное топливо. Используемые методы: получение хроматограммы с помощью газового хроматографа. Идентификация компонентов смеси с помощью базы данных. Вычисление относительного содержания компонентов в смеси.
Лабораторная работа № 4 (6 час.). Тема работы: Изучение кинетики реакции алкилирования. Объект исследования: бутандиол-1,4, аллилхлорид, оксид пиридина. Используемые методы: отбор проб реакционной среды, химический анализ продуктов реакции (моно - и диаллиловый эфиры бутандиола), определение выхода продуктов, вычисление активности и селективности катализатора.
Примерная тематика курсовых работ.
Курсовые работы учебным планом не предусмотрены
Учебно-методическое обеспечение самостоятельной работы аспирантов.
Оценочные средства для текущего контроля успеваемости, промежуточной аттестации по итогам освоения дисциплины (модуля).
Основным принципом организации самостоятельной работы является комплексный подход, направленный на стимулирование у аспирантов следующих видов деятельности по получению компетенций:
репродуктивной – выполнение заданий по образцу с целью закрепления теоретических знаний, формирования умений и навыков (прочтение, просмотр, конспектирование, прослушивание, запоминание; ответы на вопросы для самопроверки; повторение учебного материала, решение типовых задач);
реконструктивной – выполнение заданий с обязательным преобразованием информации (подготовка к аудиторным занятиям, тематическим дискуссиям; подготовка сообщений, докладов и выступлений на семинарских занятиях; подбор литературы; выполнение контрольных работ; решение практических задач);
творческой – отбор и критический анализ информации (написание рефератов, докладов; участие в научно-исследовательской работе, выполнение специальных творческих заданий; подготовка проектов и слайдовых презентаций).
Перечень контрольных вопросов для зачета
Стационарные состояния атомов и молекул: электронные, колебательные, вращательные, ядерные спиновые. Квантовые переходы между стационарными состояниями, вероятности и правила отбора. Типы атомных и молекулярных спектров: электронные, колебательно-вращательные, ЯМР, фотоэлектронные. Методы регистрации и обработки спектров. Качественный, количественный и структурный спектральный анализ. Дифракция электромагнитных волн и электронных пучков на точечных объектах и кристаллах. Адсорбционные характеристики органических молекул. Хроматограмма и ее характеристики, методы регистрации и обработки. Время удерживания и индексы удерживания, их связь со строением молекул сорбата и сорбента. Основные методики хроматографического анализа. Качественный, количественный и структурный хроматографический анализ. Строение растворов электролитов. Электрохимические процессы и их механизмы. Идентификация химических соединений спектральными методами: использование УФ-, ИК - и ЯМР-спектроскопии и масс-спектрометрии. Рентгеновская спектроскопия: метод РФЭС, метод протяженной тонкой структуры рентгеновского поглощения (ПТСРП, EXAFS). Связь спектра с природой исследуемого вещества. Возможности и ограничения. Количественное определение химических элементов и соединений спектральными методами. Чувствительность, селективность и точность анализа. Структурный спектральный анализ. Определение структурных фрагментов молекулы (радикалы, функциональные группы, тип скелета, кратные связи и т. д.). Современные дифрактометрические методы: рентгеновская дифрактометрия, дифракция низкоэнергетических (медленных) электронов (LEED), рассеяние ионных пучков низкой энергии (LEIS), рассеяние рентгеновских лучей при малых углах (XANES), просвечивающая / сканирующая электронная микроскопия. Сканирующая туннельная микроскопия. Использование спектральных методов для исследования структуры молекул и твердых тел, катализаторов, механизмов химических реакций. Идентификация органических соединений хроматографическими методами: использование ГЖХ - и ВЭЖХ-методов. Методы повышения качества хроматограммы, подбор детекторов, колонок, неподвижных фаз, элюентов, температурных режимов. Капиллярный электрофорез. Возможности и ограничения сепарационных методов. Количественное определение ионов и органических соединений сепарационными методами. Чувствительность, селективность и точность анализа. Структурный хроматографический анализ. Индексы удерживания, их связь со строением молекул. Определение структурных фрагментов молекулы (радикалы, функциональные группы, тип скелета, кратные связи и т. д.). Новое в электрохимических методах анализа: потенциометрии, вольтамперометрии, кулонометрии, электрогравиметрии.
Примерная тематика контрольных работ и опросов
1. Электронные переходы в органических молекулах
2. Колебательно-вращательные переходы в органических молекулах
3. Спиновые ядерные переходы в органических молекулах
4. Адсорбционные свойства органических молекул
5. Методы математической обработки молекулярных спектров
6. Методы математической обработки хроматограмм
7. Дифракционные методы исследования
8. Методы исследования механизмов реакций
9. Современные спектральные и хроматографические приборы
Примерные тесты и вопросы для самоконтроля
Спектральные методы:
1. Какие признаки положены в основу деления шкалы электромагнитных волн на диапазоны и каковы особенности оптического диапазона?
2. Как связано волновое число с длиной волны?
1) ν = λ; 2) Δν = –Δλ/λ2; 3) ν = с/λ; 4) ν = 1/λ..
3. Наибольшая энергия требуется:
1) для возбуждения электронов;
2) для возбуждения колебаний атомов в молекуле;
3) для возбуждения вращений молекулы;
4) для переориентации спинов ядер.
4. Каково соотношение между энергиями электронных Ее, колебательных Еυ и вращательных Еr состояний молекулы?
1) Еe > Еυ > Еr ; 2) Еυ > Еr > Еe ; 3) Еr > Еe > Еυ ; 4) Еr > Еυ > Еe.
5. При рассмотрении спектров какого типа необходимо учитывать принцип Франка-Кондона?
1) ИК-. 2) вращательных. 3) КР-. 4) электронных.
6. В каких областях спектра наблюдаются электронно-колебательно-вращательные, колебательно-вращательные и вращательные спектры?
7. В каких областях спектра проявляются переходы между электронными, колебательными и вращательными состояниями молекул?
1) Колебательные — в ИК-области, вращательные — в УФ-области, электронные — в микроволновой.
2) Колебательные — в микроволновой, электронные — в УФ-области, вращательные — в ИК-области.
3) Колебательные — в ИК-области, вращательные — в микроволновой, электронные — в УФ-области.
4) Колебательные — в УФ-области, электронные — в ИК-области, вращательные — в микроволновой.
8. Методы анализа, основанные на измерении поглощенного образцом света, называются:
1) радиометрией; 2) абсорбциометрией; 3) флюориметрией;
4) турбидиметрией.
Хроматографические методы:
Для какой цели проводят кондиционирование хроматографических колонок? Почему эту процедуру проводят без подключения колонки к детектору? Какое отношение диаметра колонки и размера зерен сорбента является оптимальным для насадочных колонок? Если объем колонки составляет 45 мл, какой объем насадки нужно взять для заполнения колонки? Какой механизм лежит в основе обработки минеральных носителей диметилдихлорсиланом, триметилхлорсиланом и гексаметилдисилазаном? В каком случае образуются опасные газообразные продукты? Если на хроматограмме время удерживания додекана и тетрадекана составляет 12,4 и 14,7 мин, соответственно, какое число теоретических тарелок для этой колонки будет больше: рассчитанное 1) как по додекану так и по тетрадекану, 2) по додекану, 3) по тетрадекану? Если ВЭТТ для металлической колонки (2 м × 3 мм) заполненной полимерным сорбентом Porapak N (80-100 меш) при анализе пробы пропана в гелии (С = 0,3 % об.) составляет 8,3; 6,6; 2,1; 2,7; 4,5 и 5,4 мм при объемной скорости гелия 10; 13; 15; 20; 30 и 40 мл/мин, то какой будет оптимальная скорость газа-носителя для эффективного разделения пропана, изобутана и н-бутана? Можно ли определить мертвое время по воздуху детектором ДТП при использовании хроматографической колонки, заполненной молекулярным ситом СаХ (колонка 2 м × 3 мм, фракция сорбента 0,25-0,30 мм, скорость гелия – 15 мл/мин, температура термостата: 45 °С)? Если анализируемую пробу (объемом 1 мкл) вводили в испаритель хроматографа микрошприцами на 1 и 10 мкл по 5 раз, в каком случае среднее квадратичное отклонение высот и площадей хроматографических пиков будет больше? Какой фактор является определяющим при постоянном времени удерживания анализируемого соединения (скорость газа-носителя, точность поддержания температуры термостата колонок, одинаковая процедура ввода пробы микрошприцом в испаритель)? Если график зависимости исправленных времен удерживания нормальных углеводородов додекан (С12) – тетракозан (С24) имеет перелом после элюирования С21, что можно сказать о температурном режиме термостата колонки (капиллярная колонка НР-5, 30 м × 0,32 мм, линейная скорость гелия – 30 см/с)? Какие соединения могут быть использованы в качестве стандартов при определении индексов удерживания в биохимических исследованиях проб методом газовой хроматографии? Какая комбинация последовательно-работающих детекторов позволит определить концентрацию метилтретбутилового эфира (МТБЭА) в бензине марки А-92? Какой детектор предпочтителен при определении соединений серы в нефти и нефтепродуктах? Какова величина окна поиска индексов Ковача углеводородов в сложной смеси? Какие неподвижные фазы можно использовать при установлении индивидуального состава бензина методом капиллярной газовой хроматографии?
Критерии оценки СРС:
качество освоения учебного материала (умение студента использовать теоретические знания при выполнении практических задач); проработанность всех аспектов задания, оформление материала в соответствии с требованиями, соблюдение установленных сроков представления работы на проверку; степень самостоятельности, творческой активности, инициативности аспирантов, наличие элементов новизны в процессе выполнения заданий.Итоги СРС подводятся во время контрольных недель, сроки которых определяются графиком учебного процесса.
Образовательные технологии.
Виды учебной работы | Образовательные технологии |
Аудиторные | а) Чтение лекций (мультимедийные и видео-демонстрации, письменное тестирование по пройденному материалу (4 теста по 10 вопросов в каждом). б) Проведение лабораторных занятий (разработка плана эксперимента, групповое обсуждение и анализ проблем, мультимедийные демонстрации, заслушивание и обсуждение устных докладов, сообщений, выступлений, встречи с преподавателями других дисциплин). в) Интерактивные технологии (групповые дискуссии, разбор конкретных ситуаций). |
Самостоятельная работа | а) Изучение учебной и методической литературы, т. ч. поиск информации в электронных сетях и базах данных, подготовка презентаций. б) Подготовка к контрольным работам в) Подготовка лабораторных работ к защите (с использованием мультимедийных презентаций) |
11.1. Основная литература:
1. , Аналитическая химия. М.: ИЦ «Академия». 2011.
2. Периодические журналы: «Аналитическая химия», «Успехи химии», «Российский химический журнал» за 2001-2011 гг.
11.2. Дополнительная литература:
1. , Планирование и математическая обработка результатов химического эксперимента. Омск: Изд-во ОмГУ. 2005.
2. Практический курс атомно-абсорбционного анализа. Курс лекций. Екатеринбург. 2003.
3. Методы исследования катализаторов / под ред. Дж. Томаса и Р. Лемберта. М., Мир, 1983.
11.3. Программное обеспечение и Интернет – ресурсы:
www. e-library. ru
chem. /rus/teaching/analyt/
www. ftchemistry. dsmu. /ana_him/lek_13.html
Технические средства и материально-техническое обеспечение дисциплины (модуля).
Лекции обеспечены мультимедийными презентациями и видеофильмами. Для чтения лекций необходимо наличие аудиторий, оснащенных мультимедийной техникой (компьютер, проектор и др.).
Для проведения лабораторных работ имеются оборудованные лаборатории спектроскопии (117, корп. 5) и хроматографии (116, корп. 5).
Для самостоятельной работы аспирантов необходим доступ в компьютерный класс, имеющий выход в Интернет.