Elemente transuranice. Elemente chimice Progrese în sinteza de noi elemente chimice
Patru noi elemente chimice au fost adăugate oficial în tabelul periodic. Astfel a fost completat al șaptelea rând al ei. Elemente noi - 113, 115, 117 și 118 - au fost sintetizate artificial în laboratoare din Rusia, SUA și Japonia (adică nu există în natură). Cu toate acestea, recunoașterea oficială a descoperirilor făcute de un grup de experți independenți a trebuit să aștepte până la sfârșitul anului 2015: Uniunea Internațională de Chimie Pură și Aplicată a anunțat reaprovizionarea pe 30 decembrie 2015.
Toate elementele „noi” au fost sintetizate în condiții de laborator folosind nuclee atomice mai ușoare. Pe vremuri, era posibil să izolați oxigenul prin arderea oxidului de mercur - dar acum oamenii de știință trebuie să petreacă ani de zile și să folosească acceleratori masivi de particule pentru a descoperi elemente noi. În plus, aglomerările instabile de protoni și neutroni (așa apar elemente noi pentru oamenii de știință) se lipesc împreună doar pentru o fracțiune de secundă înainte de a se rupe în „fragmente” mai mici, dar mai stabile.
Acum echipele care au primit și au dovedit existența unor elemente noi ale tabelului au dreptul să propună nume noi pentru aceste elemente, precum și simboluri cu două litere pentru a le desemna.
Elementele pot fi denumite după una dintre proprietățile lor chimice sau fizice sau după numele unui mineral, al unui loc sau al unui om de știință. Numele se poate baza și pe nume mitologice.
În prezent, elementele au nume de lucru disonante - ununtrium (Uut), ununpentium (Uup), ununseptium (Uus) și ununoctium (Uuo) - care corespund denumirilor latine ale numerelor din numărul lor.
Materialul modern și baza tehnică de producție este compusă în proporție de aproximativ 90% din doar două tipuri de materiale: metale și ceramică. Aproximativ 600 de milioane de tone de metal sunt produse anual în lume - peste 150 kg. pentru fiecare locuitor al planetei. Aproximativ aceeași cantitate de ceramică este produsă împreună cu cărămizi. Producția de metal costă de sute și de mii de ori mai mult, producția de ceramică este mult mai ușoară din punct de vedere tehnic și mai rentabilă din punct de vedere economic și, cel mai important, ceramica se dovedește în multe cazuri a fi un material structural mai potrivit în comparație cu metalul.
Folosind elemente chimice noi - zirconiu, titan, bor, germaniu, crom, molibden, wolfram etc. Recent, au fost sintetizate ceramică rezistentă la foc, rezistentă la căldură, rezistentă la chimicale, cu duritate mare, precum și ceramică cu un set de proprietăți electrofizice specificate.
Material superdur - hexanit-R, ca una dintre soiurile cristaline de nitrură de bor, cu un punct de topire de peste 3200 0 C și o duritate apropiată de duritatea diamantului, are o vâscozitate record, adică nu este la fel de fragil ca toate. alte materiale ceramice. Astfel, una dintre cele mai dificile probleme științifice și tehnice ale secolului a fost rezolvată: până acum, toate ceramicele structurale aveau un dezavantaj comun - fragilitatea, dar acum s-a făcut un pas pentru a o depăși.
Marele avantaj al ceramicii tehnice din noua compoziție este că din aceasta se realizează piesele de mașini prin presarea pulberilor pentru a obține produse finite de forme și dimensiuni date.
Astăzi putem numi o altă proprietate unică a ceramicii - supraconductivitatea la temperaturi peste punctul de fierbere al azotului; această proprietate deschide un spațiu fără precedent pentru progresul științific și tehnologic, pentru crearea de motoare super-puternice și generatoare electrice, crearea transportului de levitație magnetică. , dezvoltarea acceleratoarelor electromagnetice super-puternice pentru lansarea sarcinilor utile în spațiu etc.
Chimia compușilor organosiliciului a făcut posibilă crearea unei producții pe scară largă a unei game largi de polimeri cu ignifuge, hidrofuge, izolație electrică și alte proprietăți valoroase. Acești polimeri sunt indispensabili într-o serie de industrii energetice și aviatice.
Fluorocarburile sunt tetrafluormetanul, hexafluoretanul și derivații lor, unde atomul de carbon poartă o sarcină pozitivă slabă, iar atomul de fluor cu electronegativitatea inerentă fluorului are o sarcină negativă slabă. Drept urmare, fluorocarburile au o stabilitate excepțională chiar și în medii foarte agresive de acizi și alcaline, activitate specială la suprafață și capacitatea de a absorbi oxigen și peroxizi. Prin urmare, ele sunt folosite ca material pentru protezele organelor interne umane.
Întrebarea 57. Procese chimice și procese vitale. Catalizatori și enzime.
Cercetările recente intense au vizat elucidarea atât compoziției materiale a țesuturilor vegetale și animale, cât și a proceselor chimice care au loc în organism. Ideea rolului principal al enzimelor, propusă pentru prima dată de marele naturalist francez Louis Pasteur (1822-1895), rămâne fundamentală până în prezent. În același timp, biochimia statică studiază compoziția moleculară și structura țesutului organismelor vii și nevii.
Biochimia dinamică s-a născut la începutul secolelor al XVIII-lea și al XIX-lea, când au început să facă distincția între procesele de respirație și fermentație, asimilare și disimilare ca anumite transformări ale substanțelor.
Cercetarea fermentației constituie subiectul principal fermentatie - ramură de bază a cunoștințelor despre procesele vieții. Pe parcursul unei istorii foarte lungi de cercetare, procesul de biocataliză a fost luat în considerare din două puncte de vedere diferite. Unul dintre ele, numit în mod convențional chimic, a fost aderat de J. Liebig și M. Berthelot, iar celălalt, biologic, a fost aderat de L. Pasteur.
În conceptul chimic, toată cataliza a fost redusă la o cataliză chimică obișnuită. În ciuda abordării simplificate, în cadrul conceptului au fost stabilite prevederi importante: o analogie între biocataliză și cataliză, între enzime și catalizatori; prezența a două componente inegale în enzime - centrii activi și purtători; concluzie despre rolul important al ionilor metalelor de tranziție și al centrilor activi ai multor enzime; concluzie despre extinderea legilor cineticii chimice la biocataliză; reducerea în unele cazuri a biocatalizei la cataliză prin agenți anorganici.
La începutul dezvoltării sale, conceptul biologic nu avea dovezi experimentale atât de extinse. Principalul său suport l-au constituit lucrările lui L. Pasteur și, în special, observațiile sale directe asupra activității bacteriilor lactice, care au făcut posibilă identificarea fermentației și a capacității microorganismelor de a obține energia de care au nevoie pentru viață prin fermentație. Din observațiile sale, Pasteur a concluzionat că enzimele aveau un nivel special de organizare materială. Cu toate acestea, toate argumentele sale, dacă nu au fost infirmate, au fost cel puțin retrogradate în plan secund după descoperirea fermentației extracelulare, iar poziția lui Pasteur a fost declarată vitalistă.
Cu toate acestea, de-a lungul timpului, conceptul lui Pasteur a câștigat. Promisiunea acestui concept este evidențiată de cataliză evolutivă modernă și biologia moleculară. Pe de o parte, s-a stabilit că compoziția și structura moleculelor de biopolimer reprezintă un singur set pentru toate ființele vii, care este destul de accesibil pentru studierea proprietăților fizice și chimice - aceleași legi fizice și chimice guvernează atât procesele abiogene, cât și procesele vieții. Pe de altă parte, s-a dovedit specificul excepțional al viețuitoarelor, manifestat nu numai în cele mai înalte niveluri de organizare celulară, ci și în comportamentul fragmentelor de sisteme vii la nivel molecular, care reflectă tiparele altor niveluri. Specificul nivelului molecular al viețuitoarelor constă în diferența semnificativă între principiile de acțiune a catalizatorilor și enzimelor, în diferența dintre mecanismele de formare a polimerilor și biopolimerilor, a căror structură este determinată numai de codul genetic și , în sfârșit, în faptul său neobișnuit: multe reacții chimice de oxidare-reducere într-o celulă vie pot avea loc fără contact direct între moleculele care reacţionează. Aceasta înseamnă că transformările chimice pot avea loc în sistemele vii care nu au fost detectate în lumea neînsuflețită.
La începutul anului 2011, IUPAC a recunoscut colaborarea JINR cu LLNL (SUA) ca având prioritate în descoperirea elementelor 114 și 116, care au fost denumite: element 114 - Flerovium, Fl; 116 element ― Livermorium, Lv.
Flerovium - în onoarea Laboratorului de Reacții Nucleare care poartă numele. G.N. Flerov JINR, care este un lider recunoscut în domeniul sintezei elementelor supergrele, și fondatorul său, remarcabilul fizician Academician G.N. Flerov (1913−1990) - autorul descoperirii unui nou tip de radioactivitate de fisiune spontană a grelelor nuclei, fondatorul unui număr de noi direcții științifice, fondatorul și primul director al FLNR JINR, care îi poartă acum numele.
Livermorium - în onoarea Laboratorului Național Livermore. Lawrence și locația sa - orașul Livermore (California, SUA). Oamenii de știință de la Livermore participă de mai bine de 20 de ani la experimente privind sinteza de noi elemente, efectuate în Dubna.
În general, decizia IUPAC este o recunoaștere a contribuției remarcabile a oamenilor de știință JINR la descoperirea „insulei stabilității” elementelor supergrele, care este una dintre cele mai importante realizări ale fizicii nucleare moderne.
Există, de asemenea, restricții privind existența nucleelor atomice din elemente supergrele. Elementele cu Z > 92 nu au fost găsite în condiții naturale. Calculele folosind modelul picăturii lichide prezic dispariția barierei de fisiune pentru nucleele cu Z2/A ≈ 46 (aproximativ elementul 112). În problema sintezei nucleelor supergrele ar trebui să se distingă două domenii de probleme.
- Ce proprietăți ar trebui să aibă nucleele supergrele? Vor exista numere magice în această regiune Z și N. Care sunt principalele canale de descompunere și timpii de înjumătățire ale nucleelor supergrele?
- Ce reacții ar trebui folosite pentru a sintetiza nuclee supergrele, tipuri de nuclee de bombardare, valori așteptate ale secțiunii transversale, energii de excitație așteptate ale nucleului compus și canale de deexcitare?
Deoarece formarea nucleelor supergrele are loc ca urmare a fuziunii complete a nucleului țintă și a particulei incidente, este necesar să se creeze modele teoretice care să descrie dinamica procesului de fuziune a două nuclee care se ciocnesc într-un nucleu compus.
Problema sintetizării elementelor supergrele este strâns legată de faptul că nucleele cu Z,N = 8, 20, 28, 50, 82, N = 126 (numere magice) au stabilitate crescută în raport cu diferitele moduri de dezintegrare radioactivă. Acest fenomen este explicat în cadrul modelului cochiliei - numerele magice corespund cochiliilor umplute. În mod firesc, apare întrebarea cu privire la existența următoarelor numere magice în Z și N. Dacă acestea există în regiunea diagramei N-Z a nucleelor atomice N > 150, Z > 101, nucleele supergrele ar trebui observate cu timpi de înjumătățire crescut, adică trebuie să existe o Insulă de Stabilitate. În lucrare, pe baza calculelor efectuate folosind potențialul Woods-Saxon ținând cont de interacțiunea spin-orbită, s-a arătat că ar trebui să se aștepte o creștere a stabilității nucleelor pentru un nucleu cu Z = 114, adică următorul învelișul de protoni umplut corespunde cu Z = 114, învelișul de neutroni umplut corespunde numărului N ~
184. Obuzele închise pot crește semnificativ înălțimea barierei de fisiune și, în consecință, pot crește durata de viață a nucleului. Astfel, în această regiune de nuclee (Z = 114, N ~
184) ar trebui să cauți Insula Stabilității. Același rezultat a fost obținut independent în lucrare.
Nuclei cu Z = 101–109 au fost descoperiți înainte de 1986 și au fost denumiti: 101 - Md (Menelevium), 102 - No (Nobelium), 103 - Lr (Lawrencium), 104 - Rf (Rutherfordium, 106 - Sg (Seaborgium), 107 - Ns (Nielsborium), 108 - Hs (Hassium), 109 - Mt (Meitnerium). Ținând cont de meritele cercetătorilor din Dubna în descoperirea unui număr mare de izotopi ai elementelor grele (102-105), în 1997, prin hotărâre a Adunării Generale de Chimie Pură și Aplicată, elementului denumit Dubnium (Db) i s-a atribuit Z = 105. Acest element era numit anterior Ha (Hannium).
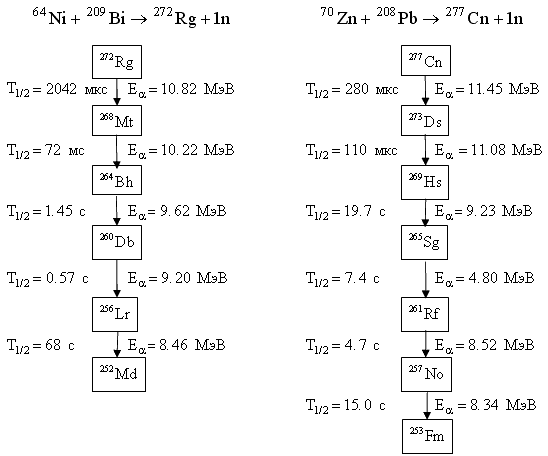
Orez. 12.3. Lanțuri de dezintegrare ale izotopilor Ds (Z = 110), Rg (Z = 111), Cn (Z = 112).
O nouă etapă în studiul nucleelor supergrele a început în 1994, când eficiența de înregistrare a fost semnificativ crescută și tehnica de observare a nucleelor supergrele a fost îmbunătățită. Ca rezultat, au fost descoperiți izotopii Ds (Z = 110), Rg (Z = 111) și Cn (Z = 112).
Pentru a obține nuclee supergrele, s-au folosit fascicule accelerate de 50 Ti, 51 V, 58 Fe, 62 Ni, 64 Ni, 70 Zn și 82 Se. Izotopii 208 Pb și 209 Bi au fost utilizați ca ținte. Diferiți izotopi ai elementului 110 au fost sintetizați la Laboratorul de Reacții Nucleare, numit după. G.N. Flerov folosind reacția 244 Pu(34 S,5n) 272 110 și la GSI (Darmstadt) în reacția 208 Pb(62 Ni,n) 269 110. Izotopii 269 Ds, 271 Ds, 272 Rg și 277 Cn au fost înregistrați conform la lanţurile lor de dezintegrare (Fig. 12.3).
Un rol major în producerea elementelor supergrele îl joacă modelele teoretice, cu ajutorul cărora se calculează caracteristicile așteptate ale elementelor chimice și reacțiile în care se pot forma.
Pe baza diferitelor modele teoretice, au fost calculate caracteristicile de dezintegrare ale nucleelor supergrele. Rezultatele unui astfel de calcul sunt prezentate în Fig. 12.4. Timpurile de înjumătățire ale nucleelor chiar și supergrele sunt date în raport cu fisiunea spontană (a), α-desintegrarea (b), β-desintegrarea (c) și pentru toate procesele de dezintegrare posibile (d). Cel mai stabil nucleu în raport cu fisiunea spontană (Fig. 12.4a) este nucleul cu Z = 114 și N = 184. Pentru acesta, timpul de înjumătățire față de fisiunea spontană este de ~10 16 ani. Pentru izotopii elementului 114 care diferă de cel mai stabil cu 6-8 neutroni, timpii de înjumătățire scad cu
10-15 ordine de mărime. Timpurile de înjumătățire relativ la dezintegrarea α sunt prezentate în Fig. 12.5b. Miezul cel mai stabil este situat în regiunea Z = 114 și N = 184 (T 1/2 = 10 15 ani).
În Fig. 12,4 V cu puncte întunecate. În fig. Figura 12.4d prezintă timpii de înjumătățire total, care pentru nucleele pare-pare situate în interiorul conturului central sunt de ~10 5 ani. Astfel, după luarea în considerare a tuturor tipurilor de dezintegrare, se dovedește că nucleele din vecinătatea Z = 110 și N = 184 formează o „insulă a stabilității”. Nucleul 294110 are un timp de înjumătățire de aproximativ 109 ani. Diferența dintre valoarea Z și numărul magic 114 prezis de modelul învelișului se datorează competiției dintre fisiune (față de care nucleul cu Z = 114 este cel mai stabil) și dezintegrarea α (față de care nucleele cu Z inferior sunt stabile). ). Nucleele impar-pare și par-impar au timpi de înjumătățire relativ la
Dezintegrarea α și fisiunea spontană cresc, iar în raport cu dezintegrarea β acestea scad. Trebuie remarcat faptul că estimările de mai sus depind puternic de parametrii utilizați în calcule și pot fi considerate doar ca indicii ale posibilității existenței nucleelor supergrele cu durate de viață suficient de lungi pentru detectarea lor experimentală.

Orez. 12.4. Timpurile de înjumătățire calculate pentru nucleele supergrele par-chi (numerele reprezintă timpii de înjumătățire în ani):
a - în ceea ce privește fisiunea spontană, b - α-decay, c - e-capture și β-decay, d - pentru toate procesele de dezintegrare
Rezultatele unui alt calcul al formei de echilibru a nucleelor supergrele și al timpilor lor de înjumătățire sunt prezentate în Fig. 12.5, 12.6. În fig. Figura 12.5 arată dependența energiei de deformare a echilibrului de numărul de neutroni și protoni pentru nucleele cu Z = 104-120. Energia de deformare este definită ca diferența dintre energiile nucleelor aflate în echilibru și forma sferică. Din aceste date este clar că în regiunea Z = 114 și N = 184 ar trebui să existe nuclee care au formă sferică în starea fundamentală. Toate nucleele supergrele descoperite până în prezent (sunt prezentate în Fig. 12.5 ca diamante întunecate) sunt deformate. Diamantele ușoare prezintă nuclee care sunt stabile în raport cu degradarea β. Aceste nuclee trebuie să se descompună prin dezintegrare α sau fisiune. Canalul principal de dezintegrare ar trebui să fie α-decay.
Timpurile de înjumătățire pentru izotopii β-stabili chiar și chiar sunt prezentate în Fig. 12.6. Conform acestor predicții, timpii de înjumătățire sunt așteptați pentru majoritatea nucleelor mult mai lungi decât cele observate pentru nucleele supergrele deja descoperite (0,1–1 ms). De exemplu, pentru nucleul 292 Ds, este prezisă o durată de viață de ~ 51 de ani.
Astfel, conform calculelor microscopice moderne, stabilitatea nucleelor supergrele crește brusc pe măsură ce se apropie de numărul magic al neutronilor N = 184. Până de curând, singurul izotop al elementului Z = 112 Cn (coperniciu) era izotopul 277 Cn, care are un timp de înjumătățire de 0,24 ms. Izotopul mai greu 283 Cn a fost sintetizat în reacția de fuziune la rece 48 Ca + 238 U. Timpul de iradiere a fost de 25 de zile. Numărul total de 48 de ioni de Ca pe țintă este de 3,5·1018. Au fost înregistrate două cazuri care au fost interpretate ca fisiune spontană a izotopului rezultat 283 Cn. Timpul de înjumătățire estimat al acestui nou izotop este T 1/2 = 81 s. Astfel, este clar că o creștere a numărului de neutroni în izotopul 283 Cn față de izotopul 277 Cn cu 6 unități crește durata de viață cu 5 ordine de mărime.
În fig. 12.7 luate din lucrare, perioadele de dezintegrare α măsurate experimental sunt comparate cu rezultatele calculelor teoretice bazate pe modelul picăturii lichide fără a lua în considerare structura învelișului nucleelor. Se poate observa că pentru toate nucleele grele, cu excepția izotopilor ușoare ai uraniului, efectele învelișului cresc timpul de înjumătățire cu 2-5 ordine de mărime pentru majoritatea nucleelor. Structura învelișului nucleului are o influență și mai puternică asupra timpilor de înjumătățire ale fisiunii relativ spontane. Creșterea timpului de înjumătățire pentru izotopii Pu este de câteva ordine de mărime și crește pentru izotopul de 260 Sg.
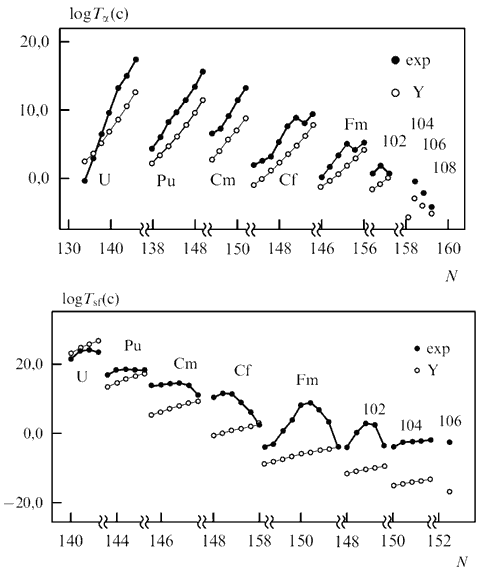
Orez. 12.7. Timpurile de înjumătățire măsurate experimental (● exp) și calculate teoretic (○ Y) ale elementelor transuraniu pe baza modelului picăturii lichide, fără a lua în considerare structura învelișului nucleului. Imaginea de sus este timpul de înjumătățire pentru dezintegrarea α, imaginea de jos este timpul de înjumătățire pentru fisiunea spontană.
În fig. Figura 12.8 prezintă durata de viață măsurată a izotopilor de seaborgiu Sg (Z = 106) în comparație cu predicțiile diferitelor modele teoretice. De remarcat este scăderea duratei de viață a izotopului cu N = 164 cu aproape un ordin de mărime în comparație cu durata de viață a izotopului cu N = 162.
Cea mai apropiată apropiere de insula de stabilitate poate fi realizată în reacția 76 Ge + 208 Pb. Un nucleu foarte greu aproape sferic poate fi format într-o reacție de fuziune urmată de emisia de γ cuante sau a unui singur neutron. Conform estimărilor, nucleul rezultat de 284 114 ar trebui să se descompună odată cu emisia de particule α cu un timp de înjumătățire de ~ 1 ms. Informații suplimentare despre ocuparea cochiliei în regiunea N = 162 pot fi obținute prin studierea dezintegrarilor α ale nucleelor de 271 Hs și 267 Sg. Pentru aceste nuclee sunt prezise timpi de înjumătățire de 1 min. si 1 ora. Pentru nucleele 263 Sg, 262 Bh, 205 Hs, 271.273 Ds, este de așteptat izomerie, motiv pentru care este umplerea subcociilor cu j = 1/2 și j = 13/2 în regiunea N = 162 pentru nucleele deformate în starea fundamentală.
În fig. Figura 12.9 prezintă funcțiile de excitație măsurate experimental pentru reacția de formare a elementelor Rf (Z = 104) și Hs (Z = 108) pentru reacțiile de fuziune ale ionilor incidenti 50 Ti și 56 Fe cu nucleul țintă 208 Pb.
Nucleul compus rezultat este răcit prin emisia a unul sau doi neutroni. Informațiile despre funcțiile de excitare ale reacțiilor de fuziune cu ioni grei sunt deosebit de importante pentru obținerea nucleelor supergrele. În reacția de fuziune a ionilor grei, este necesar să se echilibreze cu precizie efectele forțelor Coulomb și ale forțelor de tensiune superficială. Dacă energia ionului incident nu este suficient de mare, atunci distanța minimă de apropiere nu va fi suficientă pentru fuziunea sistemului nuclear binar. Dacă energia particulei incidente este prea mare, atunci sistemul rezultat va avea o energie de excitație mare și cel mai probabil se va dezintegra în fragmente. Fuziunea eficientă are loc într-un interval energetic destul de îngust de particule care se ciocnesc.

Fig. 12.10. Diagrama potențialelor pentru fuziunea 64 Ni și 208 Pb.
Reacțiile de fuziune cu emisia unui număr minim de neutroni (1–2) prezintă un interes deosebit, deoarece în nucleele supergrele sintetizate, este de dorit să existe cel mai mare raport N/Z posibil. În fig. Figura 12.10 prezintă potențialul de fuziune pentru nuclee în reacția 64 Ni + 208 Pb → 272 Ds. Cele mai simple estimări arată că probabilitatea efectului de tunel pentru fuziunea nucleară este de ~10–21, ceea ce este semnificativ mai mic decât valoarea secțiunii transversale observată. Acest lucru poate fi explicat după cum urmează. La o distanță de 14 fm între centrele nucleelor, energia cinetică inițială de 236,2 MeV este complet compensată de potențialul Coulomb. La această distanță, doar nucleonii aflați pe suprafața nucleului sunt în contact. Energia acestor nucleoni este scăzută. Prin urmare, există o mare probabilitate ca nucleonii sau perechile de nucleoni să părăsească orbitalii într-un nucleu și să se deplaseze în stările libere ale nucleului partener. Transferul de nucleoni de la un nucleu incident la un nucleu țintă este deosebit de atractiv în cazul în care izotopul de plumb dublu magic 208 Pb este utilizat ca țintă. În 208 Pb, subînvelișul de protoni h 11/2 și subînvelișurile de neutroni h 9/2 și i 13/2 sunt umplute. Inițial, transferul de protoni este stimulat de forțele de atracție proton-proton, iar după umplerea subînvelișului h 9/2 - de forțele de atracție proton-neutron. În mod similar, neutronii se deplasează în subînvelișul liber i 11/2, atrași de neutroni din subînvelișul deja umplut i 13/2. Datorită energiei de împerechere și momentelor unghiulare orbitale mari, transferul unei perechi de nucleoni este mai probabil decât transferul unui singur nucleon. După transferul a doi protoni din 64 Ni 208 Pb, bariera Coulomb scade cu 14 MeV, ceea ce favorizează contactul mai strâns al ionilor care interacționează și continuarea procesului de transfer de nucleoni.
În lucrările lui [V.V. Volkov. Reacții nucleare de transferuri inelastice profunde. M. Energoizdat, 1982; V.V. Volkov. Izv. Academia de Științe a URSS, seria fizică, 1986, vol. 50 p. 1879] a fost studiat în detaliu mecanismul reacției de fuziune. Se arată că deja în stadiul de captare se formează un sistem nuclear dublu după disiparea completă a energiei cinetice a particulei incidente și nucleonii unuia dintre nuclei sunt transferați treptat, coajă cu coajă, către celălalt nucleu. Adică, structura învelișului nucleelor joacă un rol semnificativ în formarea miezului compus. Pe baza acestui model, a fost posibil să se descrie destul de bine energia de excitație a nucleelor compuși și secțiunea transversală pentru formarea elementelor Z = 102–112 în reacțiile de fuziune la rece.
Astfel, progresul în sinteza elementelor transuraniu Z = 107–112 a fost asociat cu „descoperirea” reacțiilor de fuziune la rece în care izotopii magici 208 Pb și 209 Bi au fost iradiați cu ioni cu Z = 22–30. Nucleul format în reacția de fuziune la rece este slab încălzit și se răcește ca urmare a emisiei unui neutron. Așa s-au obținut pentru prima dată izotopii elementelor chimice cu Z = 107–112. Aceste elemente chimice au fost obținute în perioada 1978–1998. în Germania la un accelerator special construit la centrul de cercetare GSI din Darmstadt. Cu toate acestea, progresul suplimentar către nuclee mai grele folosind această metodă se dovedește a fi dificil din cauza creșterii barierei potențiale dintre nucleele care se ciocnesc. Prin urmare, în Dubna a fost implementată o altă metodă de producere a nucleelor supergrele. S-au folosit cei mai grei izotopi ai elementelor chimice obținute artificial plutoniu Pu (Z = 94), americiu Am (Z = 95), curiu Cm (Z = 96), berkeliu Bk (Z = 97) și californiu Cf (Z = 98). ca tinte.. Ca ioni accelerați a fost ales izotopul de calciu 48 Ca (Z = 20). O vedere schematică a separatorului și detectorului de nuclee de recul este prezentată în Fig. 12.11.
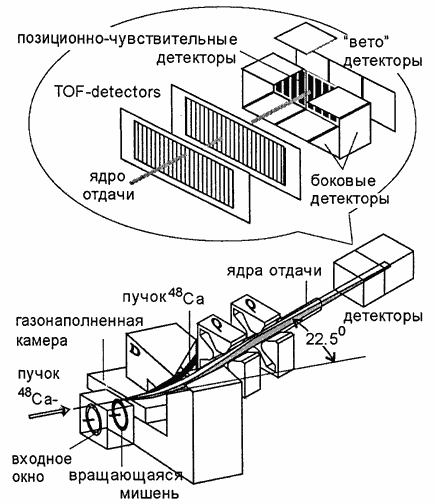
Orez. 12.11. Vedere schematică a separatorului de nuclee de recul, unde se desfășoară experimente privind sinteza elementelor supergrele în Dubna.
Separatorul magnetic al nucleelor de recul reduce fondul produselor secundare de reacție de 10 5 – 10 7 ori. Produsele de reacție au fost înregistrate folosind un detector de siliciu sensibil la poziție. Au fost măsurate energia, coordonatele și timpul de zbor al nucleelor de recul. După oprire, toate semnalele ulterioare de la particulele de degradare detectate trebuie să vină din punctul de oprire al nucleului implantat. Tehnica creată a făcut posibilă stabilirea cu un grad ridicat de fiabilitate (≈ 100%) a unei legături între un nucleu supergreu oprit în detector și produsele sale de descompunere. Folosind această tehnică, elemente supergrele cu
Z = 110–118 (Tabelul 12.2).
Tabelul 12.2 prezintă caracteristicile elementelor chimice supergrele cu Z = 110–118: numărul de masă A, m - prezența unei stări izomerice într-un izotop cu număr de masă A, paritatea spin JP, energia de legare nucleară Est, energia de legare specifică ε, energiile de separare a neutronilor B n și protonul B p , timpul de înjumătățire T 1/2 și principalele canale de dezintegrare.
Elementele chimice Z > 112 nu au încă denumiri și sunt date în notații internaționale acceptate.
Tabelul 12.2
Caracteristicile elementelor chimice supergrele Z = 110–118
| XX-A-m | J P | Greutate sâmburi, MeV |
EST, MeV |
ε, MeV |
Bn, MeV |
Bp, MeV |
T 1/2 | Moduri de dezintegrare |
|---|---|---|---|---|---|---|---|---|
| Z = 110 − darmstadtium | ||||||||
| Ds-267 | 248787.19 | 1934.5 | 7.2 | 0.7 | 2,8 ac | α ≈100% | ||
| Ds-268 | 0 + | 249718.08 | 1943.2 | 7.3 | 8.7 | 1.3 | 100 ac | α ≈ |
| Ds-269 | 250650.86 | 1950.0 | 7.2 | 6.8 | 1.3 | 179 ac | α 100% | |
| Ds-270 | 0 + | 251581.97 | 1958.4 | 7.3 | 8.5 | 0,10 ms | α ≈100%, SF< 0.20% | |
| Ds-270-m | 251583.07 | 1957.3 | 7.2 | 6,0 ms | α >70%, IT ≤ 30% | |||
| Ds-271 | 252514.72 | 1965.2 | 7.3 | 6.8 | 2.2 | 1,63 ms | α ≈100% | |
| Ds-271-m | 252514.72 | 1965.2 | 7.3 | 69 ms | IT?, α >0% | |||
| Ds-272 | 0 + | 253446.46 | 1973.1 | 7.3 | 7.8 | 2.5 | 1 s | SF |
| Ds-273 | 254380.32 | 1978.8 | 7.2 | 5.7 | 2.5 | 0,17 ms | α ≈100% | |
| Ds-274 | 0 + | 255312.45 | 1986.2 | 7.2 | 7.4 | 3.0 | 2 s | α?, SF? |
| Ds-275 | 256246.44 | 1991.8 | 7.2 | 5.6 | 2.9 | 2 s | α? | |
| Ds-276 | 0 + | 257178.73 | 1999.1 | 7.2 | 7.3 | 3.2 | 5 s | SF?, α? |
| Ds-277 | 258112.63 | 2004.7 | 7.2 | 5.7 | 3.1 | 5 s | α? | |
| Ds-278 | 0 + | 259044.92 | 2012.0 | 7.2 | 7.3 | 10 s | SF?, α? |
|
| Ds-279 | 259978.62 | 2017.9 | 7.2 | 5.9 | 0,18 s | SF ≈90%, α ≈10% |
||
| Ds-281 | 261844.60 | 2031.0 | 7.2 | 9,6 s | SF ≈100% | |||
| Z =111 − roentgeniu | ||||||||
| Rg-272 | 253452.75 | 1965.5 | 7.2 | 0.2 | 3,8 ms | α ≈100% | ||
| Rg-273 | 254384.34 | 1973.5 | 7.2 | 8.0 | 0.4 | 5 ms | α? | |
| Rg-274 | 255317.74 | 1979.6 | 7.2 | 6.2 | 0.9 | 6,4 ms | α ≈100% | |
| Rg-275 | 256249.53 | 1987.4 | 7.2 | 7.8 | 1.2 | 10 ms | α? | |
| Rg-276 | 257183.22 | 1993.3 | 7.2 | 5.9 | 1.5 | 100 ms | SF?, α? |
|
| Rg-277 | 258115.72 | 2000.4 | 7.2 | 7.1 | 1.3 | 1 s | α?, SF? |
|
| Rg-278 | 259049.11 | 2006.5 | 7.2 | 6.2 | 1.8 | 4,2 ms | α ≈100%, SF |
|
| Rg-279 | 259981.41 | 2013.8 | 7.2 | 7.3 | 1.8 | 0,17 s | α ≈100% | |
| Rg-280 | 260914.80 | 2020.0 | 7.2 | 6.2 | 2.1 | 3,6 s | α ≈100% | |
| Rg-281 | 261847.09 | 2027.2 | 7.2 | 7.3 | 1m | α?, SF? | ||
| Rg-282 | 262780.59 | 2033.3 | 7.2 | 6.1 | 2.3 | 4 m | SF?, α? | |
| Rg-283 | 263712.98 | 2040.5 | 7.2 | 7.2 | 10 m | SF?, α? | ||
| Z = 112 − coperniciu | ||||||||
| Cn-277 | 258119.32 | 1995.5 | 7.2 | 2.2 | 0,69 ms | α ≈100% | ||
| Cn-278 | 0 + | 259051.20 | 2003.1 | 7.2 | 7.7 | 2.8 | 10 ms | SF?, α? |
| Cn-279 | 259984.69 | 2009.2 | 7.2 | 6.1 | 2.7 | 0,1 s | SF?, α? | |
| Cn -280 | 0 + | 260916.69 | 2016.8 | 7.2 | 7.6 | 3.0 | 1 s | α?, SF? |
| Cn-282 | 0 + | 262782.18 | 2030.4 | 7.2 | 3.2 | 0,50 ms | SF ≈100% | |
| Cn-283 | 263715.57 | 2036.6 | 7.2 | 6.2 | 3.3 | 4,0 s | α ≥90%, SF ≤10% | |
| Cn-284 | 0 + | 264647.66 | 2044.1 | 7.2 | 7.5 | 3.6 | 101 ms | SF ≈100% |
| Cn -285 | 265580.76 | 2050.5 | 7.2 | 6.5 | 34 s | α ≈100% | ||
| Z=113 | ||||||||
| Uut-278 | 0,24 ms | α 100% | ||||||
| Uut-283 | 263719.46 | 2031.4 | 7.2 | 1.0 | 100 ms | α 100% | ||
| Uut-284 | 264652.45 | 2038.0 | 7.2 | 6.6 | 1.4 | 0,48 s | α ≈100% | |
| Uut-285 | 265584.55 | 2045.5 | 7.2 | 7.5 | 1.4 | 2 m | α?, SF? | |
| Uut-286 | 266517.64 | 2051.9 | 7.2 | 6.5 | 1.4 | 5 m | α?, SF? | |
| Uut-287 | 267449.64 | 2059.5 | 7.2 | 7.6 | 20 m | α?, SF? | ||
| Z=114 | ||||||||
| Uuq-286 | 0 + | 266520.33 | 2048.0 | 7.2 | 2.5 | 0,16 s | SF ≈60%, α ≈40% | |
| Uuq-287 | 267453.42 | 2054.4 | 7.2 | 6.5 | 2.5 | 0,51 s | α ≈100% | |
| Uuq-288 | 0 + | 268385.02 | 2062.4 | 7.2 | 8.0 | 2.9 | 0,80 s | α ≈100% |
| Uuq-289 | 269317.91 | 2069.1 | 7.2 | 6.7 | 2,7 s | α ≈100% | ||
| Z=115 | ||||||||
| Uup-287 | 267458.11 | 2048.4 | 7.1 | 0.5 | 32 ms | α 100% | ||
| Uup-288 | 268390.81 | 2055.3 | 7.1 | 6.9 | 0.9 | 87 ms | α 100% | |
| Uup-289 | 269322.50 | 2063.2 | 7.1 | 7.9 | 0.8 | 10 s | SF?, α? | |
| Uup-290 | 270255.30 | 2070.0 | 7.1 | 6.8 | 0.9 | 10 s | SF?, α? | |
| Uup-291 | 271187.09 | 2077.7 | 7.1 | 7.8 | 1m | α?, SF? | ||
| Z=116 | ||||||||
| Uuh-290 | 0 + | 270258.98 | 2065.0 | 7.1 | 1.8 | 15 ms | α ≈100% | |
| Uuh-291 | 271191.78 | 2071.7 | 7.1 | 6.8 | 1.8 | 6,3 ms | α 100% | |
| Uuh-292 | 0 + | 272123.07 | 2080.0 | 7.1 | 8.3 | 2.3 | 18 ms | α ≈100% |
| Uuh-293 | 53 ms | α ≈100% | ||||||
| Z=117 | ||||||||
| Uus-291 | 271197.37 | 2064.9 | 7.1 | -0.1 | 10 ms | SF?, α? | ||
| Uus-292 | 272129.76 | 2072.0 | 7.1 | 7.2 | 0.3 | 50 ms | SF?, α? | |
| Z=118 | ||||||||
| Uuo-294 | 0 + | 1,8 ms | α ≈100% | |||||
În fig. Figura 12.12 prezintă toți cei mai grei izotopi cunoscuți cu Z = 110–118 obținuți în reacțiile de sinteză, indicând timpul de înjumătățire măsurat experimental. Poziția prezisă teoretic a insulei de stabilitate este de asemenea prezentată aici (Z = 114, N = 184).

Orez. 12.12. Diagrama N-Z a elementelor Z = 110–118.
Rezultatele obținute indică clar o creștere a stabilității izotopilor pe măsură ce se apropie de nucleul dublu magic (Z = 114, N = 184). Adăugarea a 7-8 neutroni la nuclee cu Z = 110 și 112 crește timpul de înjumătățire de la 2,8 ca (Ds-267) la ≈ 10 s (Ds-168, Ds 271). Timpul de înjumătățire T 1/2 (272 Rg, 273 Rg) ≈ 4–5 ms crește la T 1/2 (283 Rg) ≈ 10 min. Cei mai grei izotopi ai elementelor Z = 110–112 conțin ≈ 170 de neutroni, ceea ce este încă departe de numărul magic N = 184. Toți cei mai grei izotopi cu Z > 111 și N > 172 se descompun în principal ca urmare a
α-desintegrare, fisiune spontană - o descompunere mai rară. Aceste rezultate sunt în acord cu predicțiile teoretice.
La Laboratorul de Reacții Nucleare care poartă numele. G.N. Flerov (Dubna) a sintetizat un element cu Z = 114. S-a folosit reacția
Identificarea nucleului 289 114 a fost efectuată folosind un lanț de descompunere α. Evaluarea experimentală a timpului de înjumătățire al izotopului 289 114 ~30 s. Rezultatul obtinut este in buna concordanta cu calculele efectuate anterior.
În timpul sintezei elementului 114 în reacția 48 Cu + 244 Pu, s-a observat randamentul maxim de izotopi cu Z = 114 în canal cu evaporarea a trei neutroni. În acest caz, energia de excitație a nucleului compus 289 114 a fost de 35 MeV.
Secvența prezisă teoretic a descompunerilor care apar cu nucleul 296 116 format în reacția 248 Cm + 48 Ca → 296 116 este prezentată în Fig. 12.13.

Orez. 12.13. Diagrama dezintegrarii nucleare 296 116.
Izotopul 296 116 se răcește ca urmare a emisiei a patru neutroni și se transformă în izotopul 292 116, care apoi, cu o probabilitate de 5%, în urma a două e-capturi consecutive, se transformă în izotopul 292 114. Ca rezultat a dezintegrarii α (T 1/2 = 85 zile ) izotopul 292 114 se transformă în izotopul 288 112. Formarea izotopului 288 112 are loc și prin canal
Nucleul final 288 112 rezultat din ambele lanțuri are un timp de înjumătățire de aproximativ 1 oră și se descompune prin fisiune spontană. Cu o probabilitate de aproximativ 10%, ca urmare a dezintegrarii α a izotopului 288 114, se poate forma izotopul 284 112. Perioadele și canalele de dezintegrare de mai sus au fost obținute prin calcul.
În fig. Figura 12.14 prezintă un lanț de dezintegrari α succesive ale izotopului 288115, măsurate în experimente din Dubna. ER este energia nucleului de recul implantat într-un detector de siliciu sensibil la poziție. Se poate observa o concordanță bună în timpul de înjumătățire și energiile dezintegrarilor α în cele trei experimente, ceea ce indică fiabilitatea metodei de identificare a elementelor supergrele folosind măsurători ale spectrelor particulelor α.

Orez. 12.14. Un lanț de dezintegrari α succesive ale izotopului 288115, măsurate în experimente din Dubna.
Cel mai greu element produs în laborator cu Z = 118 a fost sintetizat în reacție
48 Ca + 249 Cf → 294 118 + 3n.
La energiile ionice din apropierea barierei Coulomb au fost observate trei cazuri de formare a elementului 118. 294.118 nuclee au fost implantate într-un detector de siliciu și a fost observată un lanț de dezintegrari succesive α. Secțiunea transversală pentru formarea elementului 118 a fost de ~2 picobarns. Timpul de înjumătățire al izotopului 293118 este de 120 ms.
În fig. Figura 12.15 prezintă un lanț calculat teoretic de dezintegrari succesive α ale izotopului 293 118 și arată perioadele de înjumătățire ale nucleelor fiice formate ca urmare a descompunerilor α.

Orez. 12.15. Un lanț de dezintegrari α succesive ale izotopului 293 118.
Sunt date durata medie de viață a nucleelor fiice formate ca urmare a descompunerilor α.
La analizarea diferitelor posibilități de formare a elementelor supergrele în reacții cu ioni grei trebuie avute în vedere următoarele circumstanțe.
- Este necesar să se creeze un nucleu cu un raport suficient de mare dintre numărul de neutroni și numărul de protoni. Prin urmare, ionii grei cu un N/Z mare trebuie să fie aleși ca particule incidente.
- Este necesar ca nucleul compus rezultat să aibă o energie de excitație scăzută și un moment unghiular mic, deoarece altfel înălțimea efectivă a barierei de fisiune va scădea.
- Este necesar ca nucleul rezultat să aibă o formă apropiată de sferică, deoarece chiar și o deformare ușoară va duce la fisiunea rapidă a nucleului supergreu.
O metodă foarte promițătoare pentru producerea nucleelor supergrele sunt reacții precum 238 U + 238 U, 238 U + 248 Cm, 238 U + 249 Cf, 238 U + 254 Es. În fig. Figura 12.16 prezintă secțiunile transversale estimate pentru formarea elementelor transuraniu în timpul iradierii țintelor de 248 Cm, 249 Cf și 254 Es cu ioni accelerați de 238 U. În aceste reacții s-au obținut deja primele rezultate asupra secțiunilor transversale pentru formarea elementelor cu Z > 100. Pentru a crește randamentele reacțiilor studiate, grosimile țintă au fost alese în așa fel încât produsele de reacție să rămână în ținta. După iradiere, elementele chimice individuale au fost separate de țintă. Produșii de descompunere α și fragmentele de fisiune au fost înregistrate în probele obținute pe parcursul mai multor luni. Datele obținute folosind ioni de uraniu accelerați indică în mod clar o creștere a randamentului elementelor transuraniu grele în comparație cu ionii de bombardare mai ușori. Acest fapt este extrem de important pentru rezolvarea problemei fuziunii nucleelor supergrele. În ciuda dificultăților de a lucra cu ținte adecvate, previziunile pentru progresul către Z mare par destul de optimiste.

Orez. 12.16. Estimări ale secțiunilor transversale pentru formarea elementelor transuraniu în reacțiile de 238 U cu 248 Cm, 249 Cf și 254 Es
Progresele în domeniul nucleelor supergrele din ultimii ani au fost uimitor de impresionante. Cu toate acestea, toate încercările de a descoperi Insula Stabilității au fost până acum fără succes. Căutarea lui continuă intens.
Structura învelișului nucleelor atomice joacă un rol semnificativ în creșterea stabilității nucleelor supergrele. Numerele magice Z ≈ 114 și N ≈ 184, dacă există într-adevăr, pot duce la o creștere semnificativă a stabilității nucleelor atomice. De asemenea, este semnificativ faptul că dezintegrarea nucleelor supergrele va avea loc ca urmare a dezintegrarii α, care este importantă pentru dezvoltarea metodelor experimentale pentru detectarea și identificarea de noi nuclee supergrele.
„Era chimică” în chimioterapie a început odată cu dezvoltarea
industria prelucrătoare. Geniala analiza
Marx și Lenin ne arată cum a avut loc procesul
dezvoltarea capitalismului în industrie: de la simpla cooperare
munca prin manufactura (in secolele XVI-VII) industrie
la sfârșitul secolului al XVIII-lea și începutul secolului al XIX-lea a trecut la capitalist
fabrică, adică producția de mașini la scară largă.
Munca manuală a fost înlocuită cu munca la mașină.
Motoare cu abur, dezvoltarea transportului feroviar și pe apă
transport cu abur, filare mașină, metode noi
fontă și oțel - toate acestea au provocat o revoluție în industrie.
Era revoluției industriale a sosit.
Știința chimică abia putea ține pasul cu cerințele științei mecanice
industrie. În domeniul teoriei, această știință a făcut
un salt major înainte la mijlocul secolului al XVIII-lea.
Bazele chimiei științifice și ale termodinamicii au fost puse de noi
celebrul compatriot Lomonosov.
În 1748, într-o celebră scrisoare către matematicianul Euler, membru al Academiei Ruse de Științe, Lomonosov a formulat pentru prima dată
legea constanței materiei și a mișcării. L
aparține celui de-al doilea merit ca importanță: a promovat
ideea necesității de a studia problema atomului și
structura moleculară a materiei, deoarece
proprietățile tuturor corpurilor, natura lor chimică și fizică.
≪ ...Chimie”, a scris Lomonosov în Cuvântul său despre beneficiile chimiei,
Primul lider va fi în dezvăluirea interiorului
săli de trupuri, primele care au pătruns în ascunzătoarele interioare
corp, primul vă va permite să vă familiarizați cu părțile corpului și ≫ .
≪ Chimia își întinde mâinile larg în treburile umane
≫ - cu acest cuvânt a încheiat una dintre secțiunile acestuia
≪Cuvinte≫. ≪ Nașterea continuă și distrugerea corpurilor este suficientă
vorbește elocvent despre mișcarea unui corpuscul≫, scria
mort, mișcare în plante - vii și morți, în minerale
sau în anorganic, deci, în tot≫.
Mecanizarea producției de țesut a creat nevoia
revoluții în mecanica și chimia tipăririi și vopsirii calico
afaceri, prelucrarea metalelor, călirea lor necesară
intervenția profundă a elementelor chimice în proces
Fără îndoială, principalele realizări ale chimiei moderne
știința datorează trei chimiști ruși geniali - Nikolai
Lui Nikolaevici Zinin, Alexandru Mihailovici Butlerov I
Dmitri Ivanovici Mendeleev.
Profesor la Universitatea din Kazan N. N. Zinin în 1841
obtinut prin sinteza chimica dintr-un compus ciclic
nitrobenzen anilina este produsul de plecare din care
Prin prelucrare se obțin zeci de coloranți diferiți.
Înainte de aceasta, vopselele erau preparate din produse vegetale.
Zinin este considerat pe bună dreptate tatăl așa-zisului
chimie sintetică.
Dacă Zinin n-ar fi făcut altceva decât să se transforme
nitrobenzen în anilină, atunci numele lui ar fi fost inclus în
istoria științei ca nume al celui mai mare chimist. Sinteza anilinei
a deschis o nouă eră în industria chimică și medicinală.
Prin tratarea anilinei cu acid clorhidric, alcool metilic,
fosgen și alți reactivi, puteți obține foarte
un număr mare de coloranți pentru țesături. Peste două sute de coloranți
produs de industria chimică sovietică din
anilină incoloră. În producție se folosește anilina
filme, precum și dezvoltatori pentru filme color. Din anilină
produce o substanță care accelerează procesul de vulcanizare
cauciuc. Peste o sută de medicamente fabricate
în prezent, inclusiv streptocid și sulfonamide,
sunt derivați ai anilinei.
În secolul al XVIII-lea, mintea limpede a lui Lomonosov a prevăzut semnificația
chimie pentru medicină: ≪ Medic fără cunoștințe suficiente de chimie
nu poate fi perfect...≫ ; ≪ speranță numai din chimicale
posibilă corectarea deficienţelor ştiinţei medicale...≫ .
Succesorul lui Zinin, A.M. Butlerov, a făcut o revoluție în
doctrina structurii compușilor chimici organici.
Convins de realitatea atomilor, Butlerov a stabilit obiectivul
exprimă legăturile chimice dintre atomi în formule precise,
formând o moleculă dintr-un compus organic. Butlerov
credea că este posibil să se afle structura moleculelor folosind
metode fizice și prin transformări chimice.
Urmând această cale, și-a dezvoltat teoria chimică
structura compușilor organici. După experimente persistente
cu alcooli butilici Butlerov l-a stabilit pe acela şi
același număr de anumiți atomi (de exemplu, carbon,
hidrogen și oxigen), care sunt într-o conexiune în lanț,
poate produce diferite produse și care sunt proprietățile rezultatului
produsele chimice depind de ordinea în care vor fi
elementele sunt legate între ele. A crescut ca un număr
combinații posibile în sinteza de noi substanțe chimice,
și numărul de medicamente primite
prin sinteză chimică.
Cea mai mare descoperire a secolului al XIX-lea este legea periodică
Mendeleev - . a dus la instaurarea ordinii stricte şi
modele între elementele chimice. Măsura acestui lucru
greutatea atomică a devenit un model. Multe medicamente pentru chimioterapie
în trecut au fost descoperite întâmplător. Dar știința este dușmanul întâmplării.
Pe măsură ce cunoștințele științifice au progresat, multe lucruri păreau misterioase
și de neînțeles, a devenit clar și firesc.
Legea periodică a lui Mendeleev pune toate substanțele chimice
știință și, în special, chimioterapia pe o bază științifică solidă.
„Înainte de legea periodică”, a scris Mendeleev, „. simplu
corpurile reprezentau doar fenomene fragmentare, aleatorii
natura: nu era niciun motiv să ne așteptăm la altele noi, dar din nou
găsite în proprietățile lor au fost o noutate complet neașteptată.
Legalitatea periodică a fost prima care a făcut-o posibil
pentru a vedea elemente care nu au fost încă descoperite la o asemenea distanță încât să nu fie posibil
viziune chimică înarmată cu acest tipar până când
porii nu au ajuns și, în același timp, elemente noi, descoperite anterior,
au fost desenate cu o serie întreagă de proprietăți≫ 1.
Nu e de mirare că Engels a caracterizat previziunea științifică
Mendeleev ca faptă științifică. A fost cu adevărat extraordinar
o victorie pentru știința fenomenelor chimice, o victorie care a permis
umanitatea să urmeze o cale durabilă de eliberare
din puterea întâmplării și subjugarea forțelor naturii. Periodic
Sistemul periodic a făcut posibilă găsirea unui întreg
un grup de elemente chimice apropiate unele de altele, utile
pentru tratamentul multor boli (arsen, mercur, antimoniu).
Aceste elemente au apărut oamenilor de știință la sfârșitul secolului al XIX-lea ca
ar fi o mină de aur. În același timp, oamenii de știință au folosit pe deplin
Principiul Zinin al sintezei chimice și combinațiile lui Butlerov
în aranjarea atomilor şi moleculelor.
Printre oamenii de știință medicali implicați în producția de materiale sintetice
droguri, cel mai mare succes i-a revenit lui Ehrlich.
Întreaga viață a lui Ehrlich a fost dedicată implementării persistente
o idee - obținută prin compus chimic
fără a dăuna organismului.
Este important de subliniat că această idee a fost exprimată în 1891
fondatorul chimioterapiei D. L. Romanovsky. El a scris,
ceea ce el consideră un medicament ideal ≪ o substanţă care
injectarea într-un corp bolnav va cauza cel mai mic rău
acesta din urmă și va provoca cea mai mare schimbare distructivă în
agent dăunător≫. Romanovsky a anticipat ideea lui Early
ha despre „gloanțele magice” care lovesc cu ușurință inamicii. Romanovsky
a fost primul care a stabilit, pe baza unor observații exacte,
cea mai importantă lege a chimioterapiei este mecanismul direct de acţiune
medicina chimică împotriva agentului cauzal al bolii.
≪ Chinină, atunci când este introdusă în corpul unui pacient cu malarie în mod suficient
modificări distructive ușor de observat, în principal
imagine - nucleul său, de ce acest remediu ar trebui considerat adevărat
medicament specific împotriva malariei≫.
se reflectă specificul acestui remediu pentru malarie - adevărata specificitate a acțiunii asupra însăși esenței bolii,
Romanovski a fost primul care a pus problema ≪ acțiunii radicale
≫ medicamente pentru chimioterapie pentru agenți patogeni sau, după cum a spus el,
boala ≪ producătorilor≫. Deci el a fost inițiatorul
idei pentru o terapie de sterilizare excelentă.
Dacă chinina există în natură, motivat după
pentru corpul uman, atunci trebuie să fie și altele
substanțe similare care pot fi folosite pentru a învinge alte boli.
La sfârșitul secolului al XIX-lea, știința chimică și-a continuat
procesiune triumfală începută de Lomonosov și încheiată
Zinin, Butlerov și Mendeleev.
Reviste au fost pline de noi și interesante
relatări despre cucerirea chimiei.
Totuși, de unde să încep? Care substanță din sutele deja obținute
chimic poate fi folosit pentru sinteza
chimioterapie?
În timp ce era încă student, Ehrlich a repetat experimentul binecunoscut
Profesorul de la Kiev Geibel, care a dovedit că atunci când
În caz de otrăvire cu plumb, acest metal este distribuit neuniform
în organism: în unele organe plumbul se acumulează în vizibil
cantități, dar nu poate fi detectat într-un cadavru nici măcar cu cele mai fine
reactivi. Aceasta înseamnă că substanțele chimice au
acţiune selectivă, a decis Ehrlich.
Cu toate acestea, Ehrlich a abandonat experimentele cu plumb, deoarece
În ochi, celulele otrăvite nu erau diferite de cele sănătoase.
S-a hotărât pe vopsea albastră de metilen pentru că
va fi mai convenabil pentru observație și a sugerat tratarea malariei
albastru de metil. Acest tratament a dat unele rezultate.
Ehrlich a fost încurajat de ei și a început să-și extindă experimentele.
frunză îngustă cu coadă și evocatoare de cai
șoareci și le-a provocat o boală fatală.
Erlich s-a așezat în laborator și a început să verifice vopselele
soareci infectati. Acesta a fost probabil o modalitate simplificată,
dar aceștia au fost primii pași ai chimioterapiei științifice. Dificil
stabiliți imediat ce vopsea are în condiții animale
O vopsea a făcut șoarecii chenilie, alta i-a făcut galbeni și
tripanozomii cu coadă pluteau încă în fluxul sanguin
soareci si i-a ucis. Nu a ieșit nimic cu vopselele.
În știința naturii se nasc „granule de aur ale adevărului”.
de la ≪ mii de tone de minereu prelucrat≫. Trebuie doar să-l deschizi
orice remediu, și apoi chimistul îl va dezmembra, adaugă
acid sau alcalin, combinați cu reactivi, determinați atomic
greutate, îl va testa pe animale bolnave și apoi pe oameni...
Și apoi în tabelul medicamentelor de chimioterapie terapeutică apare
un nou remediu salvator.
A fost greu să treci la chimioterapie rațională.
A fost necesar să se caute o busolă care să conducă la corect
cale. A trebuit să căutăm modele...
Și apoi, într-o zi, stând în biroul lui, Erlich a citit
ultimul număr al unui jurnal de chimie despre un nou patentat
mijloace. A fost numit „atoxil”, ceea ce înseamnă netoxic.
Testarea acestui medicament a început pe șoareci infectați cu
tripanozomi.
După sute de experimente s-a putut observa că atoxil
chiar vindecă șoarecii.
Dar unii șoareci tot au murit. Prin urmare, nu
Deci atoxilul este deja inofensiv.
Ehrlich a decis să-l facă inofensiv. Acest produs a meritat
pentru a lucra la el.
Atoxil conține același inel benzenic ca
si in unele culori.
Un inel benzenic este format din șase atomi de carbon legați între ei.
într-un singur cerc. Dar i s-a adăugat oxid de arsenic.
Acest lucru, evident, a făcut ca medicamentul să se vindece. Arsenic - cunoscut
otravă, dar atunci când este combinată cu un inel de benzen
S-a dovedit a fi un medicament pentru chimioterapie.
Cu toate acestea, a fost necesar să „înnobilăm” mai mult această otravă, întorcându-se
într-un mod chiar mai sigur și în același timp puternic
remediu împotriva agenților patogeni.
atoxil, ei au spus că este imposibil să schimbi atoxil, este chiar acolo
se va destrama. Cu toate acestea, Ehrlich a reușit să modifice acest medicament
în sute de preparate cu arsenic, fără a deranja
combinații de benzen și arsenic.
A lucrat în laboratorul său timp de doi ani până când el
a descoperit un remediu care curăța complet sângele
soareci de la tripanozomii feroce care i-au ucis. In acelasi timp nou
Produsul s-a dovedit a fi inofensiv pentru șoareci. Au tolerat-o bine
≪ 606≫ sau salvarsan, acesta era numele noului medicament,
căci el era cea de-a 606-a variantă de atoxil. Acest drog a fost
un produs al celei mai bune sinteze chimice și prepararea acestuia
a fost asociat cu pericolul de explozie și incendiu din cauza
un număr mare de compuși care participă la reacție
vapori eterici.
Și cel mai important, a fost posibil să se stabilească că medicamentul este necesar
depozitați într-o fiolă fără aer - amestecul de aer face
este otrăvitoare.
Acesta a fost medicamentul, care purta numele chimic: dioc-
Si-diamino-arsenobenzen-diclorhidrat.
Dar apoi a avut loc un eveniment semnificativ.
Cu puțin timp înainte de cercetarea lui Ehrlich, celebrul om de știință Shaw.
Dean a descoperit agentul cauzal al sifilisului, spirochete pallidum, care apare
din familia tripanozomilor.
Dar, se gândi Erlich, nu te poți opri la cai
tripanozomi, este necesar să se influențeze spirocheta,
care afectează o persoană.
Cu toate acestea, nu a trecut imediat la oameni; s-a infectat cu sifilis
iepuri și apoi i-a tratat cu medicamentul ≪ 606≫. După
mai multe infuzii au lăsat iepurii fără nici una
spirochetele. Dozele de medicament au fost dezvoltate și la iepuri.
Ehrlich a produs încă 308 compuși și a obținut un compuși mai perfect
medicament -≪ 914≫ (neosalvarsan). Acest medicament
dizolvat în 5 centimetri cubi de apă. Introducerea lui
în corp s-a dovedit a fi și mai sigur: au existat reacții
Medicamentele au păstrat încă unele proprietăți toxice.
La unii pacienți, mai ales când se administrează doze mari,
medicamentele ≪ 606≫ și ≪ 914≫ au provocat inflamație a creierului, pierderea
conștiență, febră, hemoragii cutanate.
Dușmanii lui Ehrlich au făcut tam-tam în legătură cu noile medicamente.
I-au cauzat lui Erlich multe necazuri.
Când medicamentele lui Ehrlich au fost testate în număr mare
pacienților, s-a dovedit că au un efect toxic
rareori.
Întreaga lume a recunoscut importanța enormă a noilor instrumente.
Sifilisul a încetat să mai fie o boală teribilă. Tratamentul a dat
rezultate excelente; ulcerele bolnavilor au dispărut după
mai multe infuzii.
Ehrlich a decis să elimine spirocheta febrei recidivante,
înrudit cu spirocheta sifilitică.
În acest moment, în unele orașe din Rusia au fost observate
focare de febră recurentă. Medici ruși Yu. Yu. Iversen în
Petersburg și P.K. Galler din Saratov au luat o decizie îndrăzneață
iar primul din lume a pus la cale un test amplu al noului
medicament pentru pacienții cu febră recurentă.
Efectul tratamentului a fost uimitor: după pacient
la o temperatură de 40° s-a turnat jumătate de gram de Ehrlich
medicament, după 14-6 ore a început transpirația cea mai puternică și
temperatura a scăzut complet. Pacientul și-a revenit complet.
Corpul lui a fost complet eliberat de spirochete.
Nu este aceasta împlinirea viselor oamenilor de știință de o mare sterilizare
După câțiva ani de utilizare a salvarsanului, oamenii de știință ruși
constatat ca dupa infuzii salvarsane exista
doar reacții minore, dar apar complicații fatale
extrem de rar (un deces la 100.000 de perfuzii).
Îmbunătățirea calității medicamentului, stabilirea corectă
doze si contraindicatii exacte, scris in 1916-917
ani, oamenii de știință G.I. Meshchersky, S.L. Bogrov și V.V. Iva.
nou - va duce la faptul că acest remediu va fi complet
sigur.
Cercetători și medici avansați în chimie ruși vor fi în curând
după descoperirea lui Ehrlich, ei și-au pus sarcina de a face
salvarsan domestic.
Chimistul V. A. Smirnov în laboratorul farmaceutic al lui V. K. Ferein
Deja în 1914, un medicament bun, netoxic de acest tip
salvarsana. Singurul său dezavantaj a fost puțin redus
șoareci produși de Ya. G. Shereshevsky, S. L. Bogrov,
S. S. Usoltsev et al., un nou medicament, care a fost numit ≪ ben-
Zarsan≫ a început să fie utilizat în clinici pentru tratarea pacienților. Profesor
T. P. Pavlov, G. I. Meshchersky și V. V. Ivanov într-o serie de articole publicate
în 1916-917 în „Doctor rus”, „Ziar medical” și
≪Revista Rusă de Boli de piele și venerice≫, au oferit informații despre primul
salvarsana excelenta recenzie.
Ulterior, din 1916, s-a organizat producția de fabrică de masă
producție de salvarsan rusesc. Această producție a fost condusă de celebrii
Chimistul rus P.F. Ryumshin, care a dezvoltat originalul general acceptat
tehnologie pentru sinteza salvarsanului.
Concomitent cu Smirnov, salvarsanul rus (sub numele ≪ ar-
Ol≫) au fost sintetizate în 1914 de chimiștii moscovi I. I. Ostromyslen-
skiy și S.S. Kelbasinsky.
În 1915, în „Jurnalul rus al bolilor de piele și venerice”
a existat o recenzie foarte favorabilă a lui Bogrov și Meshchersky despre aceasta
medicament.
După Marea Revoluție Socialistă din Octombrie, a fost înființată
producția de salvarsan rusesc (novarsalan, novarsol) în fabrică



