Условие равновесия. Константа равновесия. Константы равновесия Kр, Кс и Кх связаны между собой соотношением Расчёт константы равновесия методами статистической термодинамики
Химическим равновесием называется такое состояние обратимой химической реакции
aA + b B = c C + d D,
при котором с течением времени не происходит изменения концентраций реагирующих веществ в реакционной смеси. Состояние химического равновесия характеризуется константой химического равновесия :
где C i – концентрации компонентов в равновесной идеальной смеси.
Константа равновесия может быть выражена также через равновесные мольные доли X i компонентов:
Для реакций, протекающих в газовой фазе, константу равновесия удобно выражать через равновесные парциальные давления P i компонентов:
Для идеальных газов P i = C i RT и P i = X i P , где P – общее давление, поэтому K P , K C и K X связаны следующим соотношением:
K P = K C (RT) c+d–a–b = K X P c+d–a–b . (9.4)
Константа равновесия связана с r G o химической реакции:
![]() (9.5)
(9.5)
![]() (9.6)
(9.6)
Изменение r G или r F в химической реакции при заданных (не обязательно равновесных) парциальных давлениях P i или концентрациях C i компонентов можно рассчитать по уравнению изотермы химической реакции (изотермы Вант-Гоффа ):
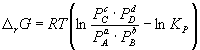 . (9.7)
. (9.7)
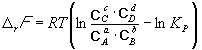 . (9.8)
. (9.8)
Согласно принципу Ле Шателье , если на систему, находящуюся в равновесии, оказать внешнее воздействие, то равновесие сместится так, чтобы уменьшить эффект внешнего воздействия. Так, повышение давления сдвигает равновесие в сторону уменьшения количества молекул газа. Добавление в равновесную смесь какого-либо компонента реакции сдвигает равновесие в сторону уменьшения количества этого компонента. Повышение (или понижение) температуры сдвигает равновесие в сторону реакции, протекающей с поглощением (выделением) теплоты.
Количественно зависимость константы равновесия от температуры описывается уравнением изобары химической реакции (изобары Вант-Гоффа )
![]() (9.9)
(9.9)
и изохоры химической реакции (изохоры Вант-Гоффа )
![]() . (9.10)
. (9.10)
Интегрирование уравнения (9.9) в предположении, что r H реакции не зависит от температуры (что справедливо в узких интервалах температур), дает:
![]() (9.11)
(9.11)
![]() (9.12)
(9.12)
где C – константа интегрирования. Таким образом, зависимость ln K P от 1/Т должна быть линейной, а наклон прямой равен – r H /R .
Интегрирование в пределах K 1 , K 2 , и T 1, T 2 дает:
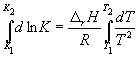 (9.13)
(9.13)
 (9.14)
(9.14)
По этому уравнению, зная константы равновесия при двух разных температурах, можно рассчитать r H реакции. Соответственно, зная r H реакции и константу равновесия при одной температуре, можно рассчитать константу равновесия при другой температуре.
ПРИМЕРЫ
CO(г) + 2H 2 (г) = CH 3 OH(г)
при 500 K. f G o для CO(г) и CH 3 OH(г) при 500 К равны –155.41 кДж. моль –1 и –134.20 кДж. моль –1 соответственно.
Решение. G o реакции:
r G o = f G o (CH 3 OH) – f G o (CO) = –134.20 – (–155.41) = 21.21 кДж. моль –1 .
![]() = 6.09 10 –3 .
= 6.09 10 –3 .
Пример 9-2. Константа равновесия реакции
равна K P = 1.64 10 –4 при 400 o C. Какое общее давление необходимо приложить к эквимолярной смеси N 2 и H 2 , чтобы 10% N 2 превратилось в NH 3 ? Газы считать идеальными.
Решение. Пусть прореагировало моль N 2 . Тогда
| N 2 (г) | + | 3H 2 (г) | = | 2NH 3 (г) | |
| Исходное количество | 1 | 1 | |||
| Равновесное количество | 1– | 1–3 | 2 (Всего: 2–2) | ||
| Равновесная мольная доля: |
Следовательно, K
X = 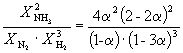 и K P = K X . P
–2
=
и K P = K X . P
–2
= 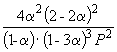 .
.
Подставляя = 0.1 в полученную формулу, имеем
1.64 10 –4 = , откуда P
= 51.2 атм.
, откуда P
= 51.2 атм.
Пример 9-3. Константа равновесия реакции
CO(г) + 2H 2 (г) = CH 3 OH(г)
при 500 K равна K P = 6.09 10 –3 . Реакционная смесь, состоящая из 1 моль CO, 2 моль H 2 и 1 моль инертного газа (N 2) нагрета до 500 K и общего давления 100 атм. Рассчитать состав равновесной смеси.
Решение. Пусть прореагировало моль CO. Тогда
| CO(г) | + | 2H 2 (г) | = | CH 3 OH(г) | |
| Исходное количество: | 1 | 2 | 0 | ||
| Равновесное количество: | 1– | 2–2 | |||
| Всего в равновесной смеси: | 3–2 моль компонентов + 1 моль N 2 = 4–2 моль | ||||
| Равновесная мольная доля | |||||
Следовательно, K
X = 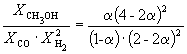 и K P = K X . P –2
=
и K P = K X . P –2
= ![]() .
.
Таким образом, 6.09 10 –3
= ![]() .
.
Решая это уравнение, получаем = 0.732. Соответственно, мольные доли веществ в равновесной смеси равны: = 0.288, = 0.106, = 0.212 и = 0.394.
Пример 9-4. Для реакции
N 2 (г) + 3H 2 (г) = 2NH 3 (г)
при 298 К K P = 6.0 10 5 , а f H o (NH 3) = –46.1 кДж. моль –1 . Оценить значение константы равновесия при 500 К.
Решение. Стандартная мольная энтальпия реакции равна
r H o = 2 f H o (NH 3) = –92.2 кДж. моль –1 .
Согласно уравнению (9.14), 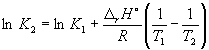 =
=
Ln (6.0 10 5) + ![]() = –1.73, откуда K
2 =
0.18.
= –1.73, откуда K
2 =
0.18.
Отметим, что константа равновесия экзотермической реакции уменьшается с ростом температуры, что соответствует принципу Ле Шателье.
ЗАДАЧИ
- При 1273 К и общем давлении 30 атм в равновесной смеси
- При 2000 o C и общем давлении 1 атм 2% воды диссоциировано на водород и кислород. Рассчитать константу равновесия реакции
- Константа равновесия реакции
- Константа равновесия реакции
- Сосуд объемом 3 л, содержащий 1.79 10 –2 моль I 2 , нагрели до 973 K. Давление в сосуде при равновесии оказалось равно 0.49 атм. Считая газы идеальными, рассчитать константу равновесия при 973 K для реакции
- Для реакции
- Для реакции
- Сосуд объемом 1 л, содержащий 0.341 моль PCl 5 и 0.233 моль N 2 , нагрели до 250 o C. Общее давление в сосуде при равновесии оказалось равно 29.33 атм. Считая все газы идеальными, рассчитать константу равновесия при 250 o C для протекающей в сосуде реакции
- Константа равновесия реакции
- При 25 o C f G o (NH 3) = –16.5 кДж. моль –1 . Рассчитать r G реакции образования NH 3 при парциальных давлениях N 2 , H 2 и NH 3 , равных 3 атм, 1 атм и 4 атм соответственно. В какую сторону реакция будет идти самопроизвольно при этих условиях?
- Экзотермическая реакция
- Константа равновесия газофазной реакции изомеризации борнеола (C 10 H 17 OH) в изоборнеол равна 0.106 при 503 K. Смесь 7.5 г борнеола и 14.0 г изоборнеола поместили в сосуд объемом 5 л и выдерживали при 503 K до достижения равновесия. Рассчитать мольные доли и массы борнеола и изоборнеола в равновесной смеси.
- Равновесие в реакции
- Рассчитать общее давление, которое необходимо приложить к смеси 3 частей H 2 и 1 части N 2 , чтобы получить равновесную смесь, содержащую 10% NH 3 по объему при 400 o C. Константа равновесия для реакции
- При 250 o C и общем давлении 1 атм PCl 5 диссоциирован на 80% по реакции
- При 2000 o C для реакции
- Рассчитать стандартную энтальпию реакции, для
которой константа равновесия
а) увеличивается в 2 раза, б) уменьшается в 2 раза при изменении температуры от 298 К до 308 К. - Зависимость константы равновесия реакции 2C 3 H 6 (г) = C 2 H 4 (г) + C 4 H 8 (г) от температуры между 300 К и 600 К описывается уравнением
CO 2 (г) + C(тв) = 2CO(г)
содержится 17% (по объему) CO 2 . Сколько процентов CO 2 будет содержаться в газе при общем давлении 20 атм? При каком давлении в газе будет содержаться 25% CO 2 ?
H 2 O(г) = H 2 (г) + 1/2O 2 (г) при этих условиях.
CO(г) + H 2 O(г) = CO 2 (г) + H 2 (г)
при 500 o C равна K p = 5.5. Смесь, состоящая из 1 моль CO и 5 моль H 2 O, нагрели до этой температуры. Рассчитать мольную долю H 2 O в равновесной смеси.
N 2 O 4 (г) = 2NO 2 (г)
при 25 o C равна K p = 0.143. Рассчитать давление, которое установится в сосуде объемом 1 л, в который поместили 1 г N 2 O 4 при этой температуре.
I 2 (г) = 2I (г).
при 250 o C r G o = –2508 Дж. моль –1 . При каком общем давлении степень превращения PCl 5 в PCl 3 и Cl 2 при 250 o C составит 30%?
2HI(г) = H 2 (г) + I 2 (г)
константа равновесия K P = 1.83 10 –2 при 698.6 К. Сколько граммов HI образуется при нагревании до этой температуры 10 г I 2 и 0.2 г H 2 в трехлитровом сосуде? Чему равны парциальные давления H 2 , I 2 и HI?
PCl 5 (г) = PCl 3 (г) + Cl 2 (г)
CO(г) + 2H 2 (г) = CH 3 OH(г)
при 500 K равна K P = 6.09 10 –3 . Рассчитать общее давление, необходимое для получения метанола с 90% выходом, если CO и H 2 взяты в соотношении 1: 2.
CO(г) + 2H 2 (г) = CH 3 OH(г)
находится в равновесии при 500 K и 10 бар. Если газы идеальные, как повлияют на выход метанола следующие факторы: а) повышение T ; б) повышение P ; в) добавление инертного газа при V = const; г) добавление инертного газа при P = const; д) добавление H 2 при P = const?
2NOCl(г) = 2NO(г) + Cl 2 (г)
устанавливается при 227 o C и общем давлении 1.0 бар, когда парциальное давление NOCl равно 0.64 бар (изначально присутствовал только NOCl). Рассчитать r G o для реакции. При каком общем давлении парциальное давление Cl 2 будет равно 0.10 бар?
N 2 (г) + 3H 2 (г) = 2NH 3 (г)
при 400 o C равна K = 1.60 10 –4 .
PCl 5 (г) = PCl 3 (г) + Cl 2 (г).
Чему будет равна степень диссоциации PCl 5 , если в систему добавить N 2 , чтобы парциальное давление азота было равно 0.9 атм? Общее давление поддерживается равным 1 атм.
N 2 (г) + O 2 (г) = 2NO(г)
K p = 2.5 10 –3 . В равновесной смеси N 2 , O 2 , NO и инертного газа при общем давлении 1 бар содержится 80% (по объему) N 2 и 16% O 2 . Сколько процентов по объему составляет NO? Чему равно парциальное давление инертного газа?
ln K = –1.04 –1088 /T +1.51 10 5 /T 2 .
Константа равновесия
Конста́нта равнове́сия - величина, определяющая для данной химической реакции соотношение между термодинамическими активностями (либо, в зависимости от условий протекания реакции, парциальными давлениями , концентрациями или фугитивностями) исходных веществ и продуктов в состоянии химического равновесия (в соответствии с законом действующих масс). Зная константу равновесия реакции, можно рассчитать равновесный состав реагирующей смеси, предельный выход продуктов, определить направление протекания реакции.
Способы выражения константы равновесия
Например, для реакции окисления монооксида углерода :
2CO + O 2 = 2CO 2
константа равновесия может быть рассчитана по уравнению:
где Δn - изменение числа молей веществ в ходе реакции. Видно, что K x зависит от давления. Если число молей продуктов реакции равно числу молей исходных веществ (), то .
Стандартная константа равновесия
Стандартная константа равновесия реакции в смеси идеальных газов (когда начальные парциальные давления участников реакции равны их значениям в стандартном состоянии = 0,1013 МПа или 1 атм) может быть рассчитана по выражению:
где - относительные парциальные давления компонентов, .Стандартная константа равновесия - безразмерная величина. Она связана с K p соотношением:
Видно, что если выражены в атмосферах, то и .
Для реакции в смеси реальных газов в стандартном начальном состоянии парциальные фугитивности газов принимаются равными их парциальным давлениям = 0,1013 МПа или 1 атм. K f связана с K 0 соотношением:
где γ i - коэффициент фугитивности i-го реального газа в смеси.Константа равновесия реакций в гетерогенных системах
FeO т + CO г = Fe т + CO 2гконстанта равновесия (при условии, что газовая фаза идеальна) имеет вид:
Константа равновесия и изменение энергии Гиббса
Константа равновесия и константа скорости реакции
Для обратимой химической реакции константа равновесия может быть выражена через константы скорости прямых и обратных реакций, исходя из того факта, что в состоянии равновесия скорости прямой и обратной реакций равны. Например, для элементарной обратимой химической реакции первого порядка
где k 1 - константа скорости прямой реакции, а k 2 - обратной. Это важное соотношение даёт одну из «точек соприкосновения» химической кинетики и химической термодинамики.Методы расчета константы равновесия
Расчётные методы определения константы равновесия реакции обычно сводятся к вычислению тем или иным способом стандартного изменения энергии Гиббса в ходе реакции (ΔG 0 ), а затем использованию формулы:
, где - универсальная газовая постоянная .При этом следует помнить, что энергия Гиббса - функция состояния системы, то есть она не зависит от пути процесса, от механизма реакции, а определяется лишь начальным и конечным состояниями системы. Следовательно, если непосредственное определение или расчёт ΔG 0 для некоторой реакции по каким-либо причинам затруднены, можно подобрать такие промежуточные реакции, для которых ΔG 0 известно или может быть легко определено, и суммирование которых даст рассматриваемую реакцию (см. Закон Гесса). В частности, в качестве таких промежуточных реакций часто используют реакции образования соединений из элементов.
Энтропийный расчёт изменения энергии Гиббса и константы равновесия реакции
Энтропийный метод расчёта ΔG реакции является одним из самых распространённых и удобных . Он основан на соотношении:
или, соответственно, для стандартного изменения энергии Гиббса:
Здесь ΔH 0 при постоянных давлении и температуре равно тепловому эффекту реакции, методы расчёта и экспериментального определения которого известны - см., например, уравнение Кирхгофа :
Необходимо получить изменение энтропии в ходе реакции. Эта задача может быть решена несколькими способами, например:
- По термическим данным - с опорой на тепловую теорему Нернста и с использованием сведений о температурной зависимости теплоёмкости участников реакции. Например, для веществ, при нормальных условиях находящихся в твёрдом состоянии:
Итак, если извеcтны , и температурные зависимости теплоёмкости, может быть рассчитано по формуле:
Несколько упрощённый вариант этой формулы получают, считая сумму теплоёмкостей веществ не зависящей от температуры и равной сумме теплоёмкостей при 298 K:
И еще более упрощённый расчёт проводят, приравнивая сумму теплоёмкостей к нулю:
Переход от к константе равновесия осуществляется по приведённой выше формуле.
Расчёт константы равновесия методами статистической термодинамики
| Этот раздел статьи ещё не написан. |
Большинство химических реакций обратимы, т.е. протекают одновременно в противоположных направлениях. В тех случаях, когда прямая и обратная реакции идут с одинаковой скоростью, наступает химическое равновесие. Например, в обратимой гомогенной реакции: H 2 (г) + I 2 (г) ↔ 2HI(г) соотношение скоростей прямой и обратной реакций согласно закону действующих масс зависит от соотношения концентраций реагирующих веществ, а именно: скорость прямой реакции: υ 1 = k 1 [Н 2 ]. Скорость обратной реакции: υ 2 = k 2 2 .
Если H 2 и I 2 – исходные вещества, то в первый момент скорость прямой реакции определяется их начальными концентрациями, а скорость обратной реакции равна нулю. По мере израсходования H 2 и I 2 и образования HI скорость прямой реакции уменьшается, а скорость обратной реакции возрастает. Спустя некоторое время обе скорости уравниваются, и в системе устанавливается химическое равновесие, т.е. число образующихся и расходуемых молекул HI в единицу времени становится одинаковым.
Так как при химическом равновесии скорости прямой и обратной реакций равны V 1 = V 2 , то k 1 = k 2 2 .
Поскольку k 1 и k 2 при данной температуре постоянны, то их отношение будет постоянным. Обозначая его через K, получим:

К – называется константой химического равновесия, а приведенное уравнение – законом действующих масс (Гульдберга - Ваале).
В общем случае для реакции вида аА+bB+…↔dD+eE+… константа равновесия равна ![]() . Для взаимодействия между газообразными веществами часто пользуются выражением , в котором реагенты представлены равновесными парциальными давлениями p. Для упомянутой реакции
. Для взаимодействия между газообразными веществами часто пользуются выражением , в котором реагенты представлены равновесными парциальными давлениями p. Для упомянутой реакции  .
.
Состояние равновесия характеризует тот предел, до которого в данных условиях реакция протекает самопроизвольно (∆G<0). Если в системе наступило химическое равновесие, то дальнейшее изменение изобарного потенциала происходить не будет, т.е. ∆G=0.
Соотношение между равновесными концентрациями не зависит от того, какие вещества берутся в качестве исходных (например, H 2 и I 2 или HI), т.е. к состоянию равновесия можно подойти с обеих сторон.
Константа химического равновесия зависит от природы реагентов и от температуры; от давления (если оно слишком высокое) и от концентрации реагентов константа равновесия не зависит.
Влияние на константу равновесия температуры, энтальпийного и энтропийного факторов . Константа равновесия связана с изменением стандартного изобарно-изотермического потенциала химической реакции ∆G o простым уравнением ∆G o =-RT ln K.
Из него видно, что большим отрицательным значениям ∆G o (∆G o <<0) отвечают большие значения К, т.е. в равновесной смеси преобладают продукты взаимодействия. Если же ∆G o характеризуется большими положительными значениями (∆G o >>0), то в равновесной смеси преобладают исходные вещества. Указанное уравнение позволяет по величине ∆G o вычислить К, а затем и равновесные концентрации (парциальные давления) реагентов. Если учесть, что ∆G o =∆Н o -Т∆S o , то после некоторого преобразования получим ![]() . Из этого уравнения видно, что константа равновесия очень чувствительна к изменению температуры. Влияние на константу равновесия природы реагентов определяет ее зависимость от энтальпийного и энтропийного факторов.
. Из этого уравнения видно, что константа равновесия очень чувствительна к изменению температуры. Влияние на константу равновесия природы реагентов определяет ее зависимость от энтальпийного и энтропийного факторов.
Принцип Ле Шателье
Состояние химического равновесия сохраняется при данных неизменных условиях любое время. При изменении же условий состояние равновесия нарушается, так как при этом скорости противоположных процессов изменяются в разной степени. Однако спустя некоторое время система снова приходит в состояние равновесия, но уже отвечающее новым изменившимся условиям.
Смещение равновесия в зависимости от изменения условий в общем виде определяется принципом Ле-Шателье (или принципом подвижного равновесия): если на систему, находящуюся в равновесии, оказывать воздействие извне путем изменения какого-либо из условий, определяющих положение равновесия, то оно смещается в направлении того процесса, протекание которого ослабляет эффект произведенного воздействия.
Так, повышение температуры вызывает смещение равновесия в направлении того из процессов, течение которого сопровождается поглощением тепла, а понижение температуры действует в противоположном направлении. Подобно этому повышение давления смещает равновесие в направлении процесса, сопровождающегося уменьшением объема, а понижение давления действует в противоположную сторону. Например, в равновесной системе 3Н 2 +N 2 2H 3 N, ∆H o = -46,2 кДж повышение температуры усиливает разложение H 3 N на водород и азот, так как этот процесс эндотермический. Повышение давления смещает равновесие в сторону образования H 3 N, ибо при этом уменьшается объем.
Если в систему, находящуюся в состоянии равновесия, добавить некоторое количество какого-либо из веществ, участвующих в реакции (или наоборот, удалить из системы), то скорости прямой и обратной реакций изменяются, но постепенно снова уравниваются. Иными словами, система снова приходит к состоянию химического равновесия. В этом новом состоянии равновесные концентрации всех веществ, присутствующих в системе, будут отличаться от первоначальных равновесных концентраций, но соотношение между ними останется прежним. Таким образом, в системе, находящейся в состоянии равновесия, нельзя изменить концентрацию одного из веществ, не вызвав изменения концентраций всех остальных.
В соответствии с принципом Ле Шателье введение в равновесную систему дополнительных количеств какого-либо реагента вызывает сдвиг равновесия в том направлении, при котором концентрация этого вещества уменьшается и соответственно увеличивается концентрация продуктов его взаимодействия.
Изучение химического равновесия имеет большое значение как для теоретических исследований, так и для решения практических задач. Определяя положение равновесия для различных температур и давлений, можно выбрать наиболее благоприятные условия проведения химического процесса. При окончательном выборе условий проведения процесса учитывают также их влияние на скорость процесса.
Пример 1. Вычисление константы равновесия реакции по равновесным концентрациям реагирующих веществ.
Вычислите константу равновесия реакции А+В 2С, если равновесные концентрации [А]=0,3моль∙л -1 ; [В]=1,1моль∙л -1 ; [С]=2,1моль∙л -1 .
Решение. Выражение константы равновесия для данной реакции имеет вид: . Подставим сюда указанные в условии задачи равновесные концентрации: =5,79.
Пример 2 . Вычисление равновесных концентраций реагирующих веществ. Реакция протекает по уравнению А+2В С.
Определите равновесные концентрации реагирующих веществ, если исходные концентрации веществ А и В соответственно равны 0,5 и 0,7 моль∙л -1 , а константа равновесия реакции К р =50.
Решение. На каждый моль веществ А и В образуется 2 моль вещества С. Если понижение концентрации веществ А и В обозначить через Х моль, то увеличение концентрации вещества будет равно 2Х моль. Равновесные концентрации реагирующих веществ будут:
С А =(о,5-х)моль∙л -1 ; С В =(0,7-х)моль∙л -1 ; С С =2х моль∙л -1
х 1 =0,86; х 2 =0,44
По условию задачи справедливо значение х 2 . Отсюда равновесные концентрации реагирующих веществ равны:
С А =0,5-0,44=0,06моль∙л -1 ; С В =0,7-0,44=0,26моль∙л -1 ; С С =0,44∙2=0,88моль∙л -1 .
Пример 3. Определение изменения энергии Гиббса ∆G o реакции по значению константы равновесия К р. Рассчитайте энергию Гиббса и определите возможность протекания реакции СО+Cl 2 =COCl 2 при 700К, если константа равновесия равна Кр=1,0685∙10 -4 . Парциальное давление всех реагирующих веществ одинаково и равно 101325Па.
Решение.
∆G 700 =2,303∙RT ![]() .
.
Для данного процесса:
Так как ∆Gо<0, то реакция СО+Cl 2 COCl 2 при 700К возможна.
Пример 4 . Смещение химического равновесия. В каком направлении сместится равновесие в системе N 2 +3H 2 2NH 3 -22ккал:
а) при увеличении концентрации N 2 ;
б) при увеличении концентрации Н 2 ;
в) при повышении температуры;
г)при уменьшении давления?
Решение. Увеличение концентрации веществ, стоящих в левой части уравнения реакции, по правилу Ле-Шателье должно вызвать процесс, стремящийся ослабить оказанное воздействие, привести к уменьшению концентраций, т.е. равновесие сместится вправо (случаи а и б).
Реакция синтеза аммиака – экзотермическая. Повышение температуры вызывает смещение равновесия влево – в сторону эндотермической реакции, ослабляющей оказанное воздействие (случай в).
Уменьшение давления (случай г) будет благоприятствовать реакции, ведущей к увеличению объема системы, т.е. в сторону образования N 2 и Н 2 .
Пример 5. Во сколько раз изменится скорость прямой и обратной реакции в системе 2SO 2 (г) + О 2 (г) 2SO 3 (r) если объем газовой смеси уменьшится в три раза? В какую сторону сместится равновесие системы?
Решение. Обозначим концентрации реагирующих веществ: =а, =b, =с. Согласно закону действующих масс, скорости прямой и обратной реакций до изменения объема равны
v пр = Ка 2 b, v обр = К 1 с 2
После уменьшения объема гомогенной системы в три раза концентрация каждого из реагирующих веществ увеличится в три раза: = 3а, [О 2 ] = 3b; = 3с. При новых концентрациях скорости v" np прямой и обратной реакций:
v" np = K(3a) 2 (3b) = 27 Ka 2 b; v o 6 p = K 1 (3c) 2 = 9K 1 c 2 .
![]() ;
; ![]()
Следовательно, скорость прямой реакции увеличилась в 27 раз, а обратной - только в девять раз. Равновесие системы сместилось в сторону образования SO 3 .
Пример 6. Вычислите, во сколько раз увеличится скорость реакции, протекающей в газовой фазе, при повышении температуры от 30 до 70 0 С, если температурный коэффициент реакции равен 2.
Решение. Зависимость скорости химической реакции от температуры определяется эмпирическим правилом Вант-Гоффа по формуле
Следовательно, скорость реакции при 70°С большескорости реакции при 30° С в 16 раз.
Пример 7. Константа равновесия гомогенной системы
СО(г) + Н 2 О(г) СО 2 (г) + Н 2 (г) при 850°С равна 1. Вычислите концентрации всех веществ при равновесии, если исходные концентрации: [СО] ИСХ = 3 моль/л, [Н 2 О] ИСХ = 2 моль/л.
Решение. При равновесии скорости прямой и обратной реакций равны, а отношение констант этих скоростей постоянно и называется константой равновесия данной системы:
V np = К 1 [СО][Н 2 О]; V o б p = К 2 [СО 2 ][Н 2 ];
![]()
В условии задачи даны исходные концентрации, тогда как в выражение К р входят только равновесные концентрации всех веществ системы. Предположим, что к моменту равновесия концентрация [СО 2 ] Р = х моль/л. Согласно уравнению системы число молей образовавшегося водорода при этом будет также х моль/л. По столько же молей (х моль/л) СО и Н 2 О расходуется для образования по х молей СО 2 и Н 2 . Следовательно, равновесные концентрации всех четырех веществ (моль/л):
[СО 2 ] Р = [Н 2 ] р = х; [СО] Р = (3 –х); P =(2-х).
Зная константу равновесия, находим значение х, а затем исходные концентрации всех веществ:
![]() ; х 2 =6-2х-3х + х 2
; 5х = 6, л = 1,2 моль/л.
; х 2 =6-2х-3х + х 2
; 5х = 6, л = 1,2 моль/л.
Лекция 3
Химическое равновесие. Закон действующих масс. Константа химического равновесия и способы ее выражения.
Химическое равновесие
В большинстве случаев химические реакции не протекают так глубоко, чтобы реагенты полностью превратились в продукты. Реакции идут до равновесия, при котором в системе имеются как продукты, так и непрореагировавшие исходные вещества, и не наблюдается дальнейшей тенденции к изменению их концентраций. Иногда количество продукта в равновесной смеси настолько превышает количество не вступивших в реакцию исходных веществ, что с практической точки зрения реакция завершается. Практически до конца доходят только такие реакции, при которых как минимум один из продуктов удаляется из сферы реакции (например, выпадает в осадок или выделяется из раствора в виде газа). Но во множестве важных случаев реакционная смесь при равновесии содержит значительные концентрации как продуктов, так и исходных веществ.
Химическое равновесие – это термодинамическое равновесие в системе, в которой возможны прямые и обратные химические реакции.
Существуют термодинамический и кинетический критерии химического равновесия. С кинетической точки зрения при химическом равновесии скорости всех реакций, идущих в двух противоположных направлениях, равны между собой, поэтому в системе не наблюдается изменения макроскопических параметров, в том числе концентраций реагирующих веществ.
С термодинамической точки зрения химическое равновесие характеризуется достижением минимального и не изменяющегося во времени значения энергии Гиббса (или энергии Гельмгольца).
Знание основных закономерностей учения о химическом равновесии совершенно необходимо химику-технологу. В промышленности, например, на химико-фармацевтических заводах, бесполезно строить сложные установки для получения тех или иных веществ, если термодинамические расчёты показывают, что реакция имеет тенденцию идти в “неправильном” направлении. Кроме того, при определении экономичности и рентабельности производства необходимо знать, как получить максимальный выход целевого продукта.
Подлинный механизм как прямой, так и обратной реакции во многих случаях сложен и часто в деталях или полностью не известен. К счастью для химиков, для того, чтобы получить правильные выводы о протекании химических процессов, нет необходимости знать настоящий механизм реакции.
Предсказание направления химической реакции, а также вычисление теоретического равновесного выхода её продуктов и состава равновесной реакционной смеси в зависимости от исходного состава, температуры и давления и является главной задачей учения о химическом равновесии.
Константа равновесия
Произвольную обратимую химическую реакцию можно описать уравнением вида:
aA + bB Û dD + eE
В соответствии с законом действующих масс в простейшем случае скорость прямой реакции связана с концентрациями исходных веществ уравнением
vпр = k пр С Аа С Вb,
а скорость обратной реакции - с концентрациями продуктов уравнением
vобр = kобр С Dd С Ee .
При достижении равновесия эти скорости равны друг другу:
vпр = vобр
Отношение друг к другу констант скорости прямой и обратной реакций будет равно константе равновесия :
Так как это выражение основано на учёте количества реагентов и продуктов реакции, оно является математической записью закона действующих масс для обратимых реакций .
Константа равновесия, выраженная через концентрации реагирующих веществ, называется концентрационной и обозначается Кс . Для более строгого рассмотрения следует вместо концентраций использовать термодинамические активности веществ а = fC (где f - коэффициент активности). При этом речь идёт о так называемой термодинамической константе равновесия
При малых концентрациях, когда коэффициенты активности исходных веществ и продуктов близки к единице, Кс и Ка практически равны друг другу.
Константа равновесия реакции, протекающей в газовой фазе, может быть выражена через парциальные давления р веществ, участвующих в реакции:
Между Кр и Кс существует соотношение, которое можно вывести таким образом. Выразим парциальные давления веществ через их концентрации с помощью уравнения Менделеева - Клапейрона:
pV = nRT ,
откуда p = (n /V )RT = CRT .
Тогда для реакции в общем виде после замены парциальных давлений на концентрации получим
Заменяя выражение (d + с) - (а + b) на равное ему D n , получим окончательное выражение
Кр = Кс (RT )D n или Кс = Кр (RT )-D n ,
где D n - изменение числа молей газообразных веществ в ходе реакции:
D n = å ni прод (г) - å ni исх (г) ).
Если D n = 0, т. е. процесс идёт без изменения числа молей газообразных веществ, и Кр = Кс .
Например, для реакции гидратации этилена, протекающей в газовой фазе:
C2H4 (г) + H2O (г) Û C2H5OH (г),
В данном случае D n = 1 - (1 + 1) = -1. Значит, соотношение между константами может быть выражено таким уравнением:
Кр = Кс (RT )- 1 или Кс = Кр RT .
Таким образом, зная Кр этой реакции при каждой данной температуре, можно вычислить значение Кс и наоборот.
Расчёты с применением констант равновесия
Константы равновесия используются главным образом для получения ответов на следующие вопросы:
1. Должна ли самопроизвольно протекать реакция при определённых условиях?
2. Какова будет концентрация продуктов (равновесный выход) после установления в системе равновесия?
Определение направления протекания обратимых реакций
Так как константа равновесия представляет собой отношение констант скорости прямой и обратной реакций, то само её значение говорит о направлении процесса. Так, если константа равновесия больше единицы, то при данных условиях самопроизвольно будет осуществляться прямая реакция, если же она меньше единицы - обратная реакция.
В соответствии с принципом Ле-Шателье положение равновесия может быть смещено при изменении условий, в которых протекает реакция. Поэтому в общем случае можно оценить смещение равновесия при изменении соотношения начальных количеств веществ, участвующих в реакции. Если соотношение концентраций реагирующих веществ в начальный момент обозначить P :
то по соотношению Z и Кс можно предсказать направление реакции при заданных условиях эксперимента:
при P < K самопроизвольно протекает прямая реакция;
при P > K самопроизвольно протекает обратная реакция;
при P = K система находится в равновесии.
Чем больше значение константы равновесия отличается от единицы, тем в большей степени равновесие реакции сдвинуто в соответствующую сторону (вправо при К > 1 и влево при К < 1).
Факторы, влияющие на равновесие. Принцип Ле-Шателье -
Брауна
При равновесии прямая и обратная реакции точно компенсируют друг друга. Но насколько чувствительна эта компенсация к изменениям условий реакций? Каким способом можно изменить состояние равновесия? Эти вопросы имеют большое практическое значение, если требуется повысить выход полезного продукта реакции, например, лекарственного вещества, или, наоборот, уменьшить выход нежелательного продукта.
Если имеется возможность непрерывно выводить продукты из реакционной смеси (раствора) в виде газа или осадка, а также с помощью таких технологических операций, как вымораживание, вымывание и пр., то тем самым реагирующая система может постоянно удерживаться в неравновесном, несбалансированном состоянии. В этих условиях возникает необходимость во все новых количествах реагентов и происходит непрерывное образование продуктов. Такой способ нарушения равновесия в сторону получения желаемого продукта осуществляется без изменения константы равновесия. Но часто можно повысить выход продуктов, увеличивая константу равновесия.
Один из способов увеличения константы равновесия - изменение температуры . Так как в большинстве случаев скорости прямой и обратной реакции зависят от Т , константа равновесия тоже проявляет зависимость от температуры. Строго говоря, изменение температуры одновременно изменяет скорость и прямой, и обратной реакции. Но, если повышение температуры ускоряет прямую реакцию в большей степени, чем обратную, то константа равновесия при этом увеличится.
Температурная зависимость положения равновесия является одним из примеров общего принципа подвижного химического равновесия, называемого принципом Ле-Шателье (или Ле-Шателье - Брауна):
Если на систему, находящуюся в состоянии химического равновесия, оказывается внешнее воздействие, положение равновесия смещается в такую сторону, чтобы противодействовать эффекту этого воздействия .
Принцип Ле-Шателье относится и к другим способам воздействия на равновесие, например, к изменению давления, но он имеет качественный характер. Количественно зависимость константы равновесия реакции от различных факторов выражается уравнениями изотермы, изобары и изохоры химической реакции, выведенными Я. Вант-Гоффом.
Влияние на равновесие начального состава реакционной
смеси. Уравнение изотермы химической реакции
Максимальная работа реакции, идущей в газовой фазе при постоянных температуре и давлении, является алгебраической суммой работ, совершённых всеми участвующими в реакции веществами при переходе от начальных парциальных давлений к равновесным.
Рассмотрим газовую реакцию, выражаемую в общем виде уравнением
aA + bB Û dD + eE.
Давление р в системе с помощью уравнения Менделеева - Клапейрона может быть выражено через объём V и температуру T :
p = nRT /V ,
откуда, принимая, что суммарное число молей всех компонентов равно 1, получаем для работы расширения
pdV = (RT /V )dV ,
Так как максимальная полезная работа может быть вычислена при интегрировании выражения: V2
А’max = ò pdV ,
получаем
а так как А’max = -D Gr ,
то можно записать:
Для процессов, идущих при постоянном объёме, можно получить аналогичные выражения, в которые входит максимальная работа и изменение энергии Гельмгольца в ходе реакции. При этом парциальные давления заменяются начальными концентрациями веществ:
Уравнения (4.1) - (4.4), выведенные Я. Вант-Гоффом, называются уравнениями изотермы химической реакции . Они дают возможность определить, в каком направлении и до какого предела может протекать реакция в рассматриваемых условиях при заданном составе реакционной смеси при постоянной температуре.
Для стандартных условий, когда исходные парциальные давления (или исходные концентрации или активности) всех веществ-участников реакции равны единице, уравнения изотермы будут выглядеть так:
А ’max = RT ln Kp ; D Gor = - RT ln Kp (4.5)
А max = RT ln K с ; D А o r = - RT ln K с .
Отсюда следует, что определяя стандартную величину D Gor или D А o r для реакции, можно легко вычислить её константу равновесия.
Влияние на равновесный выход изменения объёма
и давления реакционной смеси
Для реакций, идущих в газовой фазе, об изменении объёма реакционной смеси можно судить по изменению числа молей реагирующих веществ
D n = å ni прод - å ni исх
Возможны три случая, соответствующих различным типам химических реакций:
а) D n < 0 (реакция идет с уменьшением объёма). Например, реакция синтеза аммиака :
N2 (г) + 3H2 (г) Û 2NH3 (г) ; D n = 2 - (1 + 3) = -2
В соответствии с принципом Ле-Шателье уменьшение объёма (при увеличении давления) будет сдвигать равновесие этой и подобных реакций вправо, а увеличение объёма (при уменьшении давления) - влево.
б) D n > 0 (реакция идет с увеличением объёма). Например, реакция разложения метанола:
CH3OH (г) Û CO (г) + 2H2 (г) ; D n = (1 + 2) - 1 = 2
В этом случае уменьшение объёма (или увеличение давления) будет сдвигать равновесие влево, а увеличение объёма (при уменьшении давления) - вправо.
в) D n = 0 (реакция идет без изменения объёма). Например, реакция хлора с бромоводородом:
Cl2 (г) + 2HBr (г) Û Br2 (г) + 2HCl (г) ; D n = (1 + 2) - (1 + 2) = 0
На выходе продуктов таких реакций изменение объёма (давления) реакционной смеси не сказывается.
Химическое равновесие в гетерогенных системах
Рассмотренные ранее закономерности относятся, главным образом, к гомогенным реакциям, т. е. к реакциям с участием веществ, находящихся в одном физическом состоянии - в виде газа или в виде раствора. Равновесия, в которых принимают участие вещества, находящиеся в двух или нескольких физических состояниях (например, газ с жидкостью или с твёрдым веществом), называются гетерогенными равновесиями.
В качестве примера рассмотрим разложение карбоната кальция CaCO3, используемого в фармации в качестве антацидного средства (сниж кислотность). Это удобная модель для рассмотрения разложения различных твёрдых веществ, в том числе и лекарственных, идущего с образованием газообразных продуктов:
CaCO3 (т) Û CaO (т) + CO2 (г)
В соответствии с законом действующих масс выражение для константы равновесия этой реакции можно написать так:
Парциальные давления CaO и CaCO3 в газовой фазе, во-первых, очень малы, а во-вторых, остаются практически постоянными в любой момент протекания реакции. Это значит, что пока твёрдые CaCO3 и CaO находятся в контакте с газом, их влияние на равновесие будет неизменным. В этом случае константа равновесия не зависит от количества твёрдой фазы. Можно разделить обе части выражения для константы равновесия на величину p CaO/p CaCO3 и принять, что
K ’ p = p CO2 ,
где K ’ p = Kp p CaC03/p CaO - модифицированная константа равновесия; при этом парциальные давления CaCO3 и CaO входят в величину K ’ p в неявном виде.
Если парциальное давление СО2 над CaCO3, при данной температуре поддерживается меньшим, чем значение K ’ p , то весь CaCO3 превратится в CaO и CO2; если же парциальное давление p CO2 больше, чем K ’ p , то весь СaO превратится в CaCO3. Равновесное же парциальное давление CO2, равное K ’ p при данной температуре, называется давлением диссоциации .
При достижении давления СО2 1 атм равновесие в данной реакции сдвигается в сторону диссоциации СаСО3, т. е. разложения карбоната кальция. это происходит при температуре 897оС:
Подобные рассуждения и понятие давления диссоциации могут быть распространены и на другие гетерогенные реакции с участием твёрдых веществ. В том случае, когда лекарственное вещество (в порошке или в таблетках) может реагировать с газами, находящимися в воздухе (H2O, O2, CO2), или разлагаться с их выделением, необходимо следить, чтобы парциальное давление этих газов и паров в атмосфере склада было меньше, чем давление диссоциации (или соответствующая константа равновесия K ’ p ).
Если рассматривать обратимую газовую реакцию и считать газы идеальными, то выполняются следующие соотношения:
1) Закон Менделеева–Клапейрона pV = nRT (или p i V = n i RT).
Где
 ,
(19)
,
(19)
Отсюда можно получить следующие соотношения, показывающие взаимосвязь между k р и k с
 ,
но т.к. p i
= c i RT,
то получим:
,
но т.к. p i
= c i RT,
то получим:
 .
.
Здесь
– изменение числа молей газообразных
веществ в результате протекания одного
пробега данной реакции.  (20)
(20)
k р = k с (RT) . (21)
Если
парциальные давления компонентов
выражены в атмосферах, а концентрации
в
 ,
то в соотношение, (21) связывающее k р
и k с,
вместо R следует ставить величину
R = 0,082
,
то в соотношение, (21) связывающее k р
и k с,
вместо R следует ставить величину
R = 0,082
 .
.
k р не зависит от давления и концентрации, k с не зависит от концентрации и от давления.
3.5 Равновесие в гетерогенных реакциях.
До сих пор речь шла о гомогенных реакциях (протекающих в одной фазе). Рассмотрим гетерогенные реакции, в которых не все вещества находятся в газообразном состоянии. В случае гетерогенных систем, в которых жидкие или твёрдые вещества не образуют растворов друг с другом и с газообразными веществами, химические потенциалы этих конденсированных веществ при постоянной температуре будут постоянными, также как и давление насыщенных паров над каждым из таких веществ в смеси. Поэтому в выражения для констант равновесия входят давления только газообразных веществ.
СаО тв. + СО 2 газ СаСО 3 тв. (22)

В случае, если в гетерогенной реакции принимают участие растворы, в выражения для констант равновесия будут входить активности (концентрации) этих веществ.
3.6 Принцип Ле-Шателье.
Как отмечалось ранее, химические равновесия являются динамичными и подвижными. При изменении внешних условий может происходить сдвиг равновесия в сторону образования либо продуктов реакции, либо исходных веществ. Впервые принцип смещения равновесия сформулировал А. Ле-Шателье.
Принцип Ле–Шателье : если на систему, находящуюся в равновесии, оказывать внешнее воздействие, то равновесие смещается в сторону того процесса, который уменьшает это воздействие.
Теоретически этот принцип был выдвинут Ф. Брауном и теперь известен, как принцип Ле-Шателье – Брауна.
Обычно в качестве внешних факторов, влияющих на состояние равновесия, рассматривают влияние температуры, давления и изменения концентрации реагирующих веществ. Например, с повышением температуры равновесие смещается в сторону эндотермической реакции, протекающей с поглощением теплоты. Уменьшение давления приводит к смещению равновесия в сторону реакции, протекающей с увеличением числа молей газообразных веществ.
Пример 3 .2 Рассмотрим реакцию
 (
( )
)
Увеличим температуру: так как реакция экзотермическая, т. е. идёт с выделением тепла, равновеие смещается в сторону исходных веществ (обратная реакция идёт с поглощением тепла).
Увеличим давление: так как прямая реакция идёт с уменьшением числа молей газобразных веществ (т.е. объем уменьшается), то равновесие смещается в сторону продуктов реакции.



