Строение карбоксильной группы и карбоксилат-аниона. Карбоновые кислоты Строение карбоксильной группы
Карбоксильная группа сочетает в себе две функциональные группы – карбонил и гидроксил, взаимно влияющие друг на друга. Это влияние передается по системе сопряжения sp 2 -атомов O–C–O.
Электронное строение группы –СООН придает карбоновым кислотам характерные химические и физические свойства.
1. Смещение электронной плотности к карбонильному атому кислорода вызывает дополнительную (по сравнению со спиртами и фенолами) поляризацию связи О–Н, что определяет подвижность водородного атома (кислотные свойства
).
В водном растворе карбоновые кислоты диссоциируют на ионы:
Однако карбоновые кислоты в целом – слабые кислоты: в водных растворах их соли сильно гидролизованы.
Видеоопыт "Карбоновые кислоты – слабые электролиты".
2. Пониженная электронная плотность (δ+) на атоме углерода в карбоксильной группе обусловливает возможность реакций нуклеофильного замещения группы -ОН.
3. Группа -СООН за счет положительного заряда на атоме углерода снижает электронную плотность на связанном с ней углеводородном радикале, т.е. является по отношению к нему электроноакцепторным заместителем. В случае предельных кислот карбоксильная группа проявляет -I -эффект , а в непредельных (например, CH 2 =CH-COOH) и ароматических (С 6 Н 5 -СООН) – -I и -М -эффекты .
4. Карбоксильная группа, являясь электроноакцептором, вызывает дополнительную поляризацию связи С–Н в соседнем (α-) положении и увеличивает подвижность α-водородного атома в реакциях замещения по углеводородному радикалу.
См. также "Реакционные центры в молекулах карбоновых кислот".
Атомы водорода и кислорода в карбоксильной группе -СООН способны к образованию межмолекулярных водородных связей, что во многом определяет физические свойства карбоновых кислот.
Вследствие ассоциации молекул карбоновые кислоты имеют высокие температуры кипения и плавления. При нормальных условиях они существуют в жидком или твёрдом состоянии.
Например, простейший представитель – муравьиная кислота НСООН – бесцветная жидкость с т. кип. 101 °С, а чистая безводная уксусная кислота CH 3 COOH при охлаждении до 16,8 °С превращается в прозрачные кристаллы, напоминающие лед (отсюда ее название ледяная кислота
).
Видеоопыт "Ледяная уксусная кислота".
Простейшая ароматическая кислота - бензойная C 6 H 5 COOH (т. пл. 122,4°С) - легко возгоняется, т.е. переходит в газообразное состояние, минуя жидкое. При охлаждении её пары сублимирутся в кристаллы. Это свойство используется для очистки вещества от примесей.
Видеоопыт "Возгонка бензойной кислоты".
Растворимость карбоновых кислот в воде обусловлена образованием межмолекулярных водородных связей с растворителем:
Низшие гомологи С 1 -С 3 смешиваются с водой в любых соотношениях. С увеличением углеводородного радикала растворимость кислот в воде уменьшается. Высшие кислоты, например, пальмитиновая C 15 H 31 COOH и стеариновая C 17 H 35 COOH – бесцветные твердые вещества, не растворимые в воде.
КАРБОКСИЛЬНАЯ ГРУППА
карбоксигруппа, карбоксил, - одновалентная группа
характерная для карбоновых кислот.
Состоит из карбонильной
и гидроксильной (-ОН) групп (отсюда назв.: карб + оксил).
Большой энциклопедический политехнический словарь . 2004 .
Смотреть что такое "КАРБОКСИЛЬНАЯ ГРУППА" в других словарях:
- (карбоксил) СООН функциональная одновалентная группировка, входящая в состав карбоновых кислот и определяющая их кислотные свойства. Строение карбоксильной группы … Википедия
КАРБОКСИЛ, КАРБОКСИЛЬНАЯ группа [карбо… + гр. кислый] – одноатомная группа COOH, характеризующая органические, т. наз. карбоновые кислоты, например, уксусная кислота CH3COOH Большой словарь иностранных слов. Издательство «ИДДК», 2007 … Словарь иностранных слов русского языка
КАРБОКСИЛЬНАЯ ГРУППА - (карбоксил), СООН кислотная группа С, присутствующая в (см.); число К. г. определяет основность кислоты … Большая политехническая энциклопедия
Карбоксил, функциональная одновалентная группировка Карбоновые кислоты) и определяющая их кислотные свойства … Большая советская энциклопедия
карбоксильная группа - карбоксил … Cловарь химических синонимов I
A одновалентная гр. СООН, присутствие которой определяет принадлежность орг. соединения к карбоновым кислотам. Пример: уксусная кислота СНзСООН. При замещении в К. водорода металлом образуются соли, при замещении водородастиртовым радикалом… … Геологическая энциклопедия
Бензил ацетат имеет эфирную функциональную группу (показанно красным), ацетильную группу (зелёная) и бензильную группу (оранжевая). Функциональная группа структурный фрагмент органическо … Википедия
функциональная группа - Functional Group Функциональная группа Cтруктурный фрагмент молекулы, характерный для данного класса органических соединений и определяющий его химические свойства. Примеры функциональных групп: азидная, гидроксильная, карбонильная,… … Толковый англо-русский словарь по нанотехнологии. - М.
Карбоновыми кислотами называют производные углеводородов, содержащие одну или несколько карбоксильных групп.
Число карбоксильных групп характеризует основность кислоты.
В зависимости от количества карбоксильных групп карбоновые кислоты подразделяются на одноосновные карбоновые кислоты (содержат одну карбоксильную группу), двухосновные (содержат две карбоксильные группы) и многоосновные кислоты.
В зависимости от вида радикала, связанного с карбоксильной группой, карбоновые кислоты делятся на предельные, непредельные и ароматические. Предельные и непредельные кислоты объединяют под общим названием кислоты алифатического или жирного ряда.
Одноосновные карбоновые кислоты
1.1 Гомологический ряд и номенклатура
Гомологический ряд одноосновных предельных карбоновых кислот (иногда их называют жирными кислотами) начинается с муравьиной кислоты
Формула гомологического ряда
Номенклатура ИЮПАК разрешает сохранять для многих кислот их тривиальные названия, которые обычно указывают на природный источник, из которого была выделена та или иная кислота, например, муравьиная, уксусная, масляная, валериановая и т.д.
Для более сложных случаев названия кислот производят от названия углеводородов с тем же числом атомов углерода, что и в молекуле кислоты, с добавлением окончания -овая и слова кислота. Муравьиная кислота Н-СООН называется метановой кислотой, уксусная кислота СН 3 -СООН - этановой кислотой и т. д.
Таким образом, кислоты рассматриваются как производные углеводородов, одно звено которых превращено в карбоксил:

При составлении названий кислот с разветвленной цепью по рациональной номенклатуре их рассматривают как производные уксусной кислоты, в молекуле которой атомы водорода замещены радикалами, например, триметилуксусная кислота (СН 3) 3 С – СООН.
1.2 Физические свойства карбоновых кислот
Только с чисто формальных позиций можно рассматривать карбоксильную группу как комбинацию карбонильной и гидроксильной функций. Фактически их взаимное влияние друг на друга таково, что полностью изменяет их свойства.
Обычная для карбонила поляризация двойной связи С=0 сильно возрастает за счет дополнительного стягивания свободной электронной пары с соседнего атома кислорода гидроксильной группы:
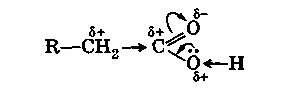
Следствием этого является значительное ослабление связи О-Н в гидроксиле и легкость отщепления атома водорода от него в виде протона (Н +). Появление пониженной электронной плотности (δ+) на центральном углеродном атоме карбоксила приводит также к стягиванию σ-электронов соседней связи С-С к карбоксильной группе и появлению (как у альдегидов и кетонов) пониженной электронной плотности (δ +) на α-углеродном атоме кислоты.
Все карбоновые кислоты обладают кислой реакцией (обнаруживается индикаторами) и образуют соли с гидроксидами, оксидами и карбонатами металлов и с активными металлами:
Карбоновые кислоты в большинстве случаев в водном растворе диссоциированы лишь в малой степени и являются слабыми кислотами, значительно уступая таким кислотам, как соляная, азотная и серная. Так, при растворении одного моля в 16 л воды степень диссоциации муравьиной кислоты равна 0,06, уксусной кислоты - 0,0167, в то время как соляная кислота при таком разбавлении диссоциирована почти полностью.
Для большинства одноосновных карбоновых кислот рК а = 4,8, только муравьиная кислота имеет меньшую величину рК а (около 3,7), что объясняется отсутствием электронодонорного эффекта алкильных групп.
В безводных минеральных кислотах карбоновые кислоты протонируются по кислороду с образованием карбкатионов:

Сдвиг электронной плотности в молекуле недиссоциированной карбоновой кислоты, о котором говорилось выше, понижает электронную плотность на гидроксильном атоме кислорода и повышает ее на карбонильном. Этот сдвиг еще больше увеличивается в анионе кислоты:

Результатом сдвига является полное выравнивание зарядов в анионе, который фактически существует в форме А - резонанс карбоксилат-аниона.
Первые четыре представителя ряда карбоновых кислот - подвижные жидкости, смешивающиеся с водой во всех отношениях. Кислоты, в молекуле которых содержится от пяти до девяти атомов углерода (а также изомасляная кислота), - маслянистые жидкости, растворимость их в воде невелика.
Высшие кислоты (от С 10) - твердые тела, практически нерастворимы в воде, при перегонке в обычных условиях они разлагаются.
Муравьиная, уксусная и пропионовая кислоты имеют острый запах; средние члены ряда обладают неприятным запахом, высшие кислоты запаха не имеют.

На физических свойствах карбоновых кислот сказывается значительная степень ассоциации вследствие образования водородных связей. Кислоты образуют прочные водородные связи, так как связи О-Н в них сильно поляризованы. Кроме того, карбоновые кислоты способны образовывать водородные связи с участием атома кислорода карбонильного диполя, обладающего значительной электроотрицательностью. Действительно, в твердом и жидком состоянии карбоновые кислоты существуют в основном в виде циклических димеров:
Такие димерные структуры сохраняются в некоторой степени даже в газообразном состоянии и в разбавленных растворах в неполярных растворителях.
Карбоксильная группа сочетает в себе две функциональные группы - карбонил и гидроксил, взаимно влияющие друг на друга:
Кислотные свойства карбоновых кислот обусловлены смещением электронной плотности к карбонильному кислороду и вызванной этим дополнительной (по сравнению со спиртами) поляризации связи О–Н.
В водном растворе карбоновые кислоты диссоциируют на ионы:
Производные карбоновых кислот: соли, сложные эфиры, хлорангидриды, ангидриды, амиды, нитрилы, их получение.
Карбоновые кислоты проявляют высокую реакционную способность. Они вступают в реакции с различными веществами и образуют разнообразные соединения, среди которых большое значение имеют функциональные производные, т.е. соединения, полученные в результате реакций по карбоксильной группе.
1. Образование солей
а) при взаимодействии с металлами:
2RCOOH + Mg ® (RCOO) 2 Mg + H 2
б) в реакциях с гидроксидами металлов:
2RCOOH + NaOH ® RCOONa + H 2 O
2. Образование сложных эфиров R"–COOR":

Реакция образования сложного эфира из кислоты и спирта называется реакцией этерификации (от лат. ether - эфир).
3. Образование амидов:

Вместо карбоновых кислот чаще используют их галогенангидриды:

Амиды образуются также при взаимодействии карбоновых кислот (их галогенангидридов или ангидридов) с органическими производными аммиака (аминами):

Амиды играют важную роль в природе. Молекулы природных пептидов и белков построены из a-аминокислот с участием амидных групп - пептидных связей
Нитри́лы - органические соединения общей формулы R-C≡N, рассматривают как производные карбоновых кислот (продукты дегидратации амидов) и именуют как производные соответствующих карбоновых кислот, например, CH 3 C≡N - ацетонитрил (нитрил уксусной кислоты), C 6 H 5 CN - бензонитрил (нитрил бензойной кислоты).
Ангидриды карбоновых кислот можно рассматривать как продукт конденсации двух групп -COOH:
R 1 -COOH + HOOC-R 2 = R 1 -(CO)O(OC)-R 2 + H 2 O
[ее рисунок, (гидр43)]
Карбоксильная группа представляет собой плоскую сопряженную систему, в которой возникает р,-сопряжение при взаимодействии р z -орбитали атома кислорода гидроксогруппы с -связью. Наличие р,-сопряжения в карбоксильной группе карбоновых кислот способствует равномерному распределению отрицательного заряда в ацилат-ионе, образующемся при отщеплении протона.
[ацилат-ион, (гидр44)]
Равномерное распределение отрицательного заряда в ацилат-ионе показывают следующим образом: (гидр45)
Наличие р,-сопряжения в карбоксильной группе карбоновых кислот значительно повышает кислотные свойства карбоновых кислот по сравнению со спиртами.
С 2 Н 5 ОН рК а =18
СН 3 СООН рК а =4,76
В кабоновых кислотах частичный положительный заряд на карбонильном атоме углерода меньше, чем в альдегидах и кетонах, поэтому кислота менее активна к восприятию атаки нуклеофильного реагента. Соответственно, реакции нуклеофильного присоединения более характерны для альдегидов и кетонов.
R-гидрофобная часть молекулы;
СООН-гидрофильная часть молекулы.
С увеличением длины углеводородного радикала понижается растворимость кислот, степень гидратированности и стабильность ацилат-аниона. Это приводит к уменьшению силы карбоновых кислот.
В карбоновых кислотах выделяют следующие реакционные центры: (гидр46)
1. основный нуклеофильный центр;
2. электрофильный центр;
3. ОН-кислотный центр;
4. СН-кислотный центр;
Химические свойства карбоновых кислот
I. Реакции диссоциации.
[карб. к-та+вода= ацилат-ион+ H 3 O + , (гидр47)]
II. Реакции галогенирования (реакции в СН-кислотном центре)
[пропионовая к-та+ Br 2 =α-бромпропионовая +HBr, (гидр48)]
III. Реакции декарбоксилирования - реакции, в ходе которых происходит удаление углекислого газа из карбоксильной группы, приводящее к разрушению карбоксильной группы.
In vitro pеакции декарбоксилирования протекают при нагревании; in vivo – с участием ферментов-декарбоксилаз.
1. [пропановая к-та= угл. газ+ этан, (гидр49)]
2. В организме декарбоксилирование дикарбоновых кислот протекает ступенчато: [янтарная= пропионовая + угл. газ=этан+ угл. газ, (гидр50)]
3. В организме также протекает окислительное декарбоксилирование, в частности, ПВК в митохондриях. С участием декарбоксилазы, дегидрогеназы и кофермента А (HS-KoA). [ПВК= этаналь+ угл. газ= ацетил-Ко-А+ НАДН+ Н + , (гидр51)]
Ацетил-КоА, будучи активным соединением, вовлекается в цикл Кребса.
IV. Реакции этерификации – нуклеофильного замещения (S N) у sр 2 -гибридизованного атома углерода. [уксусная к-та+ метанол= метилацетат, (гидр52)]
Механизм реакции нуклеофильного замещения, (гидр53)
V. Реакции окисления.
Рассмотрим на примере гидроксокислот. Окисление гидроксокислот протекает аналогично окислению вторичных спиртов с участием ферментов-дегидрогеназ.
1. [молочная= ПВК +НАДН+ Н + , (гидр54)]
2. [β-гидроксимасляная= ацетоуксусная +НАДН+ Н + , (гидр55)]
Т.о., при окислении гидроксокислот с участием ферментов-дегидрогеназ образуются кетокислоты.
Пути превращения ацетоуксусной кислоты в организме:
В норме она подвергается гидролитическому расщеплению с участием фермента гидролазы, при этом образуются 2 молекулы уксусной кислоты: [ацетоуксусная+ вода=2 уксусной к-ты, (гидр56)]
При патологии ацетоуксусная кислота декарбоксилируется с образованием ацетона: [ацетоуксусная к-та=ацетон+ угл. газ, (гидр57)]
Кетоновые тела накапливаются в крови больных сахарным, обнаруживаются в моче, они токсичны, особенно для нервной системы.



